1 . 基态锇原子( )的价电子排布式为
)的价电子排布式为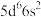 。氧化物
。氧化物 常作烯烃醇化的氧化剂,其重要的氮基锇酸盐有
常作烯烃醇化的氧化剂,其重要的氮基锇酸盐有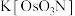 。有关反应如下:
。有关反应如下:
反应I:
反应Ⅱ:
 )的价电子排布式为
)的价电子排布式为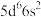 。氧化物
。氧化物 常作烯烃醇化的氧化剂,其重要的氮基锇酸盐有
常作烯烃醇化的氧化剂,其重要的氮基锇酸盐有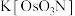 。有关反应如下:
。有关反应如下:反应I:

反应Ⅱ:

反应IⅢ:
A. 的立体异构分子中不存在手性分子 的立体异构分子中不存在手性分子 |
B.反应I中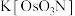 的 的 的化合价为+8 的化合价为+8 |
| C.反应Ⅱ中氧化产物与还原产物的物质的量之比为1∶1 |
D.由反应Ⅲ可推测氧化性: 强于酸性 强于酸性 溶液 溶液 |
您最近一年使用:0次
名校
解题方法
2 . 某天然气电厂对废气回收利用,在催化剂作用下重新合成天然气作为燃料再利用,反应机理如图所示。下列说法错误的是
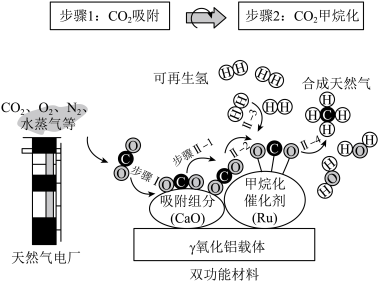
A.步骤 -2中存在极性键的断裂、Ⅱ-3中存在非极性键断裂 -2中存在极性键的断裂、Ⅱ-3中存在非极性键断裂 |
| B.步骤Ⅱ-4存在极性键生成 |
| C.当消耗1molCO2生成1molCH4时,转移8mol电子 |
| D.CO2、N2、CH4分子中各原子均满足8电子稳定结构 |
您最近一年使用:0次
2024-04-03更新
|
225次组卷
|
2卷引用:江西省赣州市兴国中学2023-2024学年高一下学期第一次阶段性考试化学试题
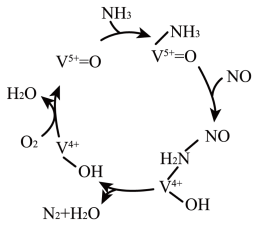
3 . 研究人员发现在某种含钒催化剂的作用下,NO可被 还原为
还原为 ,从而降低含氮气体造成的空气污染,反应机理如图所示,下列说法错误的是
,从而降低含氮气体造成的空气污染,反应机理如图所示,下列说法错误的是
 还原为
还原为 ,从而降低含氮气体造成的空气污染,反应机理如图所示,下列说法错误的是
,从而降低含氮气体造成的空气污染,反应机理如图所示,下列说法错误的是
A. 价电子排布式为 价电子排布式为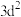 ,未成对电子数是2 ,未成对电子数是2 |
B. 和NO分子是极性分子, 和NO分子是极性分子, 为该反应的中间体 为该反应的中间体 |
| C.该转化过程中,氧化剂只有NO |
D.每生成标准状况下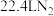 ,转移电子总数为 ,转移电子总数为 |
您最近一年使用:0次
名校
解题方法
4 . 《环境科学》刊发了我国科研部门采用零价铁活化过硫酸钠( ,其中S为+6价)去除废水中的正五价砷[As(V)]的研究成果,其反应机制模型如图所示。设阿伏加德罗常数的值为
,其中S为+6价)去除废水中的正五价砷[As(V)]的研究成果,其反应机制模型如图所示。设阿伏加德罗常数的值为 ,
,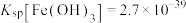 。下列叙述正确的是
。下列叙述正确的是
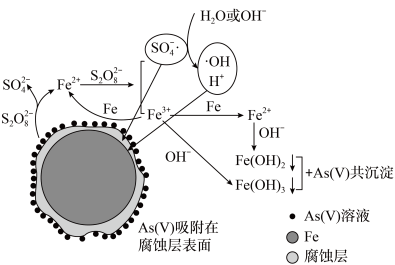
A.1 mol过硫酸钠( )含 )含 个过氧键 个过氧键 |
B.若56 g Fe参加反应,共有 个 个 被还原 被还原 |
C.室温下,中间产物 溶于水所得饱和溶液中 溶于水所得饱和溶液中 为 为 mol⋅L mol⋅L |
| D.pH越小,越有利于去除废水中的正五价砷 |
您最近一年使用:0次
5 . 实验室制取A并进一步制取无水FeCl3的实验装置如图所示。
已知:无水FeCl3在空气中易与水发生作用,加热易升华。
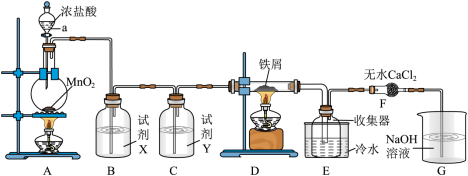
回答下列问题:
(1)仪器a的名称是_______ ,装置A所发生的氧化还原反应中,氧化剂与还原剂的物质的量之比为_______ 。
(2)试剂X是_______ 。
(3)装置F中无水CaCl2的作用是_______
(4)某温度下,将氯气通入G装置中,反应得到NaCl,NaClO和NaClO3的混合溶液,经测定ClO-与ClO 的物质的量之比为4∶1,写出该反应总的离子方程式:
的物质的量之比为4∶1,写出该反应总的离子方程式:_______ 。
已知:无水FeCl3在空气中易与水发生作用,加热易升华。

回答下列问题:
(1)仪器a的名称是
(2)试剂X是
(3)装置F中无水CaCl2的作用是
(4)某温度下,将氯气通入G装置中,反应得到NaCl,NaClO和NaClO3的混合溶液,经测定ClO-与ClO
 的物质的量之比为4∶1,写出该反应总的离子方程式:
的物质的量之比为4∶1,写出该反应总的离子方程式:
您最近一年使用:0次
解题方法
6 .  是光电转化材料。利用钛铁矿(主要成分为
是光电转化材料。利用钛铁矿(主要成分为 ,还含有少量
,还含有少量 等杂质)来制备
等杂质)来制备 ,并回收铁制备难溶于水的黄钾铁矾
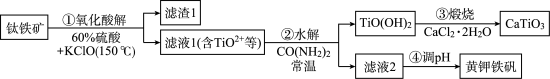
,并回收铁制备难溶于水的黄钾铁矾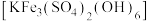 ,制备流程如图,回答下列问题:
,制备流程如图,回答下列问题:
部分原料价格表:
(1) 中Ti的化合价为
中Ti的化合价为_______ 。
(2)步骤①滤渣1的主要成分是_______ ,若氧化酸解的氧化剂用 替代
替代 ,则理论上氧化剂与还原剂物质的量之比为
,则理论上氧化剂与还原剂物质的量之比为_______ ,相同条件下,用 做氧化剂时,其酸解效率较
做氧化剂时,其酸解效率较 低,原因可能是
低,原因可能是_______ 。
(3)已知 在水中能部分水解并有
在水中能部分水解并有 生成,则相关离子方程式为
生成,则相关离子方程式为_______ ;常温下,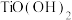
 为
为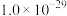 ,滤液1中
,滤液1中 浓度为
浓度为 ,步骤②中要使
,步骤②中要使 水解的转化率达99%,加
水解的转化率达99%,加 时忽略溶液体积变化,则此时溶液的pH应为
时忽略溶液体积变化,则此时溶液的pH应为_______ 。
(4)步骤③反应的化学方程式为_______ ,若在实验室煅烧,用到的实验仪器除了玻璃棒、酒精灯、三脚架及泥三角外,还需要_______ 。
(5)结合信息分析,步骤④调pH最适宜的试剂是_______。
 是光电转化材料。利用钛铁矿(主要成分为
是光电转化材料。利用钛铁矿(主要成分为 ,还含有少量
,还含有少量 等杂质)来制备
等杂质)来制备 ,并回收铁制备难溶于水的黄钾铁矾
,并回收铁制备难溶于水的黄钾铁矾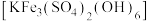 ,制备流程如图,回答下列问题:
,制备流程如图,回答下列问题:
部分原料价格表:
| 物质 | 纯碱(99% ) ) | 氢氧化钾(90% ) ) | 碳酸钾(99% ) ) | 液氨(99.9%) |
| 价格(元/吨) | 1800 | 4000 | 4500 | 25000 |
 中Ti的化合价为
中Ti的化合价为(2)步骤①滤渣1的主要成分是
 替代
替代 ,则理论上氧化剂与还原剂物质的量之比为
,则理论上氧化剂与还原剂物质的量之比为 做氧化剂时,其酸解效率较
做氧化剂时,其酸解效率较 低,原因可能是
低,原因可能是(3)已知
 在水中能部分水解并有
在水中能部分水解并有 生成,则相关离子方程式为
生成,则相关离子方程式为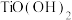
 为
为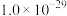 ,滤液1中
,滤液1中 浓度为
浓度为 ,步骤②中要使
,步骤②中要使 水解的转化率达99%,加
水解的转化率达99%,加 时忽略溶液体积变化,则此时溶液的pH应为
时忽略溶液体积变化,则此时溶液的pH应为(4)步骤③反应的化学方程式为
(5)结合信息分析,步骤④调pH最适宜的试剂是_______。
A. | B. | C. | D. |
您最近一年使用:0次
2024-03-28更新
|
111次组卷
|
3卷引用:2024届四川省雅安市高三上学期第一次诊断性考试理综试题
名校
解题方法
7 . 将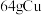 完全溶于一定量浓硝酸,产生的
完全溶于一定量浓硝酸,产生的 、
、 混合气体通入
混合气体通入 的
的 溶液中,气体恰好被
溶液中,气体恰好被 溶液完全吸收,得到
溶液完全吸收,得到 和
和 的混合溶液。则该混合溶液中
的混合溶液。则该混合溶液中 的物质的量为
的物质的量为
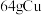 完全溶于一定量浓硝酸,产生的
完全溶于一定量浓硝酸,产生的 、
、 混合气体通入
混合气体通入 的
的 溶液中,气体恰好被
溶液中,气体恰好被 溶液完全吸收,得到
溶液完全吸收,得到 和
和 的混合溶液。则该混合溶液中
的混合溶液。则该混合溶液中 的物质的量为
的物质的量为A.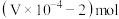 | B. |
C. | D.无法计算 |
您最近一年使用:0次
名校
解题方法
8 . 土壤中的 在硝化细菌的作用下转化为
在硝化细菌的作用下转化为 后,土壤中的
后,土壤中的 进一步将
进一步将 氧化为
氧化为 。在氧气较少的环境下,
。在氧气较少的环境下, 又可以在反硝化细菌的作用下与
又可以在反硝化细菌的作用下与 反应,使氮以
反应,使氮以 形式放出。下列说法
形式放出。下列说法不正确 的是
 在硝化细菌的作用下转化为
在硝化细菌的作用下转化为 后,土壤中的
后,土壤中的 进一步将
进一步将 氧化为
氧化为 。在氧气较少的环境下,
。在氧气较少的环境下, 又可以在反硝化细菌的作用下与
又可以在反硝化细菌的作用下与 反应,使氮以
反应,使氮以 形式放出。下列说法
形式放出。下列说法A. 被氧化为 被氧化为 的过程中, 的过程中, 与 与 的物质的量之比为 的物质的量之比为 |
B.在反硝化过程中,土壤 降低 降低 |
C. 与 与 反应时,每生成 反应时,每生成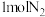 ,转移电子数为 ,转移电子数为 |
| D.适当疏松土壤,有利于提高铵态氮肥的肥效 |
您最近一年使用:0次
名校
9 . 工业上采用电解熔融NaCl制备金属钠的电解方程式为2NaCl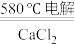 Na+Cl2↑。设NA为阿伏加德罗常数的值,下列说法正确的是
Na+Cl2↑。设NA为阿伏加德罗常数的值,下列说法正确的是
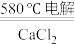 Na+Cl2↑。设NA为阿伏加德罗常数的值,下列说法正确的是
Na+Cl2↑。设NA为阿伏加德罗常数的值,下列说法正确的是| A.1molCaCl2溶于1L水配成的CaCl2溶液中,c(Cl-)为2mol•L-1 |
| B.标准状况下,22.4LCl2溶于水所得溶液中HClO的数目为NA |
| C.上述反应生成4.6gNa转移的电子数目为0.4NA |
| D.常温常压下,3.7g37Cl2中含中子数目为2NA |
您最近一年使用:0次
23-24高一下·吉林·开学考试
名校
10 . 现有部分被氧化的Fe、Cu混合物(氧化物为 、CuO)样品共5.60g,经如下处理:
、CuO)样品共5.60g,经如下处理:
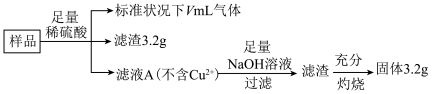
下列说法错误的是
 、CuO)样品共5.60g,经如下处理:
、CuO)样品共5.60g,经如下处理:
下列说法错误的是
| A.V=672 |
B.滤液A中的阳离子为 、 、 |
| C.样品中氧元素的物质的量为0.01mol |
| D.溶解样品的过程中消耗硫酸的总物质的量为0.05mol |
您最近一年使用:0次



