解题方法
1 . 以大洋锰结核(主要由 和铁氧化物组成,还含有
和铁氧化物组成,还含有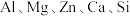 等元素)为原料制备
等元素)为原料制备 及
及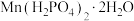 的工艺流程如下:
的工艺流程如下: 范围如下:
范围如下:
② 时,
时,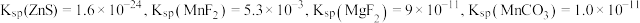 。
。
回答下列问题:
(1)锰元素在元素周期表中的位置为___________ 。
(2)“浸取”时,有副产物 生成。该副反应过程中氧化剂与还原剂的物质的量之比为
生成。该副反应过程中氧化剂与还原剂的物质的量之比为___________ 。温度对锰的浸出率、 生成率的影响如图所示,为了减少副产物的生成并降低能耗,最适宜的温度为
生成率的影响如图所示,为了减少副产物的生成并降低能耗,最适宜的温度为___________ 左右(填标号)。 B.
B. C.
C. D.
D.
(3)加氨水“调 ”时,应控制的
”时,应控制的 范围是
范围是___________ 。
(4)“净化”后,过滤出“滤渣3”,所得滤液中 的最低浓度为
的最低浓度为___________  。
。
(5)“沉锰”时,加入过量的 溶液与溶液中的
溶液与溶液中的 作用,反应的化学方程式为
作用,反应的化学方程式为___________ 。若改用加入 溶液,还会产生
溶液,还会产生 沉淀,可能的原因是:
沉淀,可能的原因是: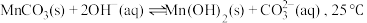 时,该反应的平衡常数的对数值
时,该反应的平衡常数的对数值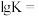
___________ (保留1位小数)。
(6)要将“溶解”后的溶液制得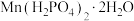 晶体,操作X为
晶体,操作X为___________ 、___________ 、过滤、洗涤、干燥。
 和铁氧化物组成,还含有
和铁氧化物组成,还含有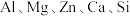 等元素)为原料制备
等元素)为原料制备 及
及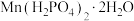 的工艺流程如下:
的工艺流程如下: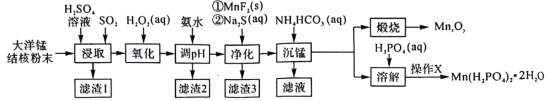
 范围如下:
范围如下:| 金属离子 |  |  |  |  |  |  |
开始沉淀的 | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 |
完全沉淀的 | 10.2 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 |
 时,
时,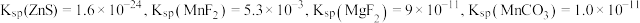 。
。回答下列问题:
(1)锰元素在元素周期表中的位置为
(2)“浸取”时,有副产物
 生成。该副反应过程中氧化剂与还原剂的物质的量之比为
生成。该副反应过程中氧化剂与还原剂的物质的量之比为 生成率的影响如图所示,为了减少副产物的生成并降低能耗,最适宜的温度为
生成率的影响如图所示,为了减少副产物的生成并降低能耗,最适宜的温度为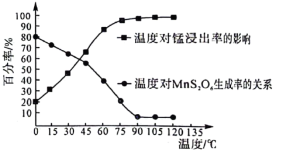
 B.
B. C.
C. D.
D.
(3)加氨水“调
 ”时,应控制的
”时,应控制的 范围是
范围是(4)“净化”后,过滤出“滤渣3”,所得滤液中
 的最低浓度为
的最低浓度为 。
。(5)“沉锰”时,加入过量的
 溶液与溶液中的
溶液与溶液中的 作用,反应的化学方程式为
作用,反应的化学方程式为 溶液,还会产生
溶液,还会产生 沉淀,可能的原因是:
沉淀,可能的原因是: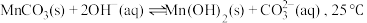 时,该反应的平衡常数的对数值
时,该反应的平衡常数的对数值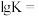
(6)要将“溶解”后的溶液制得
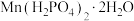 晶体,操作X为
晶体,操作X为
您最近半年使用:0次
2 . 二氯化二硫( )是一种常用的橡胶硫化剂,其结构如图所示。
)是一种常用的橡胶硫化剂,其结构如图所示。 极易水解:
极易水解: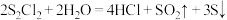 。下列说法错误的是
。下列说法错误的是
 )是一种常用的橡胶硫化剂,其结构如图所示。
)是一种常用的橡胶硫化剂,其结构如图所示。 极易水解:
极易水解: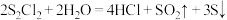 。下列说法错误的是
。下列说法错误的是
A. 中S为+1价 中S为+1价 |
B. 是由非极性键与极性键构成的极性分子 是由非极性键与极性键构成的极性分子 |
C.上述反应中 既作氧化剂又作还原剂 既作氧化剂又作还原剂 |
| D.上述反应中氧化产物与还原产物的质量比为3:1 |
您最近半年使用:0次
3 .  磁材料应用广泛,制备流程如图。下列说法错误的是
磁材料应用广泛,制备流程如图。下列说法错误的是
 磁材料应用广泛,制备流程如图。下列说法错误的是
磁材料应用广泛,制备流程如图。下列说法错误的是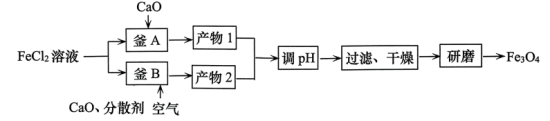
| A.“产物1”需要密封保存防止氧化 |
B.“釜B”中主要反应的化学方程式为 |
C.“产物1”与“产物2”中参与生成 反应的物质的物质的量之比为2:1 反应的物质的物质的量之比为2:1 |
| D.“分散剂”可破坏形成的胶体来促进氧化 |
您最近半年使用:0次
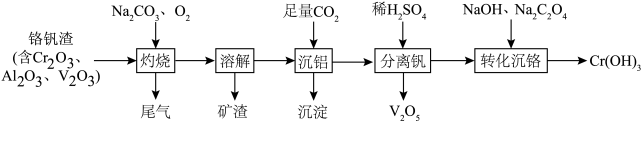
4 . 某科研团队从铬钒渣中分离钒并制备Cr(OH)3的流程如下:
②Cr的最高价含氧酸根离子在酸性介质中主要以 存在,在碱性介质中主要以
存在,在碱性介质中主要以 存在。
存在。
下列说法错误的是
②Cr的最高价含氧酸根离子在酸性介质中主要以
 存在,在碱性介质中主要以
存在,在碱性介质中主要以 存在。
存在。下列说法错误的是
| A.“灼烧”步骤的尾气中含CO2 |
B.“沉铝”步骤的离子方程式为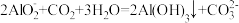 |
C.“分离钒”之后Cr元素的存在形式主要为 |
| D.“转化沉铬”步骤中氧化剂与还原剂的物质的量之比为1∶3 |
您最近半年使用:0次
7日内更新
|
230次组卷
|
2卷引用:福建省漳州市2024届高三下学期毕业班第三次质量检测三模化学试题
解题方法
5 . 工业上,常用浓氨水检验输送氯气管道是否漏气,发生反应: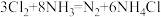 (白烟)。下列叙述错误的是
(白烟)。下列叙述错误的是
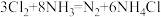 (白烟)。下列叙述错误的是
(白烟)。下列叙述错误的是A.NH3的电子式为 |
| B.1个N2分子含3个共用电子对 |
| C.NH4Cl只含共价键 |
| D.反应中每生成1molN2转移电子6mol |
您最近半年使用:0次
名校
6 . 下列关于氨气的应用及性质说法正确的是
A.氨燃料动力集装箱船中氨气燃烧的化学方程式: |
B.足量的氨气和氯气反应,氧化剂和还原剂的物质的量之比为 |
C.氨气的中心原子采取 杂化,且氮原子提供空轨道与 杂化,且氮原子提供空轨道与 形成配位键 形成配位键 |
D.氨气可用于制备高能分子磷酰三叠氮,结构简式为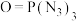 ,其分解产物 ,其分解产物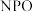 的电子式为 的电子式为 |
您最近半年使用:0次
名校
7 . “环境就是民生,青山就是美丽,蓝天也是幸福。”拥有天蓝、地绿、水净的美好家园,是每个中国人的梦想。回答下列问题:
(1)汽车尾气(含CO、N2、SO2和NO等)是城市空气污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转化器”,它能使一氧化碳跟一氧化氮反应生成可参与大气生态循环的无毒气体。写出在催化剂的作用下CO跟NO反应的化学方程式___________ 。
(2)化肥、炼油、稀土、钢铁等工业都会排放出高浓度的氨氮废水。氨氮废水是造成河流及湖泊富营养化的主要因素。某氮肥厂产生的氨氮废水中的氮元素多以 和NH3·H2O形式存在,为达到变废为宝回收利用的目的某团队设计处理流程如下:
和NH3·H2O形式存在,为达到变废为宝回收利用的目的某团队设计处理流程如下:___________ 。
②过程Ⅱ为硝化过程,在微生物的作用下实现 →
→ →
→ 的转化,在碱性条件下,
的转化,在碱性条件下, 被氧气氧化成
被氧气氧化成 的总反应的离子方程式为
的总反应的离子方程式为___________ 。
③过程Ⅲ为反硝化过程,向一定条件下的废水中加入甲醇(CH3OH)实现HNO3→ →N2的转化,将0.5mol
→N2的转化,将0.5mol 完全转化为N2,转移电子的物质的量为
完全转化为N2,转移电子的物质的量为___________ 。
(3)按如图所示装置探究浓、稀硝酸氧化性的相对强弱(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
①装置b、c、d中盛放的药品依次是___________ 、___________ 、___________ 。其中装置a中发生反应的化学方程式是___________ 。
②实验结束后,同学们发现装置a中溶液呈绿色,而不显蓝色。针对溶液呈绿色的原因,提出以下假设:
假设1:Cu2+的浓度较大所致;
假设2:溶解了生成的NO2。
探究如下:取装置a中绿色溶液,分为两等份。
取一份于如图所示装置中,___________ (填“操作”和“现象”),证实装置a中溶解了NO2。___________ (填化学试剂),溶液变为蓝色。证实假设1不成立,假设2成立。
(1)汽车尾气(含CO、N2、SO2和NO等)是城市空气污染源之一,治理的方法之一是在汽车的排气管上装一个“催化转化器”,它能使一氧化碳跟一氧化氮反应生成可参与大气生态循环的无毒气体。写出在催化剂的作用下CO跟NO反应的化学方程式
(2)化肥、炼油、稀土、钢铁等工业都会排放出高浓度的氨氮废水。氨氮废水是造成河流及湖泊富营养化的主要因素。某氮肥厂产生的氨氮废水中的氮元素多以
 和NH3·H2O形式存在,为达到变废为宝回收利用的目的某团队设计处理流程如下:
和NH3·H2O形式存在,为达到变废为宝回收利用的目的某团队设计处理流程如下: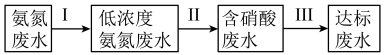
②过程Ⅱ为硝化过程,在微生物的作用下实现
 →
→ →
→ 的转化,在碱性条件下,
的转化,在碱性条件下, 被氧气氧化成
被氧气氧化成 的总反应的离子方程式为
的总反应的离子方程式为③过程Ⅲ为反硝化过程,向一定条件下的废水中加入甲醇(CH3OH)实现HNO3→
 →N2的转化,将0.5mol
→N2的转化,将0.5mol 完全转化为N2,转移电子的物质的量为
完全转化为N2,转移电子的物质的量为(3)按如图所示装置探究浓、稀硝酸氧化性的相对强弱(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
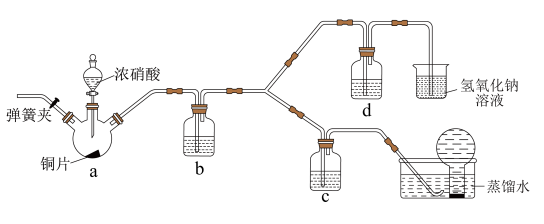
①装置b、c、d中盛放的药品依次是
②实验结束后,同学们发现装置a中溶液呈绿色,而不显蓝色。针对溶液呈绿色的原因,提出以下假设:
假设1:Cu2+的浓度较大所致;
假设2:溶解了生成的NO2。
探究如下:取装置a中绿色溶液,分为两等份。
取一份于如图所示装置中,
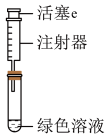
您最近半年使用:0次
8 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.将2mol NO和2mol  混合,充分反应后体系中原子总数为8 混合,充分反应后体系中原子总数为8 |
B.标准状况下,22.4L  中所含原子数为4 中所含原子数为4 |
C.1mol的铁与足量的硫粉发生反应,转移的电子数为3 |
D.100g质量分数为9.8%的 水溶液中所含氧原子数目为0.4 水溶液中所含氧原子数目为0.4 |
您最近半年使用:0次
9 . 已知反应 ,
, 为阿伏加德罗常数的值,若生成22.4L
为阿伏加德罗常数的值,若生成22.4L (标况),下列说法错误的是
(标况),下列说法错误的是
 ,
, 为阿伏加德罗常数的值,若生成22.4L
为阿伏加德罗常数的值,若生成22.4L (标况),下列说法错误的是
(标况),下列说法错误的是A.转移的电子数目为 |
B. 是由非极性共价键形成的非极性分子 是由非极性共价键形成的非极性分子 |
C.参与反应的 含有孤电子对数为 含有孤电子对数为 |
| D.生成的还原产物质量为56g |
您最近半年使用:0次
解题方法
10 . 根据元素的特征完成下列问题。
I.元素A、B、J、D、E、F、G是元素周期表前四周期的常见元素,且原子序数依次增大,其相关信息如表所示,请回答下列问题。
(1)在下列物质中属于离子化合物的是有___________ ,仅含共价键的有___________ 。
①AF ②DF ③ ④
④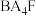
(2)E的单质与D的最高价氧化物对应水化物溶液反应的离子方程式为___________ 。
(3)B原子能与碳原子形成化学式为 的链状分子,其中所有原子都满足8电子稳定结构。
的链状分子,其中所有原子都满足8电子稳定结构。 的电子式为
的电子式为___________ 。
(4)在X中,G元素基态离子的价层电子的轨道排布式为___________ 。
Ⅱ.几种短周期元素的原子结构和性质如下所示:
(5)元素②的离子结构示意图为___________ 。
(6)元素⑦的简单氢化物与少量⑤的单质反应时,观察到有大量白烟产生,同时得到氮气。该反应中,氧化剂与还原剂的物质的量之比为___________ 。
(7)元素①和③的单质相互反应得到产物Y。用电子式表示Y 形成过程为___________ 。
I.元素A、B、J、D、E、F、G是元素周期表前四周期的常见元素,且原子序数依次增大,其相关信息如表所示,请回答下列问题。
| A | 原子核外电子只有一种运动状态 |
| B | 简单离子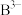 与D的离子具有相同电子排布 与D的离子具有相同电子排布 |
| J | 基态原子中s电子总数与p电子总数相等 |
| D | 元素的焰色试验呈黄色 |
| E | 基态原子价层电子排布式为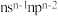 |
| F | 在基态原子的最外层上,p轨道有2个电子的自旋状态与其他电子相反 |
| G | 生活中使用最多的一种金属,其某种盐X溶液常用于刻蚀铜制印刷电路 |
①AF ②DF ③
 ④
④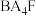
(2)E的单质与D的最高价氧化物对应水化物溶液反应的离子方程式为
(3)B原子能与碳原子形成化学式为
 的链状分子,其中所有原子都满足8电子稳定结构。
的链状分子,其中所有原子都满足8电子稳定结构。 的电子式为
的电子式为(4)在X中,G元素基态离子的价层电子的轨道排布式为
Ⅱ.几种短周期元素的原子结构和性质如下所示:
| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 最外层电子数 | 6 | 1 | 1 | ||||
| 原子半径/nm | 0.074 | 0.16 | 0.152 | 0.11 | 0.099 | 0.186 | 0.075 |
| 主要化合价 | +2 | -3,+5 | -1,+7 | -3,+5 |
(6)元素⑦的简单氢化物与少量⑤的单质反应时,观察到有大量白烟产生,同时得到氮气。该反应中,氧化剂与还原剂的物质的量之比为
(7)元素①和③的单质相互反应得到产物Y。用电子式表示Y 形成过程为
您最近半年使用:0次



