1 . NH4NO3受撞击时会发生爆炸: 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 溶液中含 溶液中含 数目为 数目为 |
B.1molN2中含 键数目为 键数目为 |
C.标准状况下,22.4LH2O中含电子数为 |
D.每生成0.2molNO2,该反应中转移电子数为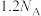 |
您最近半年使用:0次
名校
2 . 实验室可利用反应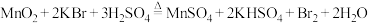 制备
制备 。设
。设 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是
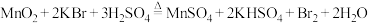 制备
制备 。设
。设 代表阿伏加德罗常数的值,下列说法正确的是
代表阿伏加德罗常数的值,下列说法正确的是A.0℃、101kPa下,11.2L  所含的分子数为0.5 所含的分子数为0.5 |
B.0.1 的 的  溶液中含有的离子数为0.3 溶液中含有的离子数为0.3 |
C.常温常压下,9.8g  和9.8g 和9.8g  中含有的氧原子数均为0.4 中含有的氧原子数均为0.4 |
D.该反应中生成0.2mol  时,转移的电子数为0.2 时,转移的电子数为0.2 |
您最近半年使用:0次
3 . 二氯化二硫( )是一种常用的橡胶硫化剂,其结构如图所示。
)是一种常用的橡胶硫化剂,其结构如图所示。 极易水解:
极易水解: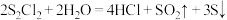 。下列说法错误的是
。下列说法错误的是
 )是一种常用的橡胶硫化剂,其结构如图所示。
)是一种常用的橡胶硫化剂,其结构如图所示。 极易水解:
极易水解: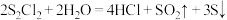 。下列说法错误的是
。下列说法错误的是
A. 中S为+1价 中S为+1价 |
B. 是由非极性键与极性键构成的极性分子 是由非极性键与极性键构成的极性分子 |
C.上述反应中 既作氧化剂又作还原剂 既作氧化剂又作还原剂 |
| D.上述反应中氧化产物与还原产物的质量比为3:1 |
您最近半年使用:0次
解题方法
4 . 酸性条件下Na2S和Na2SO3发生反应: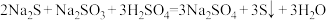 ,下列说法
,下列说法不正确 的是(设 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
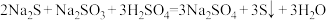 ,下列说法
,下列说法 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)A.生成24gS转移电子的数目为 | B.Na2S是还原剂,发生氧化反应 |
| C.Na2SO4是氧化产物 | D.碱性条件下S2-和 可以大量共存 可以大量共存 |
您最近半年使用:0次
5 .  磁材料应用广泛,制备流程如图。下列说法错误的是
磁材料应用广泛,制备流程如图。下列说法错误的是
 磁材料应用广泛,制备流程如图。下列说法错误的是
磁材料应用广泛,制备流程如图。下列说法错误的是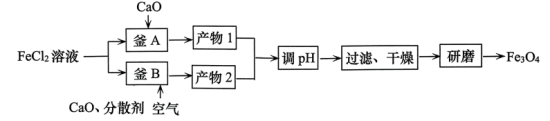
| A.“产物1”需要密封保存防止氧化 |
B.“釜B”中主要反应的化学方程式为 |
C.“产物1”与“产物2”中参与生成 反应的物质的物质的量之比为2:1 反应的物质的物质的量之比为2:1 |
| D.“分散剂”可破坏形成的胶体来促进氧化 |
您最近半年使用:0次
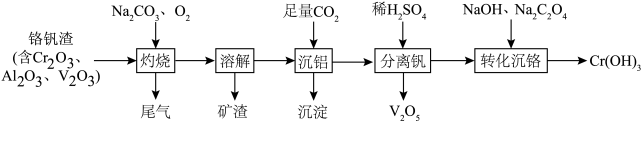
6 . 某科研团队从铬钒渣中分离钒并制备Cr(OH)3的流程如下:
②Cr的最高价含氧酸根离子在酸性介质中主要以 存在,在碱性介质中主要以
存在,在碱性介质中主要以 存在。
存在。
下列说法错误的是
②Cr的最高价含氧酸根离子在酸性介质中主要以
 存在,在碱性介质中主要以
存在,在碱性介质中主要以 存在。
存在。下列说法错误的是
| A.“灼烧”步骤的尾气中含CO2 |
B.“沉铝”步骤的离子方程式为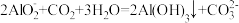 |
C.“分离钒”之后Cr元素的存在形式主要为 |
| D.“转化沉铬”步骤中氧化剂与还原剂的物质的量之比为1∶3 |
您最近半年使用:0次
7日内更新
|
230次组卷
|
2卷引用:福建省漳州市2024届高三下学期毕业班第三次质量检测三模化学试题
解题方法
7 . 工业上,常用浓氨水检验输送氯气管道是否漏气,发生反应: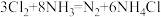 (白烟)。下列叙述错误的是
(白烟)。下列叙述错误的是
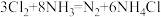 (白烟)。下列叙述错误的是
(白烟)。下列叙述错误的是A.NH3的电子式为 |
| B.1个N2分子含3个共用电子对 |
| C.NH4Cl只含共价键 |
| D.反应中每生成1molN2转移电子6mol |
您最近半年使用:0次
名校
解题方法
8 . 我国最新型055型万吨驱逐舰上使用了最新一代国产有源相控阵雷达,采用了最先进的氮化镓( )半导体技术。某工厂利用铝土矿(主要成分为
)半导体技术。某工厂利用铝土矿(主要成分为 、
、 、
、 )为原料制备
)为原料制备 的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应,
的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应, 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 )半导体技术。某工厂利用铝土矿(主要成分为
)半导体技术。某工厂利用铝土矿(主要成分为 、
、 、
、 )为原料制备
)为原料制备 的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应,
的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应, 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是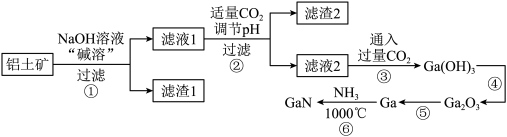
| A.可以通过粉碎铝土矿、搅拌等方法提高“碱溶”效率 |
B.由过程②、③可知, 的酸性比 的酸性比 强 强 |
C.已知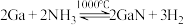 , , 与足量 与足量 反应,转移电子数为 反应,转移电子数为 |
D.滤渣1是 ,生成滤渣2的离子方程式可能为 ,生成滤渣2的离子方程式可能为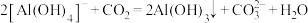 |
您最近半年使用:0次
名校
9 . 下列关于氨气的应用及性质说法正确的是
A.氨燃料动力集装箱船中氨气燃烧的化学方程式: |
B.足量的氨气和氯气反应,氧化剂和还原剂的物质的量之比为 |
C.氨气的中心原子采取 杂化,且氮原子提供空轨道与 杂化,且氮原子提供空轨道与 形成配位键 形成配位键 |
D.氨气可用于制备高能分子磷酰三叠氮,结构简式为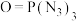 ,其分解产物 ,其分解产物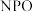 的电子式为 的电子式为 |
您最近半年使用:0次
10 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.将2mol NO和2mol  混合,充分反应后体系中原子总数为8 混合,充分反应后体系中原子总数为8 |
B.标准状况下,22.4L  中所含原子数为4 中所含原子数为4 |
C.1mol的铁与足量的硫粉发生反应,转移的电子数为3 |
D.100g质量分数为9.8%的 水溶液中所含氧原子数目为0.4 水溶液中所含氧原子数目为0.4 |
您最近半年使用:0次



