名校
1 . 设阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是A.48g正丁烷和10g异丁烷的混合物中共价键数目为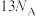 |
B.标准状况下,11.2LCH2Cl2含有原子个数为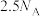 |
C.标况下22.4L丙烯与氯水完全反应后,再与氯气发生取代反应,最多共消耗Cl2 |
D.足量铜与50mL18mol·L-1硫酸溶液共热,充分反应后,被还原的硫酸为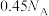 |
您最近一年使用:0次
2 . 《天工开物》记载:“凡火药以硝石、硫磺为主,草木灰为辅……而后火药成声”,涉及的主要反应为 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,22.4 L  中含有的π键数为 中含有的π键数为 |
B.1 mol  分子中的电子总数为 分子中的电子总数为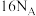 |
C.常温下,1 mol⋅L  溶液中 溶液中 数为 数为 |
D.12 g C完全反应转移电子数为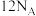 |
您最近一年使用:0次
名校
3 . 氨氮是水体的污染物之一,工业上可用次氯酸盐作处理剂,有关反应可表示为:
①
②
实验室将1L0.006mol/L的氨水分别和不同量的NaClO混合,测得溶液中氨去除率、总氮(氨氮和硝氮的总和)残余率与NaClO投入量n(NaClO)的关系如图所示。
①

②

实验室将1L0.006mol/L的氨水分别和不同量的NaClO混合,测得溶液中氨去除率、总氮(氨氮和硝氮的总和)残余率与NaClO投入量n(NaClO)的关系如图所示。

| A.n1的数值为9.75×10-3 |
B.n=n1时,c(Cl-)>4c( ) ) |
| C.n>n1时,n越大,生成N2的物质的量越少 |
| D.n<n1时,c(Na+)+c(H+)=c(Cl-)+c(OH-) |
您最近一年使用:0次
名校
解题方法
4 . 在Pt-BaO催化下,NO的“储存-还原”过程如图1所示。其中“还原”过程依次发生反应I和反应Ⅱ,各气体的物质的量变化如图2所示。

A. 、 、 与BaO的反应中, 与BaO的反应中, 是还原剂, 是还原剂, 是氧化剂 是氧化剂 |
B.反应I为 |
C.反应Ⅱ中,最终生成 的物质的量为 的物质的量为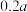 mol mol |
D.反应I和Ⅱ中消耗的 的物质的量之比是3∶5 的物质的量之比是3∶5 |
您最近一年使用:0次
5 . 已知 晶体在加热条件下发生如下反应:
晶体在加热条件下发生如下反应: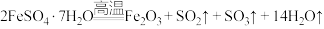 (已知:
(已知: 和
和 的熔点分别为-72.7℃、16.8℃,沸点分别为-10℃、44.8℃);利用下图装置可检验该反应的气体产物。下列说法错误的是
的熔点分别为-72.7℃、16.8℃,沸点分别为-10℃、44.8℃);利用下图装置可检验该反应的气体产物。下列说法错误的是
 晶体在加热条件下发生如下反应:
晶体在加热条件下发生如下反应: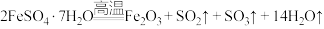 (已知:
(已知: 和
和 的熔点分别为-72.7℃、16.8℃,沸点分别为-10℃、44.8℃);利用下图装置可检验该反应的气体产物。下列说法错误的是
的熔点分别为-72.7℃、16.8℃,沸点分别为-10℃、44.8℃);利用下图装置可检验该反应的气体产物。下列说法错误的是
| A.仪器的连接顺序为a、f(或g)、g(或f)、h、i、d、e、b |
B.装置C中的X溶液为 溶液 溶液 |
| C.装置B的作用为处理尾气 |
D.反应中每生成 ,转移2mol电子 ,转移2mol电子 |
您最近一年使用:0次
名校
6 . 设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 和 和 混合固体中含 混合固体中含 的数目为 的数目为 |
B.向 溶液中通入适量 溶液中通入适量 ,当有 ,当有 被氧化时,共转移电子的数目为 被氧化时,共转移电子的数目为 |
C.用电解的方法将酸性废水中的 转化为 转化为 而除去,阴极为石墨,阳极为铁,理论上电路中每通过 而除去,阴极为石墨,阳极为铁,理论上电路中每通过 电子,就有 电子,就有 个 个 被还原 被还原 |
D.  含 含 键的数目为 键的数目为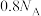 |
您最近一年使用:0次
7 . 合成氨反应为 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是A.该反应 |
B. |
C.反应中每消耗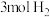 转移 转移 电子 电子 |
| D.实际生产中以低温、高压、高活性催化剂的条件来提高氨气产率 |
您最近一年使用:0次
名校
8 . 氮在自然界中的循环涉及地球上生物圈的方方面面。

| A.细菌对氮元素的循环有重要作用 |
| B.硝化过程和反硝化过程均为氧化还原反应 |
| C.氨氧化过程中氧化产物和还原产物的质量比为1∶1 |
D.Fe3+将NH 转化为N2的离子方程式为Fe3++2NH 转化为N2的离子方程式为Fe3++2NH =Fe2++N2↑+8H+ =Fe2++N2↑+8H+ |
您最近一年使用:0次
9 . 某温度下将氯气通入过量KOH溶液中,反应后得到KCl、KClO和KClO3的混合溶液,若所得溶液中ClO-和ClO 的物质的量之比为2:1,则该反应中被氧化和被还原氯元素的质量比为
的物质的量之比为2:1,则该反应中被氧化和被还原氯元素的质量比为
 的物质的量之比为2:1,则该反应中被氧化和被还原氯元素的质量比为
的物质的量之比为2:1,则该反应中被氧化和被还原氯元素的质量比为| A.3:7 | B.7:3 | C.1:1 | D.3:11 |
您最近一年使用:0次
解题方法
10 . 硫化碱法是工业上制备 的方法之一,反应原理为
的方法之一,反应原理为 下列有关说法不正确的是
下列有关说法不正确的是
 的方法之一,反应原理为
的方法之一,反应原理为 下列有关说法不正确的是
下列有关说法不正确的是A. 既是氧化产物又是还原产物 既是氧化产物又是还原产物 |
| B.适当升高温度可以加快此反应的反应速率 |
C. 是还原剂, 是还原剂, 是氧化剂 是氧化剂 |
D.生成 转移电子的数目为8 转移电子的数目为8 |
您最近一年使用:0次



