某温度下将氯气通入过量KOH溶液中,反应后得到KCl、KClO和KClO3的混合溶液,若所得溶液中ClO-和ClO 的物质的量之比为2:1,则该反应中被氧化和被还原氯元素的质量比为
的物质的量之比为2:1,则该反应中被氧化和被还原氯元素的质量比为
 的物质的量之比为2:1,则该反应中被氧化和被还原氯元素的质量比为
的物质的量之比为2:1,则该反应中被氧化和被还原氯元素的质量比为| A.3:7 | B.7:3 | C.1:1 | D.3:11 |
更新时间:2024-05-26 22:02:36
|
【知识点】 基于氧化还原反应守恒规律的计算解读
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】高铁酸钾作净水剂,既能消毒杀菌,也能吸附水中悬浮物。K2FeO4制备原理为:ClO-+Fe3++OH- —— + Cl-+ H2O (方程式未配平),下列说法正确的是
+ Cl-+ H2O (方程式未配平),下列说法正确的是
 + Cl-+ H2O (方程式未配平),下列说法正确的是
+ Cl-+ H2O (方程式未配平),下列说法正确的是| A.ClO-是氧化剂,Cl-是氧化产物 |
| B.Fe3+发生氧化反应 |
| C.当生成2 mol K2FeO4时,转移电子数为3 mol |
| D.氧化产物与还原产物的物质的量之比为3:2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关化学反应的描述中不正确的是
| A.一定条件下的可逆反应,反应物的转化率不可能达到100% |
| B.氧化还原反应中,氧化剂得到电子数目一定等于还原剂失去电子的数目 |
| C.△H<0,△S>0的化学反应一定能自发进行 |
| D.对于△H>0的反应,反应物的能量大于生成物的能量 |
您最近一年使用:0次


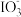 +10Cl-+6H2O
+10Cl-+6H2O

