名校
解题方法
1 . 铁是最常见的金属之一、纳米铁粉可用于处理酸性含氮废水(主要含 );铁易被腐蚀,经碱性发蓝处理可增强其抗腐蚀性,方法为:用NaOH与
);铁易被腐蚀,经碱性发蓝处理可增强其抗腐蚀性,方法为:用NaOH与 进行浸泡,在表面形成
进行浸泡,在表面形成 的同时有
的同时有 生成;铁与砷反应得到的FeAs可被Na还原得到NaFeAs,NaFeAs难溶于水,是一种超导材料。镍(Ni)与Fe单质化学性质相似,金属活动性比铁略低。酸性条件下,
生成;铁与砷反应得到的FeAs可被Na还原得到NaFeAs,NaFeAs难溶于水,是一种超导材料。镍(Ni)与Fe单质化学性质相似,金属活动性比铁略低。酸性条件下, 的氧化性强于
的氧化性强于 ,
, 的盐与碱反应可以转化为不溶性的
的盐与碱反应可以转化为不溶性的 。在隔绝空气条件下,将NaFeAs加入水中,NaFeAs转化成
。在隔绝空气条件下,将NaFeAs加入水中,NaFeAs转化成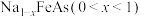 的同时释放出
的同时释放出 。下列说法正确的是
。下列说法正确的是
 );铁易被腐蚀,经碱性发蓝处理可增强其抗腐蚀性,方法为:用NaOH与
);铁易被腐蚀,经碱性发蓝处理可增强其抗腐蚀性,方法为:用NaOH与 进行浸泡,在表面形成
进行浸泡,在表面形成 的同时有
的同时有 生成;铁与砷反应得到的FeAs可被Na还原得到NaFeAs,NaFeAs难溶于水,是一种超导材料。镍(Ni)与Fe单质化学性质相似,金属活动性比铁略低。酸性条件下,
生成;铁与砷反应得到的FeAs可被Na还原得到NaFeAs,NaFeAs难溶于水,是一种超导材料。镍(Ni)与Fe单质化学性质相似,金属活动性比铁略低。酸性条件下, 的氧化性强于
的氧化性强于 ,
, 的盐与碱反应可以转化为不溶性的
的盐与碱反应可以转化为不溶性的 。在隔绝空气条件下,将NaFeAs加入水中,NaFeAs转化成
。在隔绝空气条件下,将NaFeAs加入水中,NaFeAs转化成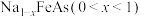 的同时释放出
的同时释放出 。下列说法正确的是
。下列说法正确的是| A.NaFeAs与水反应所得溶液pH下降 | B.消耗1 mol NaFeAs,转移2 mol电子 |
| C.NaFeAs与水反应时体现还原性 | D.制备NaFeAs无须隔绝空气和水 |
您最近一年使用:0次
2024-04-13更新
|
68次组卷
|
2卷引用:江苏省盐城市大丰高级中学2023-2024学年高一下学期(创新班)第一次阶段性考试化学试卷
名校
解题方法
2 . 铬的化合物有毒,由于Cr(Ⅵ)的强氧化性,其毒性是Cr(Ⅲ)毒性的100倍,因此必须对排放的含铬废水进行处理。实验小组收集的某500mL废水中含铬元素的质量为28.6g,还含 杂质,查阅资料设计还原法处理含Cr(Ⅵ)的废水实现铬的回收流程如图所示。
杂质,查阅资料设计还原法处理含Cr(Ⅵ)的废水实现铬的回收流程如图所示。

已知:①在酸性环境中, 的氧化性强于
的氧化性强于 。
。
② (焦亚硫酸钠)水溶液呈酸性,与强酸接触则放出二氧化硫并生成相应的盐类。
(焦亚硫酸钠)水溶液呈酸性,与强酸接触则放出二氧化硫并生成相应的盐类。
下列说法错误的是
 杂质,查阅资料设计还原法处理含Cr(Ⅵ)的废水实现铬的回收流程如图所示。
杂质,查阅资料设计还原法处理含Cr(Ⅵ)的废水实现铬的回收流程如图所示。
已知:①在酸性环境中,
 的氧化性强于
的氧化性强于 。
。②
 (焦亚硫酸钠)水溶液呈酸性,与强酸接触则放出二氧化硫并生成相应的盐类。
(焦亚硫酸钠)水溶液呈酸性,与强酸接触则放出二氧化硫并生成相应的盐类。下列说法错误的是
A.若“酸化”时 有 有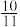 转化为 转化为 ,酸化后所得溶液中 ,酸化后所得溶液中 |
| B.“还原”工序中若加硫酸溶液调pH过低,还原处理含铬(Ⅵ)效果不好 |
C.“沉铬”时会产生 气体 气体 |
D.灼烧 得到产品 得到产品 ,再用铝热法进行冶炼可得到铬单质 ,再用铝热法进行冶炼可得到铬单质 |
您最近一年使用:0次
3 . 有资料表明,Na2O2与水反应的原理为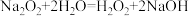 、
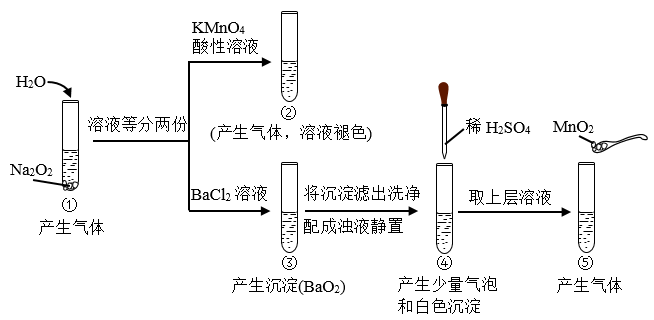
、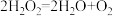 。如图实验验证该原理(已知:
。如图实验验证该原理(已知: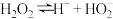 、
、 )。下列分析不正确的是
)。下列分析不正确的是
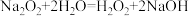 、
、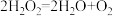 。如图实验验证该原理(已知:
。如图实验验证该原理(已知: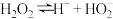 、
、 )。下列分析不正确的是
)。下列分析不正确的是
| A.①④中均发生了复分解反应和氧化还原反应 |
| B.①⑤中产生等物质的量气体转移电子数相等 |
| C.通过②⑤可比较氧化性KMnO4>H2O2、MnO2>H2O2 |
| D.③反应不能比较酸性:HCl>H2O2 |
您最近一年使用:0次
4 . 已知HNO2在低温下较稳定,酸性比醋酸略强,既有还原性又有氧化性,其氧化产物、还原产物与溶液pH的关系如下表。下列有关说法错误的是
| pH范围 | >7 | <7 |
| 产物 |  | NO、N2O、N2中的一种 |
A.碱性条件下,NaNO2与NaClO反应的离子方程式为 + ClO- = + ClO- = +Cl- +Cl- |
| B.向冷的NaNO2溶液中加入滴有淀粉的氢碘酸,若溶液变蓝色,则证明氧化性:HNO2>I2 |
| C.向冷的NaNO2溶液中通入SO2最终可得到HNO2 |
| D.低温时不用其他试剂即可区分HNO2溶液与Na2CO3溶液 |
您最近一年使用:0次
2022-01-22更新
|
132次组卷
|
2卷引用: 山西省太原市2021-2022学年高三上学期期末考试化学试题
名校
5 . 几种离子在水溶液(溶液酸碱性可调节)中有如下转化关系。下列说法正确的是
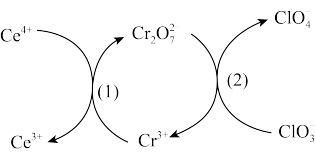

A.氧化性: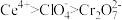 |
B.反应(1)生成 转移3mol电子 转移3mol电子 |
C.将反应(2)设计成原电池, 一定向负极迁移 一定向负极迁移 |
D.由图推知可以发生反应: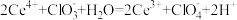 |
您最近一年使用:0次
6 . 已知酸性 溶液可与
溶液可与 反应生成
反应生成 和
和 。现将稀硫酸酸化的
。现将稀硫酸酸化的 溶液与
溶液与 溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中
溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中 的物质的量随加入的KI的物质的量的变化关系如图所示(已知
的物质的量随加入的KI的物质的量的变化关系如图所示(已知 生成
生成 ),下列说法中正确的是
),下列说法中正确的是
 溶液可与
溶液可与 反应生成
反应生成 和
和 。现将稀硫酸酸化的
。现将稀硫酸酸化的 溶液与
溶液与 溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中
溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中 的物质的量随加入的KI的物质的量的变化关系如图所示(已知
的物质的量随加入的KI的物质的量的变化关系如图所示(已知 生成
生成 ),下列说法中正确的是
),下列说法中正确的是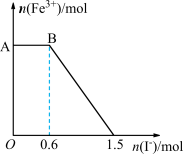
A.由图可知,氧化性: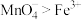 ,还原性: ,还原性: |
B.BC段发生的反应为 |
C. 与 与 反应的方程式中二者系数之比为1∶6 反应的方程式中二者系数之比为1∶6 |
D.开始加入的 为0.3mol 为0.3mol |
您最近一年使用:0次
2024-03-17更新
|
55次组卷
|
2卷引用:黑龙江省哈尔滨师范大学附属中学2023-2024学年高一下学期开学摸底考试化学试卷
名校
7 . 高铜酸钾(KCuO2)是一种难溶于水的黑色粉末状固体(其中氧元素的化合价为-2价),与高铁酸钾(K2FeO4)性质相似,可以由四羟基合铜酸钾和次溴酸在冰水浴中合成:①K2[Cu(OH)4]+HBrO→KCuO2+KBr+KBrO+H2O(未配平)。高铜酸钾在酸性条件下不稳定:②KCuO2+H2SO4→O2↑+CuSO4+H2O+K2SO4(未配平)。下列说法错误的是
| A.①中还原剂和氧化剂的数量之比为2:1 |
| B.②若有32gO2生成,则生成72gH2O |
| C.②中KCuO2既表现氧化性,又表现还原性 |
| D.由①、②可知氧化性强弱顺序为HBrO>KCuO2>O2 |
您最近一年使用:0次
名校
8 . KClO3与浓盐酸的反应是实验室制备氯气的方法之一: ,下列说法错误的是
,下列说法错误的是
 ,下列说法错误的是
,下列说法错误的是| A.氧化性:KClO3>Cl2 |
| B.被氧化的氯原子与被还原的氯原子的物质的量之比为5:1 |
C.用双线桥法表示电子得失情况: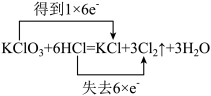 |
| D.HCl在反应中表现出还原性和酸性 |
您最近一年使用:0次
名校
解题方法
9 . 已知 Co2O3、Cl2、FeCl3和 I2的氧化性依次减弱。在酸性溶液中,Co2O3发生氧化还原反应时其还原产物为
 下列说法正确的是
下列说法正确的是

 下列说法正确的是
下列说法正确的是| A.酸性溶液中Co2O3与KI发生反应时,氧化产物与还原产物的物质的量之比为2∶1 |
B.向 FeCl3溶液中滴加 KI溶液,可发生反应: |
| C.Co2O3与浓盐酸反应时,HCl只 体现还原性 |
| D.向酸性FeCl2溶液中加入足量Co₂O₃,仅Cl⁻被氧化 |
您最近一年使用:0次
2023-11-17更新
|
267次组卷
|
2卷引用:河南省八市2023~2024学年高一上学期期中学业质量检测化学试题
解题方法
10 . 高铜酸钾(KCuO2)是一种难溶于水的黑色粉末状固体,与高铁酸钾(K2FeO4)性质相似,可以由四羟基合铜酸钾和次溴酸在冰水浴中合成:①K2[Cu(OH)4]+HBrO→KCuO2+KBr+KBrO+H2O(未配平)。高铜酸钾在酸性条件下不稳定:②KCuO2+H2SO4→O2↑+CuSO4+H2O+K2SO4(未配平)。下列说法错误的是
| A.①中还原剂和氧化剂的物质的量之比为2:1 |
| B.②若有标准状况下5.6 L O2生成,则转移电子0.5 mol |
| C.②中KCuO2既表现氧化性,又表现还原性 |
| D.由①、②可知氧化性强弱顺序为HBrO>KCuO2>O2 |
您最近一年使用:0次



