名校
1 . 已知:5PbO2+2Mn2++4H+= 5Pb2++ 2MnO4-+2H2O,下列说法正确的是
| A.PbO2为还原剂,具有还原性 | B.氧化剂与还原剂的物质的量之比为2∶5 |
| C.生成1mol的Pb2+,转移的电子为2mol | D.酸性环境下PbO2的氧化性强于MnO4- |
您最近一年使用:0次
2018-01-11更新
|
146次组卷
|
2卷引用:山东省枣庄市第八中学东校区2017-2018学年高一上学期第二次月考(12月)化学试题
名校
解题方法
2 . 根据反应 KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,下列叙述正确的是
| A.反应中被还原与被氧化的 Cl个数比为1∶5 | B.该反应中氧化剂与还原剂个数比为1∶6 |
| C.氧化性 Cl2>KClO3,还原性 HCl>Cl2 | D.每生成3个 Cl2,反应中共转移 5e- |
您最近一年使用:0次
3 . 高倩同学在做实验时引发了镁失火,她立即拿起二氧化碳灭火器欲把火扑灭,却被实验老师及时制止。原因是 可以支持镁燃烧发生以下反应:
可以支持镁燃烧发生以下反应: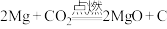 。下列关于该反应的判断正确的是
。下列关于该反应的判断正确的是
 可以支持镁燃烧发生以下反应:
可以支持镁燃烧发生以下反应: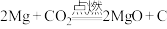 。下列关于该反应的判断正确的是
。下列关于该反应的判断正确的是A. 元素化合价由0价升高到+2价, 元素化合价由0价升高到+2价, 是还原产物 是还原产物 |
B.由此反应可以判断氧化性: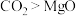 ,还原性: ,还原性: |
C. 作氧化剂,表现氧化性,发生氧化反应 作氧化剂,表现氧化性,发生氧化反应 |
D. 原子失去的电子数目等于氧原子得到的电子数目 原子失去的电子数目等于氧原子得到的电子数目 |
您最近一年使用:0次
4 . 已知KBrO3可发生反应:2KBrO3 + I2 = 2KIO3 + Br2,下列有关溴酸钾的说法不正确的是
| A.氧化剂与还原剂的物质的量之比为1:2 |
| B.该反应说明I2的还原性强于Br2 |
| C.当有1molKBrO3参与反应时转移5 mol电子 |
| D.该反应中物质氧化性强弱顺序为:KBrO3 < KIO3 |
您最近一年使用:0次
5 . 不是所有的火灾都适合使用 灭火器,比如金属镁失火,应该用沙土灭火而不是
灭火器,比如金属镁失火,应该用沙土灭火而不是 灭火器。原因是镁可以在
灭火器。原因是镁可以在 中燃烧,发生反应
中燃烧,发生反应  。判断正确的是
。判断正确的是
 灭火器,比如金属镁失火,应该用沙土灭火而不是
灭火器,比如金属镁失火,应该用沙土灭火而不是 灭火器。原因是镁可以在
灭火器。原因是镁可以在 中燃烧,发生反应
中燃烧,发生反应  。判断正确的是
。判断正确的是A. 是氧化剂,表现出氧化性,发生氧化反应 是氧化剂,表现出氧化性,发生氧化反应 |
B.由此反应可以判断该反应条件下,氧化性  > > ,还原性 ,还原性  > > |
C. 原子失去电子的总数目与 原子失去电子的总数目与 原子得到电子的总数目之比为 1:2 原子得到电子的总数目之比为 1:2 |
D.每消耗1mol 转移电子的数目为4NA 转移电子的数目为4NA |
您最近一年使用:0次
2023-11-17更新
|
124次组卷
|
4卷引用:海南省三亚市第一中学2023-2024学年高一上学期期中考试化学(B)试题
6 . 改良Claus法利用天然气脱硫产生的 回收单质硫,首先将原料气通入反应炉并发生高温反应Ⅰ:2
回收单质硫,首先将原料气通入反应炉并发生高温反应Ⅰ:2 ;反应后的混合气体通入串联的多个温度逐渐降低的转化器内进行反应Ⅱ:
;反应后的混合气体通入串联的多个温度逐渐降低的转化器内进行反应Ⅱ: 。下列说法正确的是
。下列说法正确的是
 回收单质硫,首先将原料气通入反应炉并发生高温反应Ⅰ:2
回收单质硫,首先将原料气通入反应炉并发生高温反应Ⅰ:2 ;反应后的混合气体通入串联的多个温度逐渐降低的转化器内进行反应Ⅱ:
;反应后的混合气体通入串联的多个温度逐渐降低的转化器内进行反应Ⅱ: 。下列说法正确的是
。下列说法正确的是| A.反应Ⅱ中氧化产物与还原产物的物质的量之比为1∶2 |
B.反应Ⅰ、Ⅱ中 既体现还原性又体现氧化性 既体现还原性又体现氧化性 |
C.反应Ⅰ、Ⅱ消耗等量 时,转移电子数之比为3∶1 时,转移电子数之比为3∶1 |
D.反应Ⅰ中消耗 的量占通入 的量占通入 总量的 总量的 时,硫的回收率最高 时,硫的回收率最高 |
您最近一年使用:0次
名校
解题方法
7 .  与浓盐酸的反应是实验室制备氯气的方法之一:
与浓盐酸的反应是实验室制备氯气的方法之一: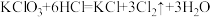 ,下列说法错误的是
,下列说法错误的是
 与浓盐酸的反应是实验室制备氯气的方法之一:
与浓盐酸的反应是实验室制备氯气的方法之一: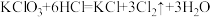 ,下列说法错误的是
,下列说法错误的是A.氧化性: |
B.被氧化的氯原子与被还原的氯原子的物质的量之比为 |
C.用双线桥法表示电子得失情况: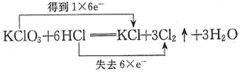 |
D. 在反应中只表现出还原性 在反应中只表现出还原性 |
您最近一年使用:0次
名校
8 . 由一种阳离子与两种酸根离子组成的盐称为混盐, 是一种常见的混盐,下列说法不正确的是
是一种常见的混盐,下列说法不正确的是
 是一种常见的混盐,下列说法不正确的是
是一种常见的混盐,下列说法不正确的是A. 中氯元素为-1价 中氯元素为-1价 |
B. 水溶液呈碱性,具有较强的氧化性 水溶液呈碱性,具有较强的氧化性 |
C.由氯气为原料,每生成1 mol  ,转移的电子数为 ,转移的电子数为 |
D. 溶液中加入足量浓硫酸,可有黄绿色气体产生 溶液中加入足量浓硫酸,可有黄绿色气体产生 |
您最近一年使用:0次
9 . 部分含氯物质的分类与相应氯元素的化合价关系如图所示。下列说法正确的是


| A.化学反应中,a能表现氧化性,也能表现还原性 |
| B.b和c均能使红色干燥的布条褪色 |
| C.a与e在一定条件下能制备b |
| D.c的氧化能力(单位质量转移的电子数,均转化为最低价)约为b的4.7倍 |
您最近一年使用:0次
解题方法
10 . 某反应的反应物与生成物有:K2Cr2O7、KCl、CrCl3、Cl2、HCl、H2O,已知氧化性:K2Cr2O7>Cl2,则下列说法错误的是
| A.氧化剂和还原剂的物质的量之比为1:14 |
| B.Cl2是该反应的还原产物 |
| C.当转移0.2mol电子时,被氧化的还原剂的物质的量为0.2mol |
| D.由此反应可知还原性:HCl>CrCl3 |
您最近一年使用:0次



