解题方法
1 . 生活离不开化学,家庭厨卫用品中有许多常见的化学物质,括号内为厨卫用品的主要成分:①漂白粉;②NaClO;③Cl2;④Na2CO3;⑤小苏打(NaHCO3);⑥生铁;⑦甲烷。回答下列问题:
(1)漂白液的有效成分NaClO在水溶液的电离方程式:___________ 。
(2)厨卫用品的主要成分(括号内的物质):是电解质的有___________ (填序号,下同),是非电解质的有___________ 。
(3)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常用的消毒药品:
84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。0.5mol过氧乙酸(CH3COOOH)的质量为___________ g。
(4)实验室制Cl2的化学方程式___________ ,收集到33.6L(折算到标准状态)氯气时该反应总共转移的电子数___________ 。
(1)漂白液的有效成分NaClO在水溶液的电离方程式:
(2)厨卫用品的主要成分(括号内的物质):是电解质的有
(3)2020年在抗击“新冠病毒”的战役中各种消毒试剂成为耀眼的明星,下面是几种常用的消毒药品:
84消毒液(NaClO)、双氧水(H2O2)、臭氧(O3)、过氧乙酸(CH3COOOH)、氯气(Cl2)等。0.5mol过氧乙酸(CH3COOOH)的质量为
(4)实验室制Cl2的化学方程式
您最近半年使用:0次
2 . 根据所学知识,回答下列问题:
(1)常温常压下,HCl气体溶于水形成的盐酸溶液,其溶质质量分数为
 ,密度为
,密度为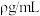 ,该溶液浓度为
,该溶液浓度为 。
。(2)“可燃冰”是由水和甲烷在一定条件下形成的类冰结晶化合物.
 “可燃冰”(
“可燃冰”( )的物质的量与
)的物质的量与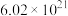 个水分子的物质的量相等,则该“可燃冰”的摩尔质量为
个水分子的物质的量相等,则该“可燃冰”的摩尔质量为(3)过氧化钠可用作呼吸面罩供氧剂,其原理可用方程式
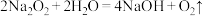 ,
,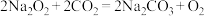 表示。若生成标况下
表示。若生成标况下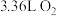 ,转移电子的数目为
,转移电子的数目为(4)现有
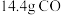 和
和 的混合气体,在标准状况下所占的体积约为
的混合气体,在标准状况下所占的体积约为 。将混合气体依次通过如图装置,最后收集在气球中,气球中收集到的气体在标况下的体积为
。将混合气体依次通过如图装置,最后收集在气球中,气球中收集到的气体在标况下的体积为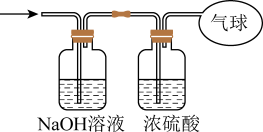
您最近半年使用:0次
名校
解题方法
3 . 某离子反应涉及 六种微粒,其中
六种微粒,其中 随着反应的进行逐渐减小,回答以下问题:
随着反应的进行逐渐减小,回答以下问题:
(1)该反应的氧化产物为_________ 。
(2)消耗 氧化剂,转移电子的物质的量为
氧化剂,转移电子的物质的量为_________  。
。
(3)写出反应的离子方程式_________ 。
 六种微粒,其中
六种微粒,其中 随着反应的进行逐渐减小,回答以下问题:
随着反应的进行逐渐减小,回答以下问题:(1)该反应的氧化产物为
(2)消耗
 氧化剂,转移电子的物质的量为
氧化剂,转移电子的物质的量为 。
。(3)写出反应的离子方程式
您最近半年使用:0次
解题方法
4 . 高铁酸盐( )被科学家们公认为绿色消毒剂,在强碱性溶液中比较稳定;聚合硫酸铁则是一种高效絮凝剂。
)被科学家们公认为绿色消毒剂,在强碱性溶液中比较稳定;聚合硫酸铁则是一种高效絮凝剂。
(1)KClO饱和溶液与 饱和溶液反应可制备K2FeO4,反应的离子方程为
饱和溶液反应可制备K2FeO4,反应的离子方程为___________ 。
(2)聚合硫酸铁[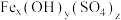 ]的组成可通过下列实验测定:
]的组成可通过下列实验测定:
①称取一定质量的聚合硫酸铁配成100.00 mL溶液A;
②准确量取20.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65 g;
③准确量取20.00 mL溶液A,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并配成250.00 mL溶液B;
④准确量取25.00 mL溶液B,用 的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液8.00 mL。
的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液8.00 mL。
通过计算确定该聚合硫酸铁的化学式_______ (写出计算过程)。
 )被科学家们公认为绿色消毒剂,在强碱性溶液中比较稳定;聚合硫酸铁则是一种高效絮凝剂。
)被科学家们公认为绿色消毒剂,在强碱性溶液中比较稳定;聚合硫酸铁则是一种高效絮凝剂。(1)KClO饱和溶液与
 饱和溶液反应可制备K2FeO4,反应的离子方程为
饱和溶液反应可制备K2FeO4,反应的离子方程为(2)聚合硫酸铁[
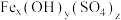 ]的组成可通过下列实验测定:
]的组成可通过下列实验测定:①称取一定质量的聚合硫酸铁配成100.00 mL溶液A;
②准确量取20.00 mL溶液A,加入盐酸酸化的BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重,得到白色固体11.65 g;
③准确量取20.00 mL溶液A,加入足量铜粉,充分反应后过滤、洗涤,将滤液和洗液合并配成250.00 mL溶液B;
④准确量取25.00 mL溶液B,用
 的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液8.00 mL。
的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液8.00 mL。通过计算确定该聚合硫酸铁的化学式
您最近半年使用:0次
5 . 氧化还原反应对我们的生产和生活同时具有正负两方面的影响,如果我们能够掌握化学变化的规律,就有可能做到趋利避害,使之更好地为社会发展服务。下面我们逐一分析:
(1)黑火药是我国古代的四大发明之一,黑火药着火时,发生如下氧化还原反应: 。在此反应中,还原剂为
。在此反应中,还原剂为_______ (填化学式),还原产物是_______ (填化学式),当该反应转移2.4mol电子时,产生气体的体积为_______ L(标况下)。
(2)湿法制备高铁酸钾 是在碱性环境中进行,反应体系中有六种反应微粒:
是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:_______ 。
(3)汽车剧烈碰撞时,安全气囊中发生反应: 。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为
。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为_______ 。
(4)在第一次世界大战期间,德军在比利时的伊普雷战役中使用了氯气制造的毒气弹。现代工业常用氯气制备漂白粉、消毒液等物质。写出制备漂白粉的化学反应方程式_______ 。
(1)黑火药是我国古代的四大发明之一,黑火药着火时,发生如下氧化还原反应:
 。在此反应中,还原剂为
。在此反应中,还原剂为(2)湿法制备高铁酸钾
 是在碱性环境中进行,反应体系中有六种反应微粒:
是在碱性环境中进行,反应体系中有六种反应微粒: 、
、 、
、 、
、 、
、 、
、 。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:
。请依据上述信息,写出并配平湿法制高铁酸钾的离子方程式:(3)汽车剧烈碰撞时,安全气囊中发生反应:
 。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为
。若反应得到的氧化产物比还原产物多2.8mol,则此过程中转移电子的个数为(4)在第一次世界大战期间,德军在比利时的伊普雷战役中使用了氯气制造的毒气弹。现代工业常用氯气制备漂白粉、消毒液等物质。写出制备漂白粉的化学反应方程式
您最近半年使用:0次
解题方法
6 . 在工业生产中要制取某种物质,除了要考虑反应进行的可能性,还要考虑原料来源、成本高低和设备要求等因素,以选取最适当的方法。例如,工业上制取NaOH(a)一般不采用Na2O(b)与H2O(c)反应的方法(Na2O作为原料,来源少、成本高),而主要采用电解饱和食盐水的方法,过去也曾采用Na2CO3(d)与Ca(OH)2(e)反应的方法。回答下列问题:
(1)Na与水反应的离子方程式为______ 。
(2)电解饱和食盐水的化学方程式为2NaCl+2H2O 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。
①该反应中的还原剂为______ 填化学式,下同),被氧化的物质为______ 。
②用双线桥法表示该反应中电子转移的方向和数目:______ 。
③每生成0.2gH2,同时生成Cl2的质量为______ g。
(3)d和e反应可制得a:将Na2CO3溶液加入澄清石灰水中,发生反应的离子方程式为______ 。
(1)Na与水反应的离子方程式为
(2)电解饱和食盐水的化学方程式为2NaCl+2H2O
 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。①该反应中的还原剂为
②用双线桥法表示该反应中电子转移的方向和数目:
③每生成0.2gH2,同时生成Cl2的质量为
(3)d和e反应可制得a:将Na2CO3溶液加入澄清石灰水中,发生反应的离子方程式为
您最近半年使用:0次
7 . 回答下列问题:
(1)①H2+CuO Cu+H2O②CaCO3+2HCl=CaCl2+CO2↑+H2O③3S+6NaOH
Cu+H2O②CaCO3+2HCl=CaCl2+CO2↑+H2O③3S+6NaOH 2Na2S+Na2SO3+3H2O④Cu2O+4HCl=2HCuCl2+H2O,上述反应中,属于氧化还原反应的有
2Na2S+Na2SO3+3H2O④Cu2O+4HCl=2HCuCl2+H2O,上述反应中,属于氧化还原反应的有______ (填序号)。
(2)用双线桥法表示下述反应的电子转移的方向和数目______ 。
MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(3)在反应KClO3+6HCl=3Cl2+KCl+3H2O中,氧化剂与还原剂的系数之比为______ 。
(4)配平下面两个反应:
____H2O+____Cl2+____SO2=____H2SO4+____HCl,(系数是1的也请填上)______ 。
____KMnO4+____HCl=____KCl+____MnCl2+____Cl2↑+____H2O(系数是1的也请填上)______ 。
根据以上两个反应反应,写出由KMnO4、K2SO4、MnSO4、SO2、H2O、H2SO4这六种物质组成的氧化还原反应的方程式并配平。______ 。
(1)①H2+CuO
 Cu+H2O②CaCO3+2HCl=CaCl2+CO2↑+H2O③3S+6NaOH
Cu+H2O②CaCO3+2HCl=CaCl2+CO2↑+H2O③3S+6NaOH 2Na2S+Na2SO3+3H2O④Cu2O+4HCl=2HCuCl2+H2O,上述反应中,属于氧化还原反应的有
2Na2S+Na2SO3+3H2O④Cu2O+4HCl=2HCuCl2+H2O,上述反应中,属于氧化还原反应的有(2)用双线桥法表示下述反应的电子转移的方向和数目
MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。(3)在反应KClO3+6HCl=3Cl2+KCl+3H2O中,氧化剂与还原剂的系数之比为
(4)配平下面两个反应:
____H2O+____Cl2+____SO2=____H2SO4+____HCl,(系数是1的也请填上)
____KMnO4+____HCl=____KCl+____MnCl2+____Cl2↑+____H2O(系数是1的也请填上)
根据以上两个反应反应,写出由KMnO4、K2SO4、MnSO4、SO2、H2O、H2SO4这六种物质组成的氧化还原反应的方程式并配平。
您最近半年使用:0次
解题方法
8 . 煤的气化是煤炭综合利用的重要途径之一,主要反应为C+H2O(g)  CO+H2。
CO+H2。
(1)该反应中,化合价升高的元素是___________ (填元素符号),氧化剂是___________ (填化学式),氧化产物是___________ (填化学式)。
(2)若消耗了1 mol C,则生成CO的体积约是___________ L(标准状况),转移电子的物质的量为___________ mol。
 CO+H2。
CO+H2。(1)该反应中,化合价升高的元素是
(2)若消耗了1 mol C,则生成CO的体积约是
您最近半年使用:0次
9 . 取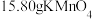 ,加热分解后剩余固体
,加热分解后剩余固体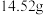 ,该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以
,该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以 存在,请计算:
存在,请计算:
(1)写出 受热分解的化学方程式
受热分解的化学方程式__________ 。
(2) 的分解率
的分解率__________ 。
(3)气体A的物质的量_________ 。
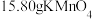 ,加热分解后剩余固体
,加热分解后剩余固体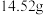 ,该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以
,该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以 存在,请计算:
存在,请计算:(1)写出
 受热分解的化学方程式
受热分解的化学方程式(2)
 的分解率
的分解率(3)气体A的物质的量
您最近半年使用:0次
名校
解题方法
10 . 某100 mL的CuCl2溶液中,已知溶液中的Cl-的浓度为0.2 mol·L-1。现将一定量的铁粉投入到该溶液中,若反应后溶液体积不变,回答下列问题:
(1)原溶液中Cu2+的浓度为___________ ;
(2)反应后测得Cl-的浓度为___________ ;
(3)反应中氧化剂是___________ ,反应后测得溶液中Fe2+的浓度为0.05 mol/L,则反应生成铜单质的质量为___________ g,转移电子___________ 个;
(4)剩余的Cu2+的物质的量浓度为___________ 。
(1)原溶液中Cu2+的浓度为
(2)反应后测得Cl-的浓度为
(3)反应中氧化剂是
(4)剩余的Cu2+的物质的量浓度为
您最近半年使用:0次



