解题方法
1 . 把3.04g某铁的氧化物FexO分成两等份,第一份溶于足量盐酸后向溶液中通入标准状况下Cl2112mL,恰好将Fe2+完全氧化;第二份混合物中加入100mL氢碘酸溶液,恰好完全反应,在反应后的溶液中加KSCN溶液,无现象。试计算:
(1)x的值为___________ 。
(2)氢碘酸溶液的物质的量浓度c(HI)___________ 。
(1)x的值为
(2)氢碘酸溶液的物质的量浓度c(HI)
您最近一年使用:0次
名校
2 . 取48.0gFe2O3,一定温度下加热,残留固体47.36g。将该剩余固体溶于足量盐酸,此过程没有气体产生;所得溶液中再加入足量KI溶液。请计算:
(1)生成I2的物质的量_____ 。
(2)若分解产物为Fe3O4,求Fe2O3的分解率_____ 。
(1)生成I2的物质的量
(2)若分解产物为Fe3O4,求Fe2O3的分解率
您最近一年使用:0次
2021-11-05更新
|
337次组卷
|
2卷引用:浙江省诸暨市2017-2018学年高三上学期期末考试化学试题
解题方法
3 . 氙和氟气反应,生成含有XeF2和XeF4的固体混合物,现用两份等质量的此种固体混合物,分别做下面的化学分析:
①用水处理此固体,获得60. 2mL气体(在17°C和1.00×105Pa条件下),其中有24. 1mL是氧气,其余的是氙气,水溶液中的XeO3可以氧化30. 0mL。浓度为0. 100 mol/L的Fe2+。
②用KI溶液处理此固体,获得单质碘,此碘需要35.0mL浓度为0.200mol/L的Na2S2O3与之完全反应。
试求:此固体混合物中XeF2和XeF4的物质的量分数___________ 。(提示:XeF2与H2O仅发生氧化还原反应;XeF4与H2O反应时,有一半的XeF4与水发生氧化还原反应,另一半的XeF4则发生歧化反应。)
①用水处理此固体,获得60. 2mL气体(在17°C和1.00×105Pa条件下),其中有24. 1mL是氧气,其余的是氙气,水溶液中的XeO3可以氧化30. 0mL。浓度为0. 100 mol/L的Fe2+。
②用KI溶液处理此固体,获得单质碘,此碘需要35.0mL浓度为0.200mol/L的Na2S2O3与之完全反应。
试求:此固体混合物中XeF2和XeF4的物质的量分数
您最近一年使用:0次
4 . Ⅰ.如图所示,一密闭容器被无摩擦可滑动的两隔板a和b分成甲、乙两室。标准状况下,在乙室中充入0.6 mol HCl,甲室中充入NH3、H2的混合气体,静止时活塞位置如下图。已知甲、乙两室中气体的质量之差为10.9 g。

(1)甲室中NH3、H2的物质的量之比为___________ ,质量之比为___________ 。
(2)甲室中气体的物质的量为___________ mol。
(3)甲室中气体的质量为___________ g。
(4)将隔板a去掉,发生下列反应:HCl(g)+NH3(g)=NH4Cl(s),当HCl与NH3完全反应后,活塞b将位于刻度“___________ ”处(填数字)。
Ⅱ.(1)向mg镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL。向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是___________ 。
A. p=m+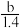 B.p=m+
B.p=m+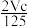 C.n=m+
C.n=m+ D. n=m+
D. n=m+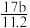
(2)一定体积的KMnO4溶液恰好能氧化一定质量的KHC2O4·H2C2O4·2H2O。若用0.1000mol·L-1的NaOH溶液中和相同质量的KHC2O4·H2C2O4·2H2O,所需NaOH溶液的体积恰好为KMnO4溶液的3倍,则KMnO4溶液的浓度(mol·L-1)为___________ 。提示:①H2C2O4是二元弱酸 ②10KHC2O4·H2C2O4+8KMnO4+17H2SO4=8MnSO4+9K2SO4+40CO2↑+32H2O

(1)甲室中NH3、H2的物质的量之比为
(2)甲室中气体的物质的量为
(3)甲室中气体的质量为
(4)将隔板a去掉,发生下列反应:HCl(g)+NH3(g)=NH4Cl(s),当HCl与NH3完全反应后,活塞b将位于刻度“
Ⅱ.(1)向mg镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL。向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。再将得到的沉淀灼烧至质量不再改变为止,得到固体p g。则下列关系不正确的是
A. p=m+
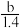 B.p=m+
B.p=m+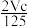 C.n=m+
C.n=m+ D. n=m+
D. n=m+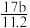
(2)一定体积的KMnO4溶液恰好能氧化一定质量的KHC2O4·H2C2O4·2H2O。若用0.1000mol·L-1的NaOH溶液中和相同质量的KHC2O4·H2C2O4·2H2O,所需NaOH溶液的体积恰好为KMnO4溶液的3倍,则KMnO4溶液的浓度(mol·L-1)为
您最近一年使用:0次
5 . 钒是人体不可缺少的元素,Heyliger 等首次报道了偏钒酸钠显著降低糖尿病大鼠血糖的作用后,钒化学的研究得到了很大发展。钒及其化合物也广泛应用于特种钢、催化剂、颜料、染料、电子材料及防腐剂等等领域。
(1)钒酸盐与磷酸盐结构相似。请画出VO 、H2VO
、H2VO 、VO2(H2O)
、VO2(H2O)  和V2O
和V2O 的空间构型
的空间构型__________ 。
(2)生理条件下的钒以多种氧化态存在,各种氧化态可以相互转化。通常细胞外的钒是V(V), 。而细胞内的钒是V(IV)。研究表明,钒酸二氢根离子可与亚铁血红素(Mtrc-Fe2+)反应,写出该反应的离子方程式__________ 。
(3)①已知配合物[VON(CH2COO)3]在水溶液中的几何构型是唯一 的,画出它的空间构型图__________ 。
②理论推测上述配合物分子在晶体中是有手性的,指出产生手性的原因__________ 。
(4)钒酸钇晶体是近年来新开发出的优良双折射光学晶体,在光电产业中得到广泛应用。可以在弱碱性溶液中用偏钒酸铵和硝酸钇合成。写出以Y2O3与V2O5为主要原料合成钒酸钇的化学方程式__________ 。
(5)若以市售分析纯偏钒酸铵为原料制备高纯钒酸钇单晶,需将杂质铁离子含量降至一定数量级。设每升偏钒酸铵溶液中含三价铁离子为5.0 ×10-5 mol,用0.01 mol dm-3的鏊合剂除铁。
①说明不采取使铁离子水解析出沉淀的方法除铁的理由__________ 。
②通过计算说明如何选择螯合剂使偏钒酸铵含铁量降至10-30moldm-3以下__________ 。
(1)钒酸盐与磷酸盐结构相似。请画出VO
 、H2VO
、H2VO 、VO2(H2O)
、VO2(H2O)  和V2O
和V2O 的空间构型
的空间构型(2)生理条件下的钒以多种氧化态存在,各种氧化态可以相互转化。通常细胞外的钒是V(V), 。而细胞内的钒是V(IV)。研究表明,钒酸二氢根离子可与亚铁血红素(Mtrc-Fe2+)反应,写出该反应的离子方程式
(3)①已知配合物[VON(CH2COO)3]在水溶液中的几何构型是唯一 的,画出它的空间构型图
②理论推测上述配合物分子在晶体中是有手性的,指出产生手性的原因
(4)钒酸钇晶体是近年来新开发出的优良双折射光学晶体,在光电产业中得到广泛应用。可以在弱碱性溶液中用偏钒酸铵和硝酸钇合成。写出以Y2O3与V2O5为主要原料合成钒酸钇的化学方程式
(5)若以市售分析纯偏钒酸铵为原料制备高纯钒酸钇单晶,需将杂质铁离子含量降至一定数量级。设每升偏钒酸铵溶液中含三价铁离子为5.0 ×10-5 mol,用0.01 mol dm-3的鏊合剂除铁。
①说明不采取使铁离子水解析出沉淀的方法除铁的理由
②通过计算说明如何选择螯合剂使偏钒酸铵含铁量降至10-30moldm-3以下
| 配离子 |  |
| [Fe(edta)]2- [Fe(edta)]- [Fe(phen)3]2+ [Fe(phen)3]3+ | 2.1×1014 1.7×1024 2.0×1021 1.3×1014 |
| 沉淀 | Ksp |
| Fe(OH)2 Fe(OH)3 | 8.0×10-16 4.0×10-38 |
您最近一年使用:0次
6 . 饮用水中NO 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO
的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO 还原为N2。
还原为N2。
(1)①配平方程式:_______Al+____NO +_____OH↑+____=_____[Al(OH)4] ↑+____N2↑
+_____OH↑+____=_____[Al(OH)4] ↑+____N2↑
______
②上述反应中,还原剂与还原产物的物质的量之比是_______ ,反应中转移电子0.3mol,生成_______ mLN2(标准状况下)。
(2)①已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为_______ 。
②Na2S2O3具有较强还原性,能作为织锦物漂白后的脱氯剂,脱氯后S2O 转变为SO
转变为SO 。现需处理含标准状况下2.24L Cl2的织锦物,理论上需要0.1mol/L Na2S2O3溶液的体积为
。现需处理含标准状况下2.24L Cl2的织锦物,理论上需要0.1mol/L Na2S2O3溶液的体积为_______ mL。
 对人类健康会产生危害,为了降低饮用水中NO
对人类健康会产生危害,为了降低饮用水中NO 的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO
的浓度,某饮用水研究人员提出,可在碱性条件下用铝粉将NO 还原为N2。
还原为N2。(1)①配平方程式:_______Al+____NO
 +_____OH↑+____=_____[Al(OH)4] ↑+____N2↑
+_____OH↑+____=_____[Al(OH)4] ↑+____N2↑②上述反应中,还原剂与还原产物的物质的量之比是
(2)①已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为
②Na2S2O3具有较强还原性,能作为织锦物漂白后的脱氯剂,脱氯后S2O
 转变为SO
转变为SO 。现需处理含标准状况下2.24L Cl2的织锦物,理论上需要0.1mol/L Na2S2O3溶液的体积为
。现需处理含标准状况下2.24L Cl2的织锦物,理论上需要0.1mol/L Na2S2O3溶液的体积为
您最近一年使用:0次
7 . (1)相同体积的三种溶液 、
、 、
、 ,所含
,所含 的物质的量浓度相同,各溶质的物质的量浓度之比为
的物质的量浓度相同,各溶质的物质的量浓度之比为___________ 。
(2)已知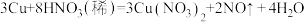 ;该反应中,若被还原的
;该反应中,若被还原的 为1mol,转移电子的物质的量为
为1mol,转移电子的物质的量为___________ mol。
(3)将15.8gNaOH与 的混合物全部溶于一定量的水中,生成气体体积为1.12L(标况下)。若反应后溶液中的粒子个数关系为:
的混合物全部溶于一定量的水中,生成气体体积为1.12L(标况下)。若反应后溶液中的粒子个数关系为: ,则原混合物中NaOH与
,则原混合物中NaOH与 的物质的量之比为
的物质的量之比为___________ ;形成这样的溶液,所需水的体积为___________ mL(水的密度以1.00 计)。
计)。
 、
、 、
、 ,所含
,所含 的物质的量浓度相同,各溶质的物质的量浓度之比为
的物质的量浓度相同,各溶质的物质的量浓度之比为(2)已知
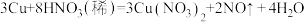 ;该反应中,若被还原的
;该反应中,若被还原的 为1mol,转移电子的物质的量为
为1mol,转移电子的物质的量为(3)将15.8gNaOH与
 的混合物全部溶于一定量的水中,生成气体体积为1.12L(标况下)。若反应后溶液中的粒子个数关系为:
的混合物全部溶于一定量的水中,生成气体体积为1.12L(标况下)。若反应后溶液中的粒子个数关系为: ,则原混合物中NaOH与
,则原混合物中NaOH与 的物质的量之比为
的物质的量之比为 计)。
计)。
您最近一年使用:0次
8 . (1)0.2molNH3的质量为_______ g
(2)配制250mL1.0mol/LH2SO4溶液,需要18mol/LH2SO4溶液体积是___ 。
(3)我国古代四大发明之一的黑火药是由硫粉、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C=K2S+N2↑+3CO2↑,反应中被还原的物质是____ (填化学式);1mol硫参加反应时转移电子数为_____ 。
(4)已知NH3和Cl2可以发生氧化还原反应,配平该方程式:NH3+Cl2=N2+HCl,_______ 。
(2)配制250mL1.0mol/LH2SO4溶液,需要18mol/LH2SO4溶液体积是
(3)我国古代四大发明之一的黑火药是由硫粉、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C=K2S+N2↑+3CO2↑,反应中被还原的物质是
(4)已知NH3和Cl2可以发生氧化还原反应,配平该方程式:NH3+Cl2=N2+HCl,
您最近一年使用:0次
名校
9 . 氧化还原反应是一类重要的反应,请按要求完成下列题目。
(1)实验室可用该反应制取氯气: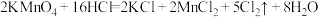 ,若有
,若有 参加反应,转移的电子数目是
参加反应,转移的电子数目是___ ,被氧化的 的物质的量是
的物质的量是__ ,请用双线桥法标出该反应电子转移的方向和数目: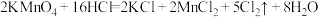 ,
,___ 。
(2)酸性 溶液可与
溶液可与 发生反应,已知
发生反应,已知 被还原为
被还原为 ,则氧化剂与还原剂的物质的量之比为
,则氧化剂与还原剂的物质的量之比为__ 。
(3)已知: ,
, 。
。
①向含有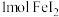 和
和 的溶液中通入
的溶液中通入 ,此时被氧化的离子是
,此时被氧化的离子是__ 。
②某溶液中含有大量的 、
、 、
、 ,若向
,若向 该混合溶液中通入一定量的
该混合溶液中通入一定量的 ,溶液中
,溶液中 、
、 、
、 的物质的量与通入
的物质的量与通入 的体积(标准状况)的关系如下表所示,分析后回答下列问题:
的体积(标准状况)的关系如下表所示,分析后回答下列问题:
原溶液中 、
、 、
、 的物质的量浓度之比为
的物质的量浓度之比为_______ 。
(1)实验室可用该反应制取氯气:
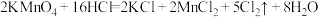 ,若有
,若有 参加反应,转移的电子数目是
参加反应,转移的电子数目是 的物质的量是
的物质的量是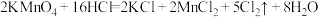 ,
,(2)酸性
 溶液可与
溶液可与 发生反应,已知
发生反应,已知 被还原为
被还原为 ,则氧化剂与还原剂的物质的量之比为
,则氧化剂与还原剂的物质的量之比为(3)已知:
 ,
, 。
。①向含有
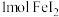 和
和 的溶液中通入
的溶液中通入 ,此时被氧化的离子是
,此时被氧化的离子是②某溶液中含有大量的
 、
、 、
、 ,若向
,若向 该混合溶液中通入一定量的
该混合溶液中通入一定量的 ,溶液中
,溶液中 、
、 、
、 的物质的量与通入
的物质的量与通入 的体积(标准状况)的关系如下表所示,分析后回答下列问题:
的体积(标准状况)的关系如下表所示,分析后回答下列问题: 的体积(标准状况) 的体积(标准状况) |  |  |  |
 | 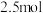 |  | 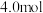 |
 |  | 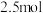 |  |
 |  | 0 | 0 |
原溶液中
 、
、 、
、 的物质的量浓度之比为
的物质的量浓度之比为
您最近一年使用:0次
解题方法
10 . (1)质量比为16:7:6的三种气体SO2、CO、NO,分子个数之比为_______ ;氧原子个数之比为_______ ;相同条件下体积比为_______ 。
(2)等质量的O2和SO2,物质的量之比为_______ ,在相同条件下的体积之比为_______ ,原子数之比为_______ 。
(3)在反应KIO3+6HI=3I2+KI+3H2O中,氧化剂与还原剂的物质的量之比为_______ 。
(4)Na2CO3溶液与CH3COOH溶液反应的离子方程式为_______
(5)大理石(CaCO3)与稀HNO3反应的离子方程式为:_______
(6)将少量NaHSO4溶液滴加到Ba(OH)2溶液中,当恰好沉淀时,反应的离子方程式为_______ 。
(2)等质量的O2和SO2,物质的量之比为
(3)在反应KIO3+6HI=3I2+KI+3H2O中,氧化剂与还原剂的物质的量之比为
(4)Na2CO3溶液与CH3COOH溶液反应的离子方程式为
(5)大理石(CaCO3)与稀HNO3反应的离子方程式为:
(6)将少量NaHSO4溶液滴加到Ba(OH)2溶液中,当恰好沉淀时,反应的离子方程式为
您最近一年使用:0次



