(1)质量比为16:7:6的三种气体SO2、CO、NO,分子个数之比为_______ ;氧原子个数之比为_______ ;相同条件下体积比为_______ 。
(2)等质量的O2和SO2,物质的量之比为_______ ,在相同条件下的体积之比为_______ ,原子数之比为_______ 。
(3)在反应KIO3+6HI=3I2+KI+3H2O中,氧化剂与还原剂的物质的量之比为_______ 。
(4)Na2CO3溶液与CH3COOH溶液反应的离子方程式为_______
(5)大理石(CaCO3)与稀HNO3反应的离子方程式为:_______
(6)将少量NaHSO4溶液滴加到Ba(OH)2溶液中,当恰好沉淀时,反应的离子方程式为_______ 。
(2)等质量的O2和SO2,物质的量之比为
(3)在反应KIO3+6HI=3I2+KI+3H2O中,氧化剂与还原剂的物质的量之比为
(4)Na2CO3溶液与CH3COOH溶液反应的离子方程式为
(5)大理石(CaCO3)与稀HNO3反应的离子方程式为:
(6)将少量NaHSO4溶液滴加到Ba(OH)2溶液中,当恰好沉淀时,反应的离子方程式为
更新时间:2021-04-04 07:30:19
|
相似题推荐
【推荐1】碱式硫酸铁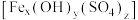 (Fe元素为+3价)是一种新型高效絮凝剂。为确定该碱式硫酸铁
(Fe元素为+3价)是一种新型高效絮凝剂。为确定该碱式硫酸铁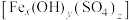 的化学式,进行了如下实验∶
的化学式,进行了如下实验∶
步骤 1.称取一定量样品完全溶于稀盐酸中,配成100.00mL溶液。
步骤2.取步骤1所得溶液25.00 mL,加入足量 BaCl2溶液,充分反应,静置、过滤、洗涤、干燥,称得沉淀 2.330 g。
步骤3.另取步骤1所得溶液25.00mL,加入足量的某试剂(与酸性KMnO4溶液不反应),将 Fe3+完全还原为 Fe2+,再向其中滴加 0.1000 mol·L-1酸性 KMnO4溶液,测得 Fe2+恰好完全反应时消耗 KMnO4溶液 16.00 mL。
已知∶ (未配平)
(未配平)
通过计算确定该碱式硫酸铁的化学式______ 。(写出计算过程)
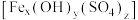 (Fe元素为+3价)是一种新型高效絮凝剂。为确定该碱式硫酸铁
(Fe元素为+3价)是一种新型高效絮凝剂。为确定该碱式硫酸铁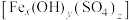 的化学式,进行了如下实验∶
的化学式,进行了如下实验∶步骤 1.称取一定量样品完全溶于稀盐酸中,配成100.00mL溶液。
步骤2.取步骤1所得溶液25.00 mL,加入足量 BaCl2溶液,充分反应,静置、过滤、洗涤、干燥,称得沉淀 2.330 g。
步骤3.另取步骤1所得溶液25.00mL,加入足量的某试剂(与酸性KMnO4溶液不反应),将 Fe3+完全还原为 Fe2+,再向其中滴加 0.1000 mol·L-1酸性 KMnO4溶液,测得 Fe2+恰好完全反应时消耗 KMnO4溶液 16.00 mL。
已知∶
 (未配平)
(未配平)通过计算确定该碱式硫酸铁的化学式
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】请按要求,回答下列问题:
(1)同温同压下,0.3mol氧气和0.2mol臭氧(O3)的质量比为_______ 。
(2)某气体的质量为3.4g,含有6.02×1022个分子,则该气体的摩尔质量为_______ 。
(3)将34.2g Al2(SO4)3溶于水配成250mL溶液,溶液中SO 的物质的量浓度为
的物质的量浓度为_______ 。
(4)7.8g Na2O2与CO2反应时,转移的电子数为_______ 。
(1)同温同压下,0.3mol氧气和0.2mol臭氧(O3)的质量比为
(2)某气体的质量为3.4g,含有6.02×1022个分子,则该气体的摩尔质量为
(3)将34.2g Al2(SO4)3溶于水配成250mL溶液,溶液中SO
 的物质的量浓度为
的物质的量浓度为(4)7.8g Na2O2与CO2反应时,转移的电子数为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】钾是活泼的碱金属,钾和氧有氧化钾(K2O)、过氧化钾(K2O2)和超氧化钾(KO2)等多种化合物。
(1)钾和硝酸钾反应可制得K2O(10K+2KNO3 = 6K2O+N2↑),39.0g钾与10.1g硝酸钾充分反应生成K2O的物质的量为__________ mol。
(2)某过氧化钾样品中氧的质量分数(杂质不含氧)为0.28,则样品中K2O2的质量分数为_____________ 。
(3)超氧化钾和二氧化碳反应生成氧气(4KO2+2CO2→2K2CO2+3O2),在医院、矿井、潜水、高空飞行中用作供氧剂。13.2L(标准状况)CO2和KO2反应后,气体体积变为18.8L(标准状况),列式计算反应消耗的KO2的物质的量__________ mol。
(1)钾和硝酸钾反应可制得K2O(10K+2KNO3 = 6K2O+N2↑),39.0g钾与10.1g硝酸钾充分反应生成K2O的物质的量为
(2)某过氧化钾样品中氧的质量分数(杂质不含氧)为0.28,则样品中K2O2的质量分数为
(3)超氧化钾和二氧化碳反应生成氧气(4KO2+2CO2→2K2CO2+3O2),在医院、矿井、潜水、高空飞行中用作供氧剂。13.2L(标准状况)CO2和KO2反应后,气体体积变为18.8L(标准状况),列式计算反应消耗的KO2的物质的量
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】在工业生产中要制取某种物质,除了要考虑反应进行的可能性,还要考虑原料来源、成本高低和设备要求等因素,以选取最适当的方法。例如,工业上制取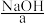 一般不采用
一般不采用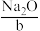 与
与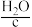 反应的方法(Na2O作为原料,来源少、成本高),而主要采用电解饱和食盐水的方法,过去也曾采用
反应的方法(Na2O作为原料,来源少、成本高),而主要采用电解饱和食盐水的方法,过去也曾采用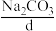 与
与 且2反应的方法。
且2反应的方法。
回答下列问题:
(1)Na与水反应的离子方程式为________ 。
(2)电解饱和食盐水的化学方程式为2NaCl+2H2O 2NaOH+H2↑+Cl2↑:
2NaOH+H2↑+Cl2↑:
①该反应中的还原剂为_______ (填化学式,下同),被氧化的物质为________ 。
②用单线桥法表示该反应中电子转移的方向和数目:_______ 。
③每生成0.2gH2,同时生成Cl2的质量为________  。
。
(3)d和e反应可制得a:
①碳酸钠的俗称为________ 。
②从碳酸钠组成的阴离子来看,其属于_______ 盐。
③将Na2CO3溶液加入澄清石灰水中,发生反应的离子方程式为_______ 。
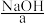 一般不采用
一般不采用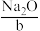 与
与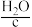 反应的方法(Na2O作为原料,来源少、成本高),而主要采用电解饱和食盐水的方法,过去也曾采用
反应的方法(Na2O作为原料,来源少、成本高),而主要采用电解饱和食盐水的方法,过去也曾采用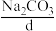 与
与 且2反应的方法。
且2反应的方法。回答下列问题:
(1)Na与水反应的离子方程式为
(2)电解饱和食盐水的化学方程式为2NaCl+2H2O
 2NaOH+H2↑+Cl2↑:
2NaOH+H2↑+Cl2↑:①该反应中的还原剂为
②用单线桥法表示该反应中电子转移的方向和数目:
③每生成0.2gH2,同时生成Cl2的质量为
 。
。(3)d和e反应可制得a:
①碳酸钠的俗称为
②从碳酸钠组成的阴离子来看,其属于
③将Na2CO3溶液加入澄清石灰水中,发生反应的离子方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】氮的化合物是化学研究的热点之一,请回答下列问题:
(1)汽车尾气中的 、
、 在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出
在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出 被
被 还原的化学方程式
还原的化学方程式_______ ,并用双线桥法标出电子转移的方向和数目。
(2)氮氧化物是造成雾霾天气的主要原因之一,利用 和
和 的溶液处理氮氧化物的反应过程如下:
的溶液处理氮氧化物的反应过程如下:
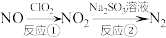
反应①的化学方程式是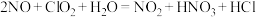 ,反应②的离子方程式是
,反应②的离子方程式是_______ ;若有1.4g 生成,需消耗
生成,需消耗
_______ g。
亚硝酸钠有咸味,有毒。已知: 。
。
(3)上述反应的还原剂为_______ (填化学式);若反应中有1分子 气体生成,则转移电子的数目为
气体生成,则转移电子的数目为_______ 。
(4)在酸性条件下,高锰酸钾可将 氧化为
氧化为 ,所得溶液中锰元素仅以
,所得溶液中锰元素仅以 形式存在,写出此反应的离子方程式:
形式存在,写出此反应的离子方程式:_______ 。
(1)汽车尾气中的
 、
、 在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出
在适宜温度下采用催化转化法处理,使它们相互反应生成参与大气循环的无毒气体。写出 被
被 还原的化学方程式
还原的化学方程式(2)氮氧化物是造成雾霾天气的主要原因之一,利用
 和
和 的溶液处理氮氧化物的反应过程如下:
的溶液处理氮氧化物的反应过程如下: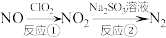
反应①的化学方程式是
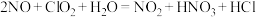 ,反应②的离子方程式是
,反应②的离子方程式是 生成,需消耗
生成,需消耗
亚硝酸钠有咸味,有毒。已知:
 。
。(3)上述反应的还原剂为
 气体生成,则转移电子的数目为
气体生成,则转移电子的数目为(4)在酸性条件下,高锰酸钾可将
 氧化为
氧化为 ,所得溶液中锰元素仅以
,所得溶液中锰元素仅以 形式存在,写出此反应的离子方程式:
形式存在,写出此反应的离子方程式:
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】在工业生产中要制取某种物质,除了要考虑反应进行的可能性,还要考虑原料来源、成本高低和设备要求等因素,以选取最适当的方法。例如,工业上制取NaOH(a)一般不采用Na2O(b)与H2O(c)反应的方法(Na2O作为原料,来源少、成本高),而主要采用电解饱和食盐水的方法,过去也曾采用Na2CO3(d)与Ca(OH)2(e)反应的方法。回答下列问题:
(1)Na与水反应的离子方程式为______ 。
(2)电解饱和食盐水的化学方程式为2NaCl+2H2O 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。
①该反应中的还原剂为______ 填化学式,下同),被氧化的物质为______ 。
②用双线桥法表示该反应中电子转移的方向和数目:______ 。
③每生成0.2gH2,同时生成Cl2的质量为______ g。
(3)d和e反应可制得a:将Na2CO3溶液加入澄清石灰水中,发生反应的离子方程式为______ 。
(1)Na与水反应的离子方程式为
(2)电解饱和食盐水的化学方程式为2NaCl+2H2O
 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。①该反应中的还原剂为
②用双线桥法表示该反应中电子转移的方向和数目:
③每生成0.2gH2,同时生成Cl2的质量为
(3)d和e反应可制得a:将Na2CO3溶液加入澄清石灰水中,发生反应的离子方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】将2.56g硫与足量NaOH的热溶液充分反应生成Na2S和Na2S2O3,然后向生成物中加入足量的NaClO和NaOH的混合溶液,硫元素全部转化为Na2SO4,第二步过程中转移电子nmol.求:n=____ mol;写出计算过程__________ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】叠氮化钠(NaN3)是一种无色晶体,易溶于水,微溶于乙醇,不溶于乙醚,广泛应用于汽车安全气囊。某硝酸工厂拟通过下列方法处理尾气并制备叠氮化钠。
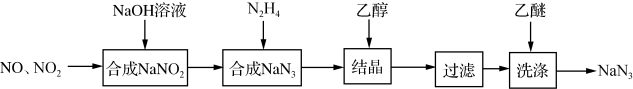
(1)NO和NO2混合气体与NaOH溶液反应可以合成NaNO2,写出该反应的化学方程式___ ,生成1molNaNO2时转移电子___ mol。
(2)汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3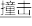 K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
①该反应中的氧化剂为___ ,还原剂为___ (填化学式)。
②欲使气囊中充满标准状况下氮气,则该安全气囊中生成的K2O和Na2O的总质量为多少克___ ?(写出计算过程,保留一位小数,不考虑固体的体积)。

(1)NO和NO2混合气体与NaOH溶液反应可以合成NaNO2,写出该反应的化学方程式
(2)汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3
 K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。①该反应中的氧化剂为
②欲使气囊中充满标准状况下氮气,则该安全气囊中生成的K2O和Na2O的总质量为多少克
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,该反应中Na2O2 是___________ (填氧化剂、还原剂)
(2)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:__________________ 。
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为__________ mol。
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是______ 。
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+、Br-完全被氧化时,c=__________ (用含a、b的代数式表示)。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,该反应中Na2O2 是
(2)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+、Br-完全被氧化时,c=
您最近一年使用:0次



