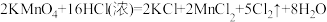叠氮化钠(NaN3)是一种无色晶体,易溶于水,微溶于乙醇,不溶于乙醚,广泛应用于汽车安全气囊。某硝酸工厂拟通过下列方法处理尾气并制备叠氮化钠。
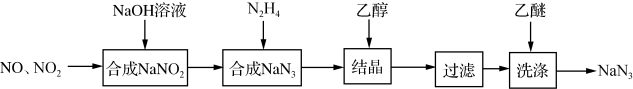
(1)NO和NO2混合气体与NaOH溶液反应可以合成NaNO2,写出该反应的化学方程式___ ,生成1molNaNO2时转移电子___ mol。
(2)汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3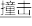 K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
①该反应中的氧化剂为___ ,还原剂为___ (填化学式)。
②欲使气囊中充满标准状况下氮气,则该安全气囊中生成的K2O和Na2O的总质量为多少克___ ?(写出计算过程,保留一位小数,不考虑固体的体积)。

(1)NO和NO2混合气体与NaOH溶液反应可以合成NaNO2,写出该反应的化学方程式
(2)汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3
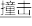 K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。
K2O+5Na2O+16N2↑。假定汽车中某个安全气囊容积为56L。①该反应中的氧化剂为
②欲使气囊中充满标准状况下氮气,则该安全气囊中生成的K2O和Na2O的总质量为多少克
更新时间:2021-04-20 14:56:38
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】用KMnO4氧化溶质质量分数为36.5%的盐酸。反应方程式如下:
2KMnO4+16HCl(浓)=2KCl+2MnCl 2+5Cl 2↑+8H2O
⑴此反应中氧化剂是________ ,氧化产物______ 。若有1mol KMnO4参加反应,转移电子的物质的量为__________ 。
⑵15.8g KMnO4完全反应,产生的Cl 2在标准状况下的体积为_____ ,有______ molHCl发生反应,有______ molHCl被氧化。
⑶若此盐酸的密度为1.2g/cm3,其物质的量浓度为______ 。
2KMnO4+16HCl(浓)=2KCl+2MnCl 2+5Cl 2↑+8H2O
⑴此反应中氧化剂是
⑵15.8g KMnO4完全反应,产生的Cl 2在标准状况下的体积为
⑶若此盐酸的密度为1.2g/cm3,其物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】实验室用MnO2和浓盐酸制氯气的反应为MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑。反应中,如果有17.4 g MnO2被还原,那么:
MnCl2+2H2O+Cl2↑。反应中,如果有17.4 g MnO2被还原,那么:
(1)产生的Cl2在标准状况下的体积为__________ ;
(2)转移电子的物质的量为_______________ ;
(3)纺织工业中常用氯气作漂白剂,漂白布匹后,过量的氯需要除去,通常可用Na2SO3作“脱氯剂”,脱氯后的产物为Na2SO4,氯变为-1价。若把本题中产生的Cl2完全转化,需要Na2SO3的质量为____________________________ 。
 MnCl2+2H2O+Cl2↑。反应中,如果有17.4 g MnO2被还原,那么:
MnCl2+2H2O+Cl2↑。反应中,如果有17.4 g MnO2被还原,那么:(1)产生的Cl2在标准状况下的体积为
(2)转移电子的物质的量为
(3)纺织工业中常用氯气作漂白剂,漂白布匹后,过量的氯需要除去,通常可用Na2SO3作“脱氯剂”,脱氯后的产物为Na2SO4,氯变为-1价。若把本题中产生的Cl2完全转化,需要Na2SO3的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】一种由CuO和KHC2O4溶液反应得到的蓝色结晶[KaCub(C2O4)c·dH2O]。为测定其组成,进行了如下实验:
步骤1:称取3.5400g该晶体,加入过量稀硫酸,待样品完全溶解后加入适量水,配制成100mL溶液A。
步骤2:量取20.00mLA溶液,滴加0.2000mol·L-1KMnO4溶液至恰好完全反应时,消耗KMnO4溶液8.00mL。
步骤3:另取20.00mLA溶液,加入足量NaOH溶液,充分反应后,经过滤、洗涤、灼烧、称重,得到黑色固体粉末0.16g。
已知:步骤2中发生反应如下,请配平:___ 。
 + H2C2O4+ H+= Mn2++ CO2↑+ H2O
+ H2C2O4+ H+= Mn2++ CO2↑+ H2O
(1)3.5400g该样品中含n( )=
)=___ mol。
(2)3.5400g该样品中含n(Cu2+)=___ mol。
(3)通过计算确定该蓝色晶体的化学式(计算过程)___ 。
步骤1:称取3.5400g该晶体,加入过量稀硫酸,待样品完全溶解后加入适量水,配制成100mL溶液A。
步骤2:量取20.00mLA溶液,滴加0.2000mol·L-1KMnO4溶液至恰好完全反应时,消耗KMnO4溶液8.00mL。
步骤3:另取20.00mLA溶液,加入足量NaOH溶液,充分反应后,经过滤、洗涤、灼烧、称重,得到黑色固体粉末0.16g。
已知:步骤2中发生反应如下,请配平:
 + H2C2O4+ H+= Mn2++ CO2↑+ H2O
+ H2C2O4+ H+= Mn2++ CO2↑+ H2O(1)3.5400g该样品中含n(
 )=
)=(2)3.5400g该样品中含n(Cu2+)=
(3)通过计算确定该蓝色晶体的化学式(计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)已知KMnO4与浓盐酸反应如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
①作还原剂的物质是___ 。
②若反应中每生成5molCl2,转移电子数目为___ 。
(2)19g某二价金属氯化物(ACl2)中含有0.4molCl-,则ACl2的相对分子质量是___ ;ACl2的化学式是____ 。
(3)将适量铁粉加到三氯化铁溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是___ 。
①作还原剂的物质是
②若反应中每生成5molCl2,转移电子数目为
(2)19g某二价金属氯化物(ACl2)中含有0.4molCl-,则ACl2的相对分子质量是
(3)将适量铁粉加到三氯化铁溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是
您最近一年使用:0次