碱式硫酸铁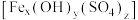 (Fe元素为+3价)是一种新型高效絮凝剂。为确定该碱式硫酸铁
(Fe元素为+3价)是一种新型高效絮凝剂。为确定该碱式硫酸铁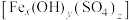 的化学式,进行了如下实验∶
的化学式,进行了如下实验∶
步骤 1.称取一定量样品完全溶于稀盐酸中,配成100.00mL溶液。
步骤2.取步骤1所得溶液25.00 mL,加入足量 BaCl2溶液,充分反应,静置、过滤、洗涤、干燥,称得沉淀 2.330 g。
步骤3.另取步骤1所得溶液25.00mL,加入足量的某试剂(与酸性KMnO4溶液不反应),将 Fe3+完全还原为 Fe2+,再向其中滴加 0.1000 mol·L-1酸性 KMnO4溶液,测得 Fe2+恰好完全反应时消耗 KMnO4溶液 16.00 mL。
已知∶ (未配平)
(未配平)
通过计算确定该碱式硫酸铁的化学式______ 。(写出计算过程)
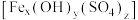 (Fe元素为+3价)是一种新型高效絮凝剂。为确定该碱式硫酸铁
(Fe元素为+3价)是一种新型高效絮凝剂。为确定该碱式硫酸铁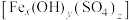 的化学式,进行了如下实验∶
的化学式,进行了如下实验∶步骤 1.称取一定量样品完全溶于稀盐酸中,配成100.00mL溶液。
步骤2.取步骤1所得溶液25.00 mL,加入足量 BaCl2溶液,充分反应,静置、过滤、洗涤、干燥,称得沉淀 2.330 g。
步骤3.另取步骤1所得溶液25.00mL,加入足量的某试剂(与酸性KMnO4溶液不反应),将 Fe3+完全还原为 Fe2+,再向其中滴加 0.1000 mol·L-1酸性 KMnO4溶液,测得 Fe2+恰好完全反应时消耗 KMnO4溶液 16.00 mL。
已知∶
 (未配平)
(未配平)通过计算确定该碱式硫酸铁的化学式
20-21高一上·江苏苏州·期末 查看更多[3]
(已下线)题型01 以物质的量为中心的计算-【好题汇编】备战2023-2024学年高一化学期末真题分类汇编(江苏专用)(已下线)专题02 化学计算中常用的几种方法-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)江苏省苏州市2020-2021学年高一上学期学业质量阳光指标调研考试化学试题
更新时间:2021-01-31 12:36:46
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】按照要求填空:
(1)在①NaCl晶体②干冰③液态醋酸④铜⑤硫酸钡固体⑥熔融KNO3⑦CuSO4·5H2O⑧稀硫酸⑨盐酸⑩酒精中,属于电解质的是___________ ,属于强电解质的是___________ ,属于非电解质的是___________ ,能导电的是___________ 。
(2)在H+、Mg2+、Fe2+、Fe3+、S2-、I-、S中,只有还原性的是___________ ,既有氧化性又有还原性的是___________ 。
(3)过氧化钠常用作供氧剂,可以与二氧化碳或水反应放出氧气,在过氧化钠中阳离子与阴离子的个数比为___________ ;它与盐酸反应的化学方程式为___________ 。
(4)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
①该反应中的还原剂是___________ 。
②写出该反应的化学方程式并用单线桥标出电子转移的方向和数目___________ 。
③如反应转移了0.3mol电子,则产生的气体在标准状况下体积为___________ 。
(5)19.6克硫酸中含有___________ 个原子,将其溶于水配成500mL溶液则溶液的物质的量浓度为___________ ,从中取出100mL可以消耗1mol/L的NaOH溶液___________ mL。
(6)物质的量相等的SO2和SO3,其质量之比为________ ,所含原子数之比为________ ,所含质子数之比为________ ,质量相等的SO2和SO3,所含氧原子数之比为___________ 。
(7)标准状况下,1.6g某气态氧化物RO2体积为0.56L,R的相对原子量为___________ 。36g 中质子数为
中质子数为___________ ,电子数为___________ (用NA表示)。
(8)CO和CO2的混合气体36g,完全燃烧后测得STP下CO2体积为22.4L,那么混合气体中CO的质量是___________ ,混合气体的平均摩尔质量为___________ ,混合气体中CO2在标准状况下的体积是___________ ,混合气体在标准状况下的密度是___________ ,该混合气体对氢气的相对密度为___________ 。
(1)在①NaCl晶体②干冰③液态醋酸④铜⑤硫酸钡固体⑥熔融KNO3⑦CuSO4·5H2O⑧稀硫酸⑨盐酸⑩酒精中,属于电解质的是
(2)在H+、Mg2+、Fe2+、Fe3+、S2-、I-、S中,只有还原性的是
(3)过氧化钠常用作供氧剂,可以与二氧化碳或水反应放出氧气,在过氧化钠中阳离子与阴离子的个数比为
(4)某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
①该反应中的还原剂是
②写出该反应的化学方程式并用单线桥标出电子转移的方向和数目
③如反应转移了0.3mol电子,则产生的气体在标准状况下体积为
(5)19.6克硫酸中含有
(6)物质的量相等的SO2和SO3,其质量之比为
(7)标准状况下,1.6g某气态氧化物RO2体积为0.56L,R的相对原子量为
 中质子数为
中质子数为(8)CO和CO2的混合气体36g,完全燃烧后测得STP下CO2体积为22.4L,那么混合气体中CO的质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】用硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]为原料通过下列流程可以制备晶体A。
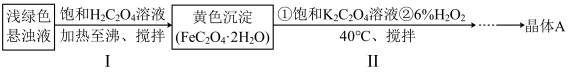
已知:25 ℃时,[Fe(C2O4)3]3-(aq)+SCN-(aq)⇌[Fe(SCN)]2+(aq)+3C2O42-(aq),K=10-16
(1)写出步骤Ⅰ生成黄色沉淀(FeC2O4·2H2O)的化学方程式:_________________ 。
(2)步骤Ⅱ水浴加热需控制40 ℃的理由是_____________________________ 。
(3)某研究小组同学欲检验晶体A中含有三价铁,取少量晶体放入试管中,用蒸馏水充分溶解,向试管中滴入几滴0.1 mol· L-1KSCN溶液。请判断上述实验方案是否可行并说明理由:______________________________________________________________________ 。
(4)某研究小组通过如下实验步骤测定晶体A的化学式:
步骤1:准确称取A样品4.910 0 g,干燥脱水至恒重,残留物质量为4.370 0 g;
步骤2:准确称取A样品4.910 0 g置于锥形瓶中,加入足量的3.000 mol·L-1 H2SO4溶液和适量蒸馏水,用0.500 0 mol·L-1 KMnO4溶液滴定,当MnO4-恰好完全被还原为Mn2+时,消耗KMnO4溶液的体积为24.00 mL;
步骤3:将步骤1所得固体溶于水,加入铁粉0.280 0 g,恰好完全反应。
通过计算确定晶体A的化学式(写出计算过程)_______ 。

已知:25 ℃时,[Fe(C2O4)3]3-(aq)+SCN-(aq)⇌[Fe(SCN)]2+(aq)+3C2O42-(aq),K=10-16
(1)写出步骤Ⅰ生成黄色沉淀(FeC2O4·2H2O)的化学方程式:
(2)步骤Ⅱ水浴加热需控制40 ℃的理由是
(3)某研究小组同学欲检验晶体A中含有三价铁,取少量晶体放入试管中,用蒸馏水充分溶解,向试管中滴入几滴0.1 mol· L-1KSCN溶液。请判断上述实验方案是否可行并说明理由:
(4)某研究小组通过如下实验步骤测定晶体A的化学式:
步骤1:准确称取A样品4.910 0 g,干燥脱水至恒重,残留物质量为4.370 0 g;
步骤2:准确称取A样品4.910 0 g置于锥形瓶中,加入足量的3.000 mol·L-1 H2SO4溶液和适量蒸馏水,用0.500 0 mol·L-1 KMnO4溶液滴定,当MnO4-恰好完全被还原为Mn2+时,消耗KMnO4溶液的体积为24.00 mL;
步骤3:将步骤1所得固体溶于水,加入铁粉0.280 0 g,恰好完全反应。
通过计算确定晶体A的化学式(写出计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】已知稀硝酸和铜能发生反应,生成硝酸铜、一氧化氮气体和水。
(1)请写出该反应的化学方程式,并用双线桥法标出反应中电子转移的方向和数目。________
(2)一次实验中,某同学用过量的稀硝酸(其密度为1.08 g·mL-1,HNO3的质量分数为12%)跟一定量的铜片反应,产生了标准状况下0.56 L的一氧化氮。试计算(简要写出计算过程):
①该稀硝酸的物质的量浓度(结果保留小数点后一位);______________
②被还原的HNO3的物质的量。________________
(1)请写出该反应的化学方程式,并用双线桥法标出反应中电子转移的方向和数目。
(2)一次实验中,某同学用过量的稀硝酸(其密度为1.08 g·mL-1,HNO3的质量分数为12%)跟一定量的铜片反应,产生了标准状况下0.56 L的一氧化氮。试计算(简要写出计算过程):
①该稀硝酸的物质的量浓度(结果保留小数点后一位);
②被还原的HNO3的物质的量。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)实验室由Al盐制备Al(OH)3最佳选择NH3·H2O,其离子反应方程式:____________________________
(2)12.4g Na2X含有0.4mol Na+, Na2X的摩尔质量为________ 。
(3)由氨气和氢气组成的混合气体的平均相对分子质量为12,则氨气和氢气的物质的量之比为_________
(4)已知 离子可与R2-离子反应,R2-被氧化为R单质,
离子可与R2-离子反应,R2-被氧化为R单质, 的还原产物中M为+3价;又已知100mL c(
的还原产物中M为+3价;又已知100mL c( )=0.2 mol·L-1的溶液可与100mL c(R2- )=0.6 mol·L-1的溶液恰好完全反应,则n值为
)=0.2 mol·L-1的溶液可与100mL c(R2- )=0.6 mol·L-1的溶液恰好完全反应,则n值为__________
A.4 B.5 C.6 D.7
(2)12.4g Na2X含有0.4mol Na+, Na2X的摩尔质量为
(3)由氨气和氢气组成的混合气体的平均相对分子质量为12,则氨气和氢气的物质的量之比为
(4)已知
 离子可与R2-离子反应,R2-被氧化为R单质,
离子可与R2-离子反应,R2-被氧化为R单质, 的还原产物中M为+3价;又已知100mL c(
的还原产物中M为+3价;又已知100mL c( )=0.2 mol·L-1的溶液可与100mL c(R2- )=0.6 mol·L-1的溶液恰好完全反应,则n值为
)=0.2 mol·L-1的溶液可与100mL c(R2- )=0.6 mol·L-1的溶液恰好完全反应,则n值为A.4 B.5 C.6 D.7
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)Cl2通入水中制氯水,反应的离子方程式:____ 。
(2)高铁酸钾(K2FeO4)被人们称为“绿色化学”净水剂。高铁酸钾在酸性至弱碱性条件下不稳定。工业上用KClO与Fe(NO3)3溶液反应制得K2FeO4,反应的离子方程式:____ 。
(3)以软锰矿(主要成分为MnO2、SiO2等)为原料制备高纯MnO2的流程如图:
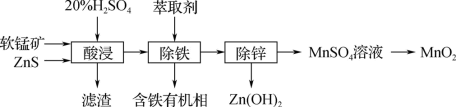
①滤渣中含大量硫单质,酸浸时主要反应的化学方程式:____ 。
②酸性条件下,用合适的氧化剂可以将MnSO4转化为高纯MnO2。用NaClO3作氧化剂时会同时产生NaCl,该反应的离子方程式:____ 。
(4)已知次氯酸可被FeSO4等物质还原。用下列实验方案测定某次试验所得溶液中次氯酸的物质的量浓度:量取10.00mL上述次氯酸溶液,并稀释至100mL,再从其中取出10.00mL于锥形瓶中,并加入10.00mL0.8000mol/L的FeSO4溶液,充分反应后,用0.05000mol/L的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液24.00mL,则原次氯酸溶液的浓度为____ (写出计算过程)。
(1)Cl2通入水中制氯水,反应的离子方程式:
(2)高铁酸钾(K2FeO4)被人们称为“绿色化学”净水剂。高铁酸钾在酸性至弱碱性条件下不稳定。工业上用KClO与Fe(NO3)3溶液反应制得K2FeO4,反应的离子方程式:
(3)以软锰矿(主要成分为MnO2、SiO2等)为原料制备高纯MnO2的流程如图:

①滤渣中含大量硫单质,酸浸时主要反应的化学方程式:
②酸性条件下,用合适的氧化剂可以将MnSO4转化为高纯MnO2。用NaClO3作氧化剂时会同时产生NaCl,该反应的离子方程式:
(4)已知次氯酸可被FeSO4等物质还原。用下列实验方案测定某次试验所得溶液中次氯酸的物质的量浓度:量取10.00mL上述次氯酸溶液,并稀释至100mL,再从其中取出10.00mL于锥形瓶中,并加入10.00mL0.8000mol/L的FeSO4溶液,充分反应后,用0.05000mol/L的酸性KMnO4溶液滴定至终点,消耗KMnO4溶液24.00mL,则原次氯酸溶液的浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】铁、铜混合粉末20.0 g加入到100 mL5.0 mol·L-1FeCl3溶液中,剩余固体质量为5.2 g(忽略反应前后溶液体积变化)。计算:还原剂失去电子的物质的量_____ ;反应后溶液中FeCl2的物质的量浓度_____ mol·L-1。
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】将NaOH和Na2CO3·nH2O组成的混合物39.6 g溶于水,配制成100 mL溶液,测得该溶液中c(Na+)=5 mol·L-1。另取相同质量的上述混合物,加入足量的盐酸完全反应后,放出的气体在标准状况下的体积为4.48 L,试计算:
(1)原混合物中NaOH的质量分数为______ (保留一位小数)。
(2)Na2CO3·nH2O中的n值为_____ 。
(1)原混合物中NaOH的质量分数为
(2)Na2CO3·nH2O中的n值为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】在标准状况下,进行甲、乙、丙三组实验,三组实验各取30mL同浓度的盐酸,加入同一种镁、铝混合物粉末,产生气体,有关数据列表如下:
(1)甲、乙两组实验中,哪一组盐酸是不足量的?_____________,理由是_____________。
(2)盐酸的物质的量浓度_____________。
(3)混合粉末中Mg的物质的量为_______________,Mg、Al的物质的量之比为__________。
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/mg | 510 | 765 | 1020 |
| 气体体积/mL | 560 | 672 | 672 |
(1)甲、乙两组实验中,哪一组盐酸是不足量的?_____________,理由是_____________。
(2)盐酸的物质的量浓度_____________。
(3)混合粉末中Mg的物质的量为_______________,Mg、Al的物质的量之比为__________。
您最近一年使用:0次



