将NaOH和Na2CO3·nH2O组成的混合物39.6 g溶于水,配制成100 mL溶液,测得该溶液中c(Na+)=5 mol·L-1。另取相同质量的上述混合物,加入足量的盐酸完全反应后,放出的气体在标准状况下的体积为4.48 L,试计算:
(1)原混合物中NaOH的质量分数为______ (保留一位小数)。
(2)Na2CO3·nH2O中的n值为_____ 。
(1)原混合物中NaOH的质量分数为
(2)Na2CO3·nH2O中的n值为
更新时间:2018-12-14 19:16:17
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】填空。
(1)标准状况下,1.92g某气体的体积为672mL,则此气体的相对分子质量为_______ 。
(2)已知标准状况下,气体A的密度为1.964g·L-1,则气体A的摩尔质量为_______ 。
(3)在一定条件下,mgNH4HCO3完全分解生成NH3、CO2、H2O(g),按要求填空:
①若所得混合气体对H2的相对密度为d,则混合气体的物质的量为_______ 。
②若在该条件下,所得NH3、CO2、H2O(g)的体积分数分别为a%、b%、c%,则混合气体的平均相对分子质量为_______ (用含a、b、c的代数式表示)。
(4)标准状况下,将560L氨气溶于水形成 氨水,其密度是
氨水,其密度是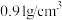 ,则此氨水的物质的量浓度为
,则此氨水的物质的量浓度为_______  。(保留两位有效数字)
。(保留两位有效数字)
(5)下列物质中:①NaOH溶液 ②铝 ③液态氯化氢 ④碱石灰 ⑤二氧化硫 ⑥氨气 ⑦氢氧化铝 ⑧碳酸氢钠 ⑨甲烷。属于强电解质的是_______ ﹔能导电的是_______ 。(填序号)
(1)标准状况下,1.92g某气体的体积为672mL,则此气体的相对分子质量为
(2)已知标准状况下,气体A的密度为1.964g·L-1,则气体A的摩尔质量为
(3)在一定条件下,mgNH4HCO3完全分解生成NH3、CO2、H2O(g),按要求填空:
①若所得混合气体对H2的相对密度为d,则混合气体的物质的量为
②若在该条件下,所得NH3、CO2、H2O(g)的体积分数分别为a%、b%、c%,则混合气体的平均相对分子质量为
(4)标准状况下,将560L氨气溶于水形成
 氨水,其密度是
氨水,其密度是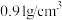 ,则此氨水的物质的量浓度为
,则此氨水的物质的量浓度为 。(保留两位有效数字)
。(保留两位有效数字)(5)下列物质中:①NaOH溶液 ②铝 ③液态氯化氢 ④碱石灰 ⑤二氧化硫 ⑥氨气 ⑦氢氧化铝 ⑧碳酸氢钠 ⑨甲烷。属于强电解质的是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】根据所学知识,填写下列空白
(1)0.3 mol NH3分子中所含原子数与________ 个 H2O分子中所含原子数相等。
(2)已知17 gH2R中含1molH,则R的摩尔质量为__________ 。
(3)含有相同氧原子数的SO2和SO3,其分子的质量比为__________ 。
(4)标准状况下,a L HCl气体溶于水配制成b L溶液。其物质的量浓度为______ mol/L。
(5)实验室用Na2CO3·10H2O晶体配制0.5 mol/L 的Na2CO3溶液970 mL,用托盘天平应称取Na2CO3·10H2O的质量是______ 。
(6)标况下,体积为8.96 L的CO和CO2的混合气体的质量为14.4 g,则CO的质量为____ g,CO2的体积为_______ L,混合气体中碳、氧两种原子的个数比为_______ ,混合气体的平均摩尔质量为________ g/mol。
(1)0.3 mol NH3分子中所含原子数与
(2)已知17 gH2R中含1molH,则R的摩尔质量为
(3)含有相同氧原子数的SO2和SO3,其分子的质量比为
(4)标准状况下,a L HCl气体溶于水配制成b L溶液。其物质的量浓度为
(5)实验室用Na2CO3·10H2O晶体配制0.5 mol/L 的Na2CO3溶液970 mL,用托盘天平应称取Na2CO3·10H2O的质量是
(6)标况下,体积为8.96 L的CO和CO2的混合气体的质量为14.4 g,则CO的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)今有五种物质:①铜线 ②熔化的NaCl ③NaCl晶体 ④氨气 ⑤液态氯化氢,其中能导电的物质是__ ;属于电解质的是___ ;属于非电解质的是___ 。
(2)0.5molH2SO4的质量是__ g,能中和___ molNaOH,该硫酸所含氢元素的质量与___ molNH3中所含氢元素的质量相同。
(3)相同质量的CH4和H2S中分子个数比为___ 。
(4)在KCl、MgCl2、Mg(NO3)2形成的混合溶液中,n(K+)=0.2mol,n(Mg2+)=0.15mol,n(Cl-)=0.2mol,则n(NO3-)为( )
A.0.05mol B.0.20mol C.0.30mol D.0.40mol
(2)0.5molH2SO4的质量是
(3)相同质量的CH4和H2S中分子个数比为
(4)在KCl、MgCl2、Mg(NO3)2形成的混合溶液中,n(K+)=0.2mol,n(Mg2+)=0.15mol,n(Cl-)=0.2mol,则n(NO3-)为
A.0.05mol B.0.20mol C.0.30mol D.0.40mol
您最近一年使用:0次
【推荐1】元素周期表中大多数元素是金属元素,金属及其化合物在生活生产中有着重要应用,根据试题信息,完成下列计算:
(1)某常见二价金属12.6g与足量稀硫酸反应,生成氢气5.04L(S.T.P),该元素原子的摩尔质量为__ g/mol.
(2)39.32g某金属混合物,由12.32g镁和0.25mol另一种比镁不活泼的金属元素A组成,该混合物与一定量盐酸反应,产生氢气4.928L(S.T.P),则参加反应的HCl为__ mol,金属A的相对原子质量为__ .
(3)由NaCl、NaHCO3、Na2CO3•10H2O组成的混合物157.8g,充分加热后,产生的气体(气体温度150℃)依次通过无水CaCl2和碱石灰,两种吸收剂分别增重59.4g和13.2g,则混合物中NaHCO3的质量分数为___ ,若等质量的该混合物与足量盐酸反应,产生二氧化碳(S.T.P)__ L.
(1)某常见二价金属12.6g与足量稀硫酸反应,生成氢气5.04L(S.T.P),该元素原子的摩尔质量为
(2)39.32g某金属混合物,由12.32g镁和0.25mol另一种比镁不活泼的金属元素A组成,该混合物与一定量盐酸反应,产生氢气4.928L(S.T.P),则参加反应的HCl为
(3)由NaCl、NaHCO3、Na2CO3•10H2O组成的混合物157.8g,充分加热后,产生的气体(气体温度150℃)依次通过无水CaCl2和碱石灰,两种吸收剂分别增重59.4g和13.2g,则混合物中NaHCO3的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】取50.0mL Na2CO3和Na2SO4的混合溶液,加入过量BaCl2溶液后,得到沉淀14.51g,将沉淀用过量稀HNO3处理后,沉淀质量减少到4.66g,并有气体放出,试计算:
(1)原溶液中Na2SO4的物质的量为______________ ;
(2)生成气体的体积(标准状况)为_________________ 。
(1)原溶液中Na2SO4的物质的量为
(2)生成气体的体积(标准状况)为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】合成氨工业生产中所用的αFe催化剂的主要成为FeO、Fe2O3。
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比4∶5,其中Fe2+与Fe3+物质的量之比为_____ 。
(2)当催化剂中Fe2+与Fe3+的物质的量之比为1∶2时,其催化剂活性最高,此时混合物中铁的质量分数为______ (保留2位小数)。
(3)写出由C(炭粉)与Fe2O3在高温下反应制备α铁触媒的化学方程式(另一种产物可溶于水)_____ 。
(4)为制得这种活性最高的催化剂,理论上应向480 g Fe2O3粉末加入炭粉的质量为_____ ,生成实验条件下CO2的体积为_____ (假设此实验条件下,气体摩尔体积为24 L·mol-1)。
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比4∶5,其中Fe2+与Fe3+物质的量之比为
(2)当催化剂中Fe2+与Fe3+的物质的量之比为1∶2时,其催化剂活性最高,此时混合物中铁的质量分数为
(3)写出由C(炭粉)与Fe2O3在高温下反应制备α铁触媒的化学方程式(另一种产物可溶于水)
(4)为制得这种活性最高的催化剂,理论上应向480 g Fe2O3粉末加入炭粉的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】(1)标准状况下,甲烷和一氧化碳的混合气体共8.96L,其质量为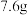 ,则混合气体中甲烷的体积分数为
,则混合气体中甲烷的体积分数为______ 。
(2)某物质 加热时按化学方程式
加热时按化学方程式 分解,产物均为气体,测得由生成物组成的混合物气体对
分解,产物均为气体,测得由生成物组成的混合物气体对 的相对密度为20,则反应物
的相对密度为20,则反应物 的摩尔质量为
的摩尔质量为______ 。
(3)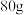 密度为
密度为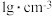 的
的 溶液里含
溶液里含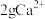 ,从中取出一半的溶液,其中
,从中取出一半的溶液,其中 的物质的量浓度是
的物质的量浓度是______ 。
(4)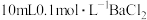 溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的
溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的 完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是
完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是______ 。
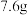 ,则混合气体中甲烷的体积分数为
,则混合气体中甲烷的体积分数为(2)某物质
 加热时按化学方程式
加热时按化学方程式 分解,产物均为气体,测得由生成物组成的混合物气体对
分解,产物均为气体,测得由生成物组成的混合物气体对 的相对密度为20,则反应物
的相对密度为20,则反应物 的摩尔质量为
的摩尔质量为(3)
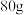 密度为
密度为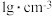 的
的 溶液里含
溶液里含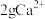 ,从中取出一半的溶液,其中
,从中取出一半的溶液,其中 的物质的量浓度是
的物质的量浓度是(4)
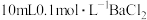 溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的
溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的 完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是
完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】质量为10g的镁铝合金,与200mL 0.5mol•L﹣1的氢氧化钠溶液恰好完全反应.已知铝与氢氧化钠溶液反应的化学方程式为:2Al+2NaOH+6H2O═2Na[Al(OH)4]+3H2↑求:
(1)合金中铝的质量分数
(2)生成气体在标准状况下的体积.
(1)合金中铝的质量分数
(2)生成气体在标准状况下的体积.
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度(可供选用的反应物只有CaCO3固体、6 mol·L-1盐酸、6 mol·L-1硫酸和蒸馏水)。
回答下列问题:
(1)装置A中液体试剂选用________________ 。
(2)装置B的作用是_________ 。装置E中碱石灰的作用是________ 。
(3)装置D中发生反应的化学方程式是__________ 。
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为_____ 。

回答下列问题:
(1)装置A中液体试剂选用
(2)装置B的作用是
(3)装置D中发生反应的化学方程式是
(4)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为
您最近一年使用:0次



