(1)标准状况下,甲烷和一氧化碳的混合气体共8.96L,其质量为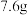 ,则混合气体中甲烷的体积分数为
,则混合气体中甲烷的体积分数为______ 。
(2)某物质 加热时按化学方程式
加热时按化学方程式 分解,产物均为气体,测得由生成物组成的混合物气体对
分解,产物均为气体,测得由生成物组成的混合物气体对 的相对密度为20,则反应物
的相对密度为20,则反应物 的摩尔质量为
的摩尔质量为______ 。
(3)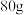 密度为
密度为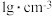 的
的 溶液里含
溶液里含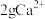 ,从中取出一半的溶液,其中
,从中取出一半的溶液,其中 的物质的量浓度是
的物质的量浓度是______ 。
(4)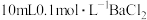 溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的
溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的 完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是
完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是______ 。
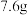 ,则混合气体中甲烷的体积分数为
,则混合气体中甲烷的体积分数为(2)某物质
 加热时按化学方程式
加热时按化学方程式 分解,产物均为气体,测得由生成物组成的混合物气体对
分解,产物均为气体,测得由生成物组成的混合物气体对 的相对密度为20,则反应物
的相对密度为20,则反应物 的摩尔质量为
的摩尔质量为(3)
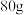 密度为
密度为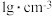 的
的 溶液里含
溶液里含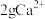 ,从中取出一半的溶液,其中
,从中取出一半的溶液,其中 的物质的量浓度是
的物质的量浓度是(4)
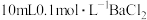 溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的
溶液分别恰好使相同体积的硫酸铁、硫酸铜两种溶液中的 完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是
完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是
更新时间:2020-09-08 06:48:18
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中后有0.58 g 白色沉淀,在所得浊液中,逐滴加入0.5mol/L的盐酸,加入盐酸的体积与生成沉淀的质量关系如图所示:

(1)混合物中NaOH的物质的量为__ 。
(2)混合物中AlCl3质量为__ 。
(3)混合物中MgCl2质量为__ 。
(4)P点表示盐酸的体积是__ 。

(1)混合物中NaOH的物质的量为
(2)混合物中AlCl3质量为
(3)混合物中MgCl2质量为
(4)P点表示盐酸的体积是
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)某同学查得Ba(OH)2·8H2O晶体在20℃时的溶解度为3.9 g/100g水,则20℃时,Ba(OH)2饱和溶液的质量分数为__________ (答案保留2位小数) 。
(2)过氧化钡(BaO2)是一种常用的氧化剂。工业上制取过氧化钡的方法之一是2BaO+O2 2BaO2。现有16.0吨的氧化钡在足量的氧气中加热反应后,固体的质量变为17.6吨。那么实际参加反应的氧化钡的质量为
2BaO2。现有16.0吨的氧化钡在足量的氧气中加热反应后,固体的质量变为17.6吨。那么实际参加反应的氧化钡的质量为______________ 吨。
(3)取不同质量由Ba(OH)2·nH2O和BaCO3组成的样品,加水溶解后加入80 mL 1.0 mol/L的盐酸,并不断地搅拌,所得CO2气体的体积(已换算为标准状况)与加入样品的质量关系通过描点得到下图(在此过程中不考虑Ba(HCO3)2的生成和CO2的溶解)。
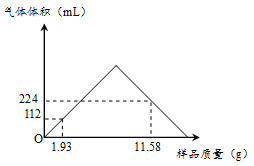
请计算:
①在11.58 g样品中BaCO3的质量为______ g?(写出计算过程)
②化学式Ba(OH)2·nH2O中n的值为_______ ?(写出计算过程)
(2)过氧化钡(BaO2)是一种常用的氧化剂。工业上制取过氧化钡的方法之一是2BaO+O2
 2BaO2。现有16.0吨的氧化钡在足量的氧气中加热反应后,固体的质量变为17.6吨。那么实际参加反应的氧化钡的质量为
2BaO2。现有16.0吨的氧化钡在足量的氧气中加热反应后,固体的质量变为17.6吨。那么实际参加反应的氧化钡的质量为(3)取不同质量由Ba(OH)2·nH2O和BaCO3组成的样品,加水溶解后加入80 mL 1.0 mol/L的盐酸,并不断地搅拌,所得CO2气体的体积(已换算为标准状况)与加入样品的质量关系通过描点得到下图(在此过程中不考虑Ba(HCO3)2的生成和CO2的溶解)。

请计算:
①在11.58 g样品中BaCO3的质量为
②化学式Ba(OH)2·nH2O中n的值为
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】有碳酸钠、碳酸氢钠的混合物19.0g,把它们加热到质量不再减轻,冷却后称量为15.9g。求:
(1)原混合物中碳酸钠的质量分数___________ 。
(2)将原混合物19.0g完全溶解于蒸馏水水中,配成500mL溶液,则其中钠离子物质的量浓度为___________ 。
(1)原混合物中碳酸钠的质量分数
(2)将原混合物19.0g完全溶解于蒸馏水水中,配成500mL溶液,则其中钠离子物质的量浓度为
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】加碘食盐是含KIO3的食盐,其中KIO3可由反应KI+3Cl2+3H2O=KIO3+6HCl制取。市面上销售的加碘食盐中的碘元素含量为20~50mg/kg。请计算:制取1000kg含碘元素25.4mg/kg的加碘食盐,需要消耗Cl2的体积是多少___ ?(标准状况)
您最近半年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】有硫酸,硫酸亚铁、硫酸铁的混合溶液 ,已知溶液中各阳离子的物质的量浓度相等,
,已知溶液中各阳离子的物质的量浓度相等, 的物质的量浓度为
的物质的量浓度为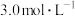 。
。
请计算:
(1)硫酸的物质的量浓度为________  。
。
(2)理论上此溶液最多可溶解铁粉的质量为________ g。
 ,已知溶液中各阳离子的物质的量浓度相等,
,已知溶液中各阳离子的物质的量浓度相等, 的物质的量浓度为
的物质的量浓度为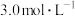 。
。请计算:
(1)硫酸的物质的量浓度为
 。
。(2)理论上此溶液最多可溶解铁粉的质量为
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐2】将200mLH2SO4 和Fe2(SO4)3的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少4.48g;向另一份中加入足量BaCl2溶液,经过滤、洗涤、干 燥、称量,得到46.6g 白色沉淀。请计算:
(1)原溶液中c(SO42-)=______ ;
(2)原溶液中H2SO4和Fe2(SO4)3的物质的量浓度之比为______ 。
(1)原溶液中c(SO42-)=
(2)原溶液中H2SO4和Fe2(SO4)3的物质的量浓度之比为
您最近半年使用:0次



