将200mLH2SO4 和Fe2(SO4)3的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少4.48g;向另一份中加入足量BaCl2溶液,经过滤、洗涤、干 燥、称量,得到46.6g 白色沉淀。请计算:
(1)原溶液中c(SO42-)=______ ;
(2)原溶液中H2SO4和Fe2(SO4)3的物质的量浓度之比为______ 。
(1)原溶液中c(SO42-)=
(2)原溶液中H2SO4和Fe2(SO4)3的物质的量浓度之比为
更新时间:2019-08-10 09:30:28
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】烟气中NOx是NO和NO2的混合物(不含N2O4)。
(1)根据废气排放标准,1 m3烟气最高允许含400 mg NOx。若NOx中NO质量分数为0.85,则l m3烟气中最高允许含NO______ L(标准状况,保留2位小数)。
(2)若用氨气除去废气中的氮氧化物(NOx):NOx+NH3→N2+H2O(l)。假如每升废气中含NOx 0.0672 L(只含NO和NO2),向100.000 L废气中通入10.000 L氨气可使NOx完全转化,测得反应后气体体积变为103.952 L(气体体积均折算到标准状况)。
①NOx 中的 x 值为_________ (保留1位小数)。
②除去废气中的NOx,至少需氨________ mol(保留2位小数)。
(3)工业上通常用溶质质量分数为0.150的Na2CO3水溶液(密度l.16g/mL)作为NOx吸收剂,该碳酸钠溶液物质的量浓度为_______ mol/L(保留2位小数)。
(4)已知:NO+NO2+Na2CO3 → 2NaNO2+CO2 ①
2NO2+Na2CO3 → NaNO2+NaNO3+CO2 ②
1 m3含2000 mg NOx的烟气用质量分数为0.150的碳酸钠溶液吸收。若吸收率为80%,吸收后的烟气排放标准_______ (填“符合”或“不符合”),理由:______________________________________ 。
(5)加入硝酸可改变烟气中NO和NO2的比,反应为:NO+2HNO3 → 3NO2+H2O
当烟气中n(NO)∶n(NO2)=2∶3时,吸收率最高。1 m3烟气含2000 mg NOx,其中n(NO) ∶n(NO2)=9∶1。
计算:
①为了达到最高吸收率,1 m3烟气需用硝酸的物质的量______________ (保留3位小数)。
②1 m3烟气达到最高吸收率90%时,吸收后生成NaNO2的质量______________ (假设上述吸收反应中,反应①比反应②迅速。计算结果保留1位小数)。
(1)根据废气排放标准,1 m3烟气最高允许含400 mg NOx。若NOx中NO质量分数为0.85,则l m3烟气中最高允许含NO
(2)若用氨气除去废气中的氮氧化物(NOx):NOx+NH3→N2+H2O(l)。假如每升废气中含NOx 0.0672 L(只含NO和NO2),向100.000 L废气中通入10.000 L氨气可使NOx完全转化,测得反应后气体体积变为103.952 L(气体体积均折算到标准状况)。
①NOx 中的 x 值为
②除去废气中的NOx,至少需氨
(3)工业上通常用溶质质量分数为0.150的Na2CO3水溶液(密度l.16g/mL)作为NOx吸收剂,该碳酸钠溶液物质的量浓度为
(4)已知:NO+NO2+Na2CO3 → 2NaNO2+CO2 ①
2NO2+Na2CO3 → NaNO2+NaNO3+CO2 ②
1 m3含2000 mg NOx的烟气用质量分数为0.150的碳酸钠溶液吸收。若吸收率为80%,吸收后的烟气排放标准
(5)加入硝酸可改变烟气中NO和NO2的比,反应为:NO+2HNO3 → 3NO2+H2O
当烟气中n(NO)∶n(NO2)=2∶3时,吸收率最高。1 m3烟气含2000 mg NOx,其中n(NO) ∶n(NO2)=9∶1。
计算:
①为了达到最高吸收率,1 m3烟气需用硝酸的物质的量
②1 m3烟气达到最高吸收率90%时,吸收后生成NaNO2的质量
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)从500 mL 0.2 mol/L Na2SO4 溶液中取出10 mL,取出的Na2SO4溶液物质的量浓度为________ mol/L;若将这10 mL溶液用水稀释到100 mL,所得溶液中Na+的物质的量浓度为______ mol/L。
(2)标准状况下,2.4g某气体的体积为672 mL,则此气体的相对分子质量为________ 。
(3)在标准状况下,V L HCl溶于1 L水中,所得溶液的密度为ρg·cm-3,则此溶液的物质的量浓度为:______________ mol/L
(2)标准状况下,2.4g某气体的体积为672 mL,则此气体的相对分子质量为
(3)在标准状况下,V L HCl溶于1 L水中,所得溶液的密度为ρg·cm-3,则此溶液的物质的量浓度为:
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】阿伏加 德罗常数的近似值为6.02×1023.按要求完成下列填空:
(1)1mol Cl2中约含有______ 个氯气分子,约含有______ 个氯原子,含有6.02×1023个氢原子的H2SO4的物质的量是______ ;
(2)标准状况下11.2L N2O4和______ mol NO所含有的原子数相等。
(3)某硫酸钠溶液中含有3.01×1023个Na+,则该溶液中SO42-的物质的量是______ 。
(4)2L 1mol/L MgCl2中镁离子的物质的量为______ ,Cl-的物质的量浓度为______ 。
(1)1mol Cl2中约含有
(2)标准状况下11.2L N2O4和
(3)某硫酸钠溶液中含有3.01×1023个Na+,则该溶液中SO42-的物质的量是
(4)2L 1mol/L MgCl2中镁离子的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】由碳酸铵 和硝酸铵
和硝酸铵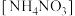 组成的均匀固体混合物13.6g,将其分成等质量的两份进行下列实验:
组成的均匀固体混合物13.6g,将其分成等质量的两份进行下列实验:
①第一份溶于水配成100mL溶液,再加入足量的 溶液,充分反应后过滤,沉淀经洗涤干燥后称得质量为5.0g
溶液,充分反应后过滤,沉淀经洗涤干燥后称得质量为5.0g
②第二份与足量浓NaOH溶液混合后加热,完全反应后生成标准状况下的气体2.8L
根据上述数据计算:
(1)每份固体中含碳酸铵的物质的量为________ mol。
(2)第一份所配溶液中硝酸铵的物质的量浓度为________  。
。
(3)原固体混合物中含氮元素的质量分数为________ 。(计算结果保留三位有效数字)
 和硝酸铵
和硝酸铵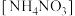 组成的均匀固体混合物13.6g,将其分成等质量的两份进行下列实验:
组成的均匀固体混合物13.6g,将其分成等质量的两份进行下列实验:①第一份溶于水配成100mL溶液,再加入足量的
 溶液,充分反应后过滤,沉淀经洗涤干燥后称得质量为5.0g
溶液,充分反应后过滤,沉淀经洗涤干燥后称得质量为5.0g②第二份与足量浓NaOH溶液混合后加热,完全反应后生成标准状况下的气体2.8L
根据上述数据计算:
(1)每份固体中含碳酸铵的物质的量为
(2)第一份所配溶液中硝酸铵的物质的量浓度为
 。
。(3)原固体混合物中含氮元素的质量分数为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】有一瓶澄清的溶液,其中可能含有H+、NH4+、Na+、Al3+、Fe3+、HCO3-、SO42-、I-,取该溶液进行以下实验:
①用pH试纸检验,溶液显强酸性;
②该溶液的焰色反应没有黄色;
③取溶液适量加入少量CCl4和数滴新制氯水振荡,CCl4层呈紫红色;
④当向该溶液中加入某浓度的NaOH溶液时,生成沉淀的物质的量变化如图
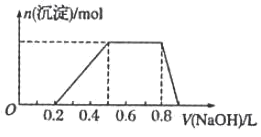
(1)该溶液中肯定含有的离子是_________ ,已确定阳离子的物质的量之比为_________
(2)肯定不含的离子是____________
(3)不能确定的离子是___________ ,如何证明该离子是否存在? __________________
(4)请写出第④步中沉淀溶解的离子方程式________________________
①用pH试纸检验,溶液显强酸性;
②该溶液的焰色反应没有黄色;
③取溶液适量加入少量CCl4和数滴新制氯水振荡,CCl4层呈紫红色;
④当向该溶液中加入某浓度的NaOH溶液时,生成沉淀的物质的量变化如图

(1)该溶液中肯定含有的离子是
(2)肯定不含的离子是
(3)不能确定的离子是
(4)请写出第④步中沉淀溶解的离子方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)写出NaHSO4在水中的电离方程式________ 。
(2)粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,要除去这些杂质,可选用以下试剂:①Na2CO3、②NaOH、③BaCl2、④HCl ,则试剂加入的先后顺序是__________ (填序号)。
(3)2KMnO4+16HCl(浓) =2KCl+2MnCl2+5Cl2↑+8H2O,用双线桥法标出该反应电子转移的方向和数目_______ ;若有0.1mol电子转移时生成Cl2的体积为__________ (标准状况),被氧化的HCl的物质的量为______________ 。
(4)某无色透明溶液可能含有K+、Cu2+、Ca2+、SO42-、CO32-、Cl﹣中的几种,现进行如下实验:
①滴加BaCl2溶液,有白色沉淀产生,将沉淀滤出。
②向上述沉淀中加入足量的稀硝酸,有部分沉淀溶解。
③向滤液加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀HNO3。
试判断:该溶液中肯定有__________ ,肯定没有_________ ,可能有_________ (填离子符号)。
(2)粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,要除去这些杂质,可选用以下试剂:①Na2CO3、②NaOH、③BaCl2、④HCl ,则试剂加入的先后顺序是
(3)2KMnO4+16HCl(浓) =2KCl+2MnCl2+5Cl2↑+8H2O,用双线桥法标出该反应电子转移的方向和数目
(4)某无色透明溶液可能含有K+、Cu2+、Ca2+、SO42-、CO32-、Cl﹣中的几种,现进行如下实验:
①滴加BaCl2溶液,有白色沉淀产生,将沉淀滤出。
②向上述沉淀中加入足量的稀硝酸,有部分沉淀溶解。
③向滤液加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀HNO3。
试判断:该溶液中肯定有
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】在标准状况下进行甲、乙、丙三组实验。三组实验各取同浓度的盐酸30mL,加入同一种镁铝合金粉末,产生气体。有关数据列表如表(气体体积均为标准状况下测得):
(1)甲组实验中,盐酸_____ ;乙组实验中,盐酸_____ (填“过量“、“适量“或“不足“)。
(2)该盐酸的物质的量浓度_____ 。
(3)合金中Mg、Al的物质的量之比为____ 。
(4)在丙组实验后,向容器中加入1mol/L的NaOH溶液,恰好使合金中的铝元素全部转化为 ,并使Mg2+刚好沉淀完全,则溶液中
,并使Mg2+刚好沉淀完全,则溶液中 的物质的量为
的物质的量为_____ mol;溶液中Na+的物质的量为______ mol。
| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量/g | 0.255 | 0.385 | 0.459 |
| 生成气体/ml | 280 | 336 | 336 |
(1)甲组实验中,盐酸
(2)该盐酸的物质的量浓度
(3)合金中Mg、Al的物质的量之比为
(4)在丙组实验后,向容器中加入1mol/L的NaOH溶液,恰好使合金中的铝元素全部转化为
 ,并使Mg2+刚好沉淀完全,则溶液中
,并使Mg2+刚好沉淀完全,则溶液中 的物质的量为
的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】我市某企业对高砷高锡铅阳极泥进行脱砷处理,分离出锡铅废渣的同时制备了砷酸钠晶体(Na3AsO4•12H2O)。其工艺流程如图:

已知:砷在高砷高锡铅阳极泥中以单质形式存在。
若m1kg的阳极泥(砷百分含量为ω)经过上述工艺流程最后制得m2kgNa3AsO4•12H2O晶体,则砷酸钠晶体的产率为__ %。(用含有m1、m2的式子表示,砷的摩尔质量为75g/mol)

已知:砷在高砷高锡铅阳极泥中以单质形式存在。
若m1kg的阳极泥(砷百分含量为ω)经过上述工艺流程最后制得m2kgNa3AsO4•12H2O晶体,则砷酸钠晶体的产率为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】钾是活泼的碱金属,钾和氧有氧化钾(K2O)、过氧化钾(K2O2)和超氧化钾(KO2)等多种化合物.
(1)钾和硝酸钾反应可制得氧化钾K+KNO3→K2O+N2(未配平),每生成18.8gK2O消耗的还原剂有______ g
(2)超氧化钾和过氧化钾都能与二氧化碳反应均生成氧气和K2CO3,在医院、矿井、潜水、高空飞行中用作供氧剂.请尝试写出超氧化钾与二氧化碳反应的化学方程式___________________________________________ ,为了维持封闭环境气压稳定,可以使用超氧化钾和过氧化钾的混合物使吸收的CO2与生成的O2体积相同(同温同压),则它们的物质的量之比为__________ 。
(3)KO2加热至600℃部分分解得到固态混合物A。18.9g A充分吸收二氧化碳生成碳酸钾并产生氧气3.36L(标准状况),如果产物A只含有两种化合物,写出所有可能组成的化学式组合,并计算A中两种化合物的物质的量之比:___________________________ 。
(1)钾和硝酸钾反应可制得氧化钾K+KNO3→K2O+N2(未配平),每生成18.8gK2O消耗的还原剂有
(2)超氧化钾和过氧化钾都能与二氧化碳反应均生成氧气和K2CO3,在医院、矿井、潜水、高空飞行中用作供氧剂.请尝试写出超氧化钾与二氧化碳反应的化学方程式
(3)KO2加热至600℃部分分解得到固态混合物A。18.9g A充分吸收二氧化碳生成碳酸钾并产生氧气3.36L(标准状况),如果产物A只含有两种化合物,写出所有可能组成的化学式组合,并计算A中两种化合物的物质的量之比:
您最近一年使用:0次



