浙江省诸暨市2017-2018学年高三上学期期末考试化学试题
浙江
高三
期末
2021-12-09
355次
整体难度:
容易
考查范围:
认识化学科学、化学实验基础、化学反应原理、化学与STSE、常见无机物及其应用、有机化学基础、物质结构与性质
浙江省诸暨市2017-2018学年高三上学期期末考试化学试题
浙江
高三
期末
2021-12-09
355次
整体难度:
容易
考查范围:
认识化学科学、化学实验基础、化学反应原理、化学与STSE、常见无机物及其应用、有机化学基础、物质结构与性质
一、单选题 添加题型下试题
单选题
|
较易(0.85)
解题方法
1. 下列物质属于碱的是
| A.纯碱 | B.Cu2(OH)2CO3 | C.Mg(OH)2 | D.CH3CH2OH |
【知识点】 酸、碱、盐、氧化物的概念及其相互联系解读
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
您最近一年使用:0次
单选题
|
容易(0.94)
解题方法
您最近一年使用:0次
单选题
|
容易(0.94)
6. 下列说法正确的是
| A.二氧化硅是太阳能电池的常用材料 |
| B.氯化铁、硫酸铁都可用于净水 |
| C.碳酸钡是医院常用的钡餐 |
| D.氧化镁、金刚石熔点很高,都是优质的耐高温材料 |
您最近一年使用:0次
单选题
|
容易(0.94)
7. 下图是某反应在密闭容器中反应前后的示意图,“●”和“○”分别表示不同的原子。对此反应的描述一定不正确的是


| A.属于化合反应 | B.属于氧化还原反应 |
| C.属于置换反应 | D.一部分反应物未完全反应完 |
【知识点】 四种基本反应类型解读 氧化还原反应基本概念
您最近一年使用:0次
单选题
|
容易(0.94)
8. 下列化学用语中,正确的是
| A.乙醛的官能团:―COH | B.MgBr2的电子式: |
C.四氯化碳的比例模型: | D.Clˉ的结构示意图: |
您最近一年使用:0次
单选题
|
较易(0.85)
10. 下列说法中不正确的是
| A.利用焰色反应可鉴别KNO3溶液和NaCl溶液 |
| B.可用灼热的氧化铜除去二氧化碳中少量的氧气 |
| C.某澄清溶液中加入足量的稀盐酸,产生白色沉淀,则原溶液中不一定含有Ag+ |
| D.某溶液能使淀粉碘化钾试纸变蓝色,则原溶液中不一定含有I2 |
您最近一年使用:0次
11. 下列说法不正确 的是
| A.分子式符合通式CnH2n+2的两种烃,不一定互为同系物 |
| B.CH3CH2C(CH3)3的名称是2,2-二甲基丁烷 |
| C.S4、S6、S8互为同素异形体,一定条件下相互转化时属于化学变化 |
| D.丙烷与氯气反应,可得到沸点不同的3种二氯代物 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
12. 下列离子方程式正确的是
A.硫酸铜溶液中加入氢氧化钡溶液:Ba2++ =BaSO4↓ =BaSO4↓ |
B.水玻璃中通入过量CO2:SiO +H2O+CO2= +H2O+CO2= +H2SiO3↓ +H2SiO3↓ |
C.硫酸铁溶液中通入SO2气体:2Fe3++SO2+2H2O=2Fe2++ +4H+ +4H+ |
D.向澄清石灰水中加入过量的NaHCO3溶液,出现白色沉淀 +Ca2++OH—=CaCO3↓+H2O +Ca2++OH—=CaCO3↓+H2O |
您最近一年使用:0次
单选题
|
适中(0.65)
13. 如图为元素周期表的一部分,W元素原子最外层电子数与K层电子数之和为核电荷数的一半。下列说法不正确的是
| X | Y | ||
| T | W | Q |
| A.原子半径大小关系为:T>X>Y |
| B.Q元素的氧化物的水化物的酸性比W强 |
| C.T和W的常见氧化物含有相同类型的化学键 |
| D.W、Q的单质或氧化物,溶于水后所得溶液可能具有漂白性 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
14. 下列说法不正确的是
| A.相等质量的乙烯和乙醇完全燃烧,耗氧量相同 |
| B.苯不可以使酸性KMnO4溶液褪色而甲苯可以 |
| C.新制氢氧化铜在一定条件下能与乙醛、乙酸等反应 |
| D.乙醇、乙酸均能与Na反应放出H2,但二者的官能团不同 |
您最近一年使用:0次
单选题
|
适中(0.65)
15. 下列说法不正确的是
| A.石油裂解的目的是获得更多的乙烯、丙烯等原料 |
| B.聚乙烯、棉布、羊毛充分燃烧的产物都只有二氧化碳和水 |
| C.含淀粉或纤维素的物质可以制造酒精 |
| D.往含蔗糖水解酶的蔗糖反应液中加入银氨溶液,水浴加热后无银镜产生,说明蔗糖未水解 |
您最近一年使用:0次
二、多选题 添加题型下试题
16. 在2L恒容密闭容器中,发生反应:2SO2(g)+O2(g) 2SO3(g)△H=—198kJ/mol。起始通入SO2和O2各2mol,5min后达到平衡,测得SO3(g)的体积分数为
2SO3(g)△H=—198kJ/mol。起始通入SO2和O2各2mol,5min后达到平衡,测得SO3(g)的体积分数为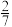 ,下列说法错误的是
,下列说法错误的是
 2SO3(g)△H=—198kJ/mol。起始通入SO2和O2各2mol,5min后达到平衡,测得SO3(g)的体积分数为
2SO3(g)△H=—198kJ/mol。起始通入SO2和O2各2mol,5min后达到平衡,测得SO3(g)的体积分数为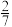 ,下列说法错误的是
,下列说法错误的是| A.达到平衡后,升高温度,则正逆反应速率均增大 |
| B.平衡时,SO2和O2的转化率之比为1:1 |
| C.达到平衡时,反应放出的热量为98kJ |
| D.单位时间内氧气与SO3消耗的物质的量之比为1:2时,达到化学平衡 |
您最近一年使用:0次
三、单选题 添加题型下试题
单选题
|
适中(0.65)
解题方法
17. 新研制的锌一空气电池适宜用作城市电动车的动力电源,其原理如图。该电池放电时Zn转化为ZnO。下列说法不正确的是


| A.Zn电极是该电池的负极 | B.Zn电极的电极反应:Zn+H2O—2e—=ZnO+2H+ |
| C.电池反应为:2Zn+O2=2ZnO | D.溶液中OH—向锌电极移动 |
您最近一年使用:0次
2021-11-05更新
|
116次组卷
|
3卷引用:浙江省诸暨市2017-2018学年高三上学期期末考试化学试题
单选题
|
适中(0.65)
解题方法
18. 下列有关说法正确的是
| A.水溶液中c(OH-)>c(H+),溶液一定显碱性 |
| B.pH均为3的盐酸和醋酸溶液与足量锌反应,后者产生的氢气多 |
| C.NH4HSO4溶液呈酸性说明NH3·H2O是弱电解质 |
| D.0.2mol/L的醋酸溶液与0.1mol/L的NaOH溶液等体积混合:c(Na+)>c(CH3COO-) |
您最近一年使用:0次
单选题
|
容易(0.94)
19. 由同一反应物发生反应Ⅰ、Ⅱ时的能量变化如图所示,下列说法正确的是
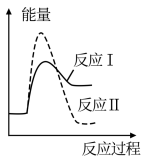

| A.反应Ⅰ能量变化类型与生石灰溶于水时的反应相同 |
| B.加催化剂后,反应结束时反应Ⅱ曲线不可能位于反应Ⅰ上方 |
| C.反应Ⅱ无需加热即可发生 |
| D.反应Ⅱ过程中断开化学键放出的能量大于形成化学键所吸收的能量 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
20. 判断有关说法正确的是
| A.NaCl晶体熔化时,既要克服离子间作用力,又要克服分子间作用力 |
| B.C60分子是有60个碳原子构成,所以C60属于原子晶体 |
| C.CCl4中所有原子最外层都形成了8个电子的结构 |
| D.MgCl2和NaOH所含有的化学键完全相同 |
您最近一年使用:0次
单选题
|
适中(0.65)
21. 某酸性工业废水中含有K2Cr2O7.光照下,草酸(H2C2O4)能将其中的Cr2O 转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:在25°C下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,作对比实验,完成以下实验设计表。
转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:在25°C下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,作对比实验,完成以下实验设计表。
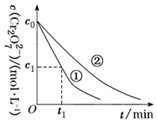
测得实验①和②溶液中的Cr2O 浓度随时间变化关系如图所示。下列叙述
浓度随时间变化关系如图所示。下列叙述不正确 的是:
 转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:在25°C下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,作对比实验,完成以下实验设计表。
转化为Cr3+。某课题组研究发现,少量铁明矾[Al2Fe(SO4)4·24H2O]即可对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:在25°C下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度草酸溶液用量,作对比实验,完成以下实验设计表。
| 实验编号 | 初始pH | 废水样品 体积mL | 草酸溶液 体积mL | 蒸馏水体 积mL |
| ① | 4 | 60 | 10 | 30 |
| ② | 5 | 60 | 10 | 30 |
| ③ | 5 | 60 | a | b |
 浓度随时间变化关系如图所示。下列叙述
浓度随时间变化关系如图所示。下列叙述| A.上述反应后草酸被氧化为CO2 |
| B.实验③中a和b如果是20和20,则反应速率③﹥② |
C.由曲线①可知,0~t1时间段反应速率v(Cr3+)= mol·L-1·min-1 mol·L-1·min-1 |
| D.实验①和②的结果表明,其他条件相同时,pH越小,该反应速率越快 |
您最近一年使用:0次
单选题
|
适中(0.65)
22. 设NA为阿伏加德罗常数的值,下列说法不正确 的是
| A.1mol甲基所含的电子数为7NA |
| B.1L0.1mol·L-1硫酸铵溶液中含有铵根离子的数目小于0.2NA |
| C.在一定条件下,1molNa与一定量O2反应生成Na2O和Na2O2的混合物,钠失去NA个电子 |
| D.0.1mol乙炔与乙二醇蒸气的混合气完全燃烧所消耗的氧分子数为0.25NA |
您最近一年使用:0次
单选题
|
适中(0.65)
23. 已知H2C2O4为二元弱酸。20℃时,往0.100mol·L-1的H2C2O4溶液中逐渐加入NaOH固体(溶液体积变化忽略不计),溶液中c(H2C2O4)、c(C2O )、c(HC2O
)、c(HC2O )随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系
)随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系正确 的是

 )、c(HC2O
)、c(HC2O )随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系
)随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系
A.图中a曲线表示H2C2O4,c曲线表示C2O |
B.当溶液中c(Na+)=0.100mol·L-1时,一定存在: c(H+)+c(H2C2O4)=c(OH-)+c(C2O ) ) |
C.M点的溶液中存在:c(HC2O )=c(C2O )=c(C2O )>c(Na+)>c(H+)>c(OH-) )>c(Na+)>c(H+)>c(OH-) |
D.pH=7.0的溶液中:c(Na+)=2c(C2O ) ) |
您最近一年使用:0次
2021-11-05更新
|
88次组卷
|
2卷引用:浙江省诸暨市2017-2018学年高三上学期期末考试化学试题
单选题
|
较易(0.85)
24. 某科研小组采用如下方案回收一种光盘金属层中的少量Ag(金属层中其他金属含量过低,对实验的影响可忽略)。

已知:①AgCl可溶于氨水:AgCl+2NH3·H2O Ag(NH3)
Ag(NH3) +Cl-+2H2O
+Cl-+2H2O
②常温时N2H4·H2O(水合肼)在碱性条件下能还原Ag(NH3) :4Ag(NH3)
:4Ag(NH3) +N2H4·H2O=4Ag↓+N2↑+4
+N2H4·H2O=4Ag↓+N2↑+4 +4NH3↑+H2O
+4NH3↑+H2O
③NaClO与NH3·H2O能发生反应
下列叙述不正确 的是:

已知:①AgCl可溶于氨水:AgCl+2NH3·H2O
 Ag(NH3)
Ag(NH3) +Cl-+2H2O
+Cl-+2H2O②常温时N2H4·H2O(水合肼)在碱性条件下能还原Ag(NH3)
 :4Ag(NH3)
:4Ag(NH3) +N2H4·H2O=4Ag↓+N2↑+4
+N2H4·H2O=4Ag↓+N2↑+4 +4NH3↑+H2O
+4NH3↑+H2O③NaClO与NH3·H2O能发生反应
下列叙述
| A.“氧化”阶段需在80℃条件下进行,适宜的加热方式为水浴加热 |
| B.“过滤Ⅰ”所得固体主要成分为AgCl |
| C.若省略“过滤Ⅰ”,直接向冷却后的反应容器中滴加10%氨水,对氨水的用量没有影响 |
| D.从“过滤Ⅱ”后的滤液中获取单质Ag的实验方案如下:向滤液中滴加2mol·L-1水合肼溶液,搅拌使其充分反应,同时用1mol·L-1H2SO4溶液吸收反应中放出的NH3,待溶液中无气泡产生,停止滴加,静置、过滤、洗涤、干燥 |
【知识点】 氧化还原反应的应用 物质分离、提纯综合应用解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
25. 氯化亚铜(CuCl)常用作有机合成工业中的催化剂,是一种白色粉末;微溶于水、不溶于乙醇及稀硫酸。下图是工业上用印刷电路的蚀刻液的废液(含Fe3+、Cu2+、Fe2+、Cl-)生产CuCl的流程:

下列叙述不正确 的是:

下列叙述
| A.物质Z可能是盐酸酸化过的双氧水 |
| B.滤渣②中主要成分为Cu |
| C.该生产流程可以实现硫酸的循环再利用 |
| D.定量分析流程图中的反应可知,理论上需不断补充SO2使氯化铜转化为CuCl晶体 |
您最近一年使用:0次
2021-11-05更新
|
122次组卷
|
2卷引用:浙江省诸暨市2017-2018学年高三上学期期末考试化学试题
四、解答题 添加题型下试题
解答题-有机推断题
|
适中(0.65)
解题方法
26. A为天然气的主要成分;B、C均能发生银镜反应;C分子式为C3H6O;D与CO、H2以物质的量1︰1︰1反应形成C;G是有芳香气味、不易溶于水的油状液体,其转化关系如下,请回答:
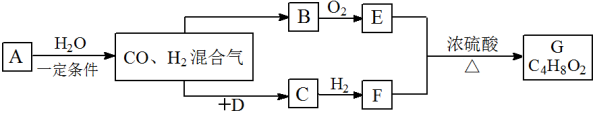
(1)D的结构式_____ 。
(2)C→F的反应类型_____ 。
(3)E+F→G的化学方程式_____ 。
(4)下列说法不正确 的是_____。

(1)D的结构式
(2)C→F的反应类型
(3)E+F→G的化学方程式
(4)下列说法
| A.可用酸性KMnO4溶液鉴别A和D |
| B.E、F均能与金属Na和NaHCO3溶液反应 |
| C.G与NaOH溶液共热后能重新生成E和F |
| D.与G具有相同官能团的同分异构体有2种 |
您最近一年使用:0次
解答题-无机推断题
|
较难(0.4)
27. 已知固体X仅由两种元素组成,实验流程和结果如下,请回答:
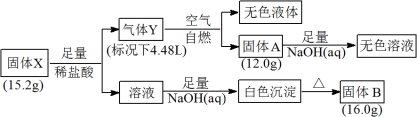
(1)白色沉淀的化学式_____ ,气体Y分子的电子式_____ 。
(2)固体A与足量NaOH溶液反应的离子方程式_____ 。
(3)已知某单质与固体A在高温下会生成固体X,试写出相应的化学方程式_____ 。

(1)白色沉淀的化学式
(2)固体A与足量NaOH溶液反应的离子方程式
(3)已知某单质与固体A在高温下会生成固体X,试写出相应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
解题方法
28. 为验证CO与灼热CuO反应的产物,某实验小组利用如下装置进行实验。
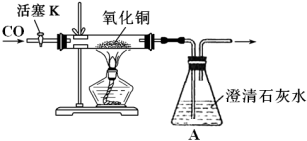
已知:红色的氧化亚铜能与酸发生反应,Cu2O+2H+=Cu2++Cu+H2O。
(1)检查装置气密性的方法是_____ 。
(2)反应结束,取反应管中的少量固体,加入稀硫酸,观察到_____ (填现象),说明反应有Cu2O生成。
(3)下列说法正确的是_____。

已知:红色的氧化亚铜能与酸发生反应,Cu2O+2H+=Cu2++Cu+H2O。
(1)检查装置气密性的方法是
(2)反应结束,取反应管中的少量固体,加入稀硫酸,观察到
(3)下列说法正确的是_____。
| A.本实验必须补充尾气处理装置 |
| B.实验开始时,先加热反应管,再缓缓通入CO |
| C.A中导管口浸入液面以下,以便于观察CO的流速并可防止反应过程中空气进入反应管 |
| D.反应结束后,必须先将A中导管口移出液面,冷却后再停止通CO,以防倒吸 |
您最近一年使用:0次
五、计算题 添加题型下试题
计算题
|
适中(0.65)
名校
29. 取48.0gFe2O3,一定温度下加热,残留固体47.36g。将该剩余固体溶于足量盐酸,此过程没有气体产生;所得溶液中再加入足量KI溶液。请计算:
(1)生成I2的物质的量_____ 。
(2)若分解产物为Fe3O4,求Fe2O3的分解率_____ 。
(1)生成I2的物质的量
(2)若分解产物为Fe3O4,求Fe2O3的分解率
您最近一年使用:0次
2021-11-05更新
|
339次组卷
|
2卷引用:浙江省诸暨市2017-2018学年高三上学期期末考试化学试题
六、解答题 添加题型下试题
解答题-原理综合题
|
适中(0.65)
30. 碳酸二甲酯[(CH3O)2CO,DMC]是一种重要的绿色化工原料,可以利用CO、O2与甲醇在PdCl2-CuCl2/AC催化剂作用下,反应得到,容器中发生如下3个反应:
反应①:2CH3OH(g)+CO(g)+1/2O2(g) DMC(g)+H2O(g)ΔH1
DMC(g)+H2O(g)ΔH1
反应②:CO(g)+1/2O2(g) CO2(g)ΔH2<0
CO2(g)ΔH2<0
反应③:DMC(g)+H2O(g) 2CH3OH(g)+CO2(g)ΔH3>0
2CH3OH(g)+CO2(g)ΔH3>0
请回答:
(1)反应①在一定条件下能自发进行,判断ΔH1_____ 0(填:<、>或=)
(2)下列说法正确的是:
(3)探究该反应进行的最佳温度和最佳CO/O2体积比,某兴趣小组查阅资料,在确定甲醇体积分数为0.20,压强为0.3MPa的条件下进行实验。
①在一定温度下,改变CO/O2体积比,得到甲醇平均转化率(图1)、DMC选择性(图2)随时间的变化关系。试问0~5h内最适宜的CO/O2体积比是_____ 。
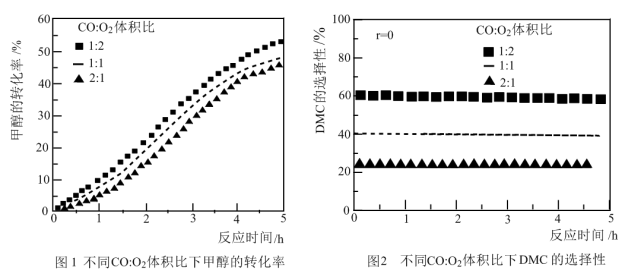
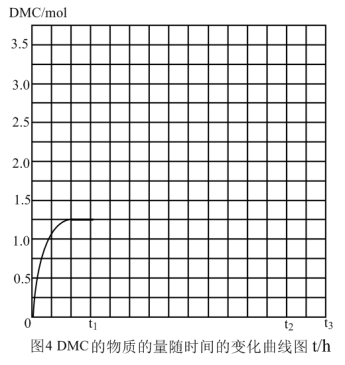
②固定CO/O2体积比和压强,改变温度,记录DMC的物质的量(I)、甲醇的物质的量(II)和CO2的物质的量(III)如图3所示。试问该反应最适宜的温度为_____ ,理由是_____ 。

③反应①在0.3MPa、400K时,甲醇的平衡转化率为52.0%,DMC的选择性为65.0%。现向某装置中加入20mol的甲醇和一定量的CO、O2,反应的起始温度为480K,在t1时刻,降低温度至400K,反应至t2重新达到平衡。试画出t1~t3时刻DMC的物质的量随时间的变化曲线_____ 。
(4)有研究表明,以铂为电极,在离子液体-CH3OK-甲醇体系中常温常压下,CO2和甲醇电催化合成DMC。在离子液体环境下,CH3OK可电离出CH3O-;而甲醇在此环境下,用K做电子转移促进剂,可直接解离成与CH3OK相同的CH3O-。试写出该状态下阳极电极方程式_____ 。
反应①:2CH3OH(g)+CO(g)+1/2O2(g)
 DMC(g)+H2O(g)ΔH1
DMC(g)+H2O(g)ΔH1反应②:CO(g)+1/2O2(g)
 CO2(g)ΔH2<0
CO2(g)ΔH2<0反应③:DMC(g)+H2O(g)
 2CH3OH(g)+CO2(g)ΔH3>0
2CH3OH(g)+CO2(g)ΔH3>0请回答:
(1)反应①在一定条件下能自发进行,判断ΔH1
(2)下列说法正确的是:
| A.在恒容容器中达平衡的反应③,在温度升高的同时带来容器内压强变大,因此平衡逆向移动 |
| B.在恒温恒容容器中达平衡的反应②,充入一定量CO2(g),重新达平衡后,CO2的体积分数大于原平衡,平衡正向移动 |
| C.当合成DMC容器中甲醇和CO2的物质的量之比不再变化时,反应③一定达到平衡状态 |
| D.反应②随着温度的升高,平衡逆向移动,平衡常数减小,正反应速率增大,逆反应速率减小 |
①在一定温度下,改变CO/O2体积比,得到甲醇平均转化率(图1)、DMC选择性(图2)随时间的变化关系。试问0~5h内最适宜的CO/O2体积比是

②固定CO/O2体积比和压强,改变温度,记录DMC的物质的量(I)、甲醇的物质的量(II)和CO2的物质的量(III)如图3所示。试问该反应最适宜的温度为

③反应①在0.3MPa、400K时,甲醇的平衡转化率为52.0%,DMC的选择性为65.0%。现向某装置中加入20mol的甲醇和一定量的CO、O2,反应的起始温度为480K,在t1时刻,降低温度至400K,反应至t2重新达到平衡。试画出t1~t3时刻DMC的物质的量随时间的变化曲线

(4)有研究表明,以铂为电极,在离子液体-CH3OK-甲醇体系中常温常压下,CO2和甲醇电催化合成DMC。在离子液体环境下,CH3OK可电离出CH3O-;而甲醇在此环境下,用K做电子转移促进剂,可直接解离成与CH3OK相同的CH3O-。试写出该状态下阳极电极方程式
您最近一年使用:0次
解答题-实验探究题
|
较难(0.4)
解题方法
31. 实验室制取溴乙烷原理如下:NaBr+H2SO4→HBr+NaHSO4;C2H5OH+HBr C2H5Br+H2O。同时会产生乙醚、乙烯、Br2等副产物。已知部分物质的物理性质:
C2H5Br+H2O。同时会产生乙醚、乙烯、Br2等副产物。已知部分物质的物理性质:


步骤如下:
①向50mL容器A中加入10mL无水乙醇、15mL浓硫酸和6mL水。
②冷至室温后,加入9.27克溴化钠及几粒沸石,进行蒸馏。
③小火加热,约30min后慢慢加大火焰,直至无油状物馏出为止。
④将馏出物倒入分液漏斗中,分出有机层,置于25mL干燥的锥形瓶中。将锥形瓶浸于冰水浴,边振荡边加入约4.5mLX。用分液漏斗分去X液,将溴乙烷倒入蒸馏烧瓶,水浴加热进行蒸馏,收集36-40℃的馏分,产量6.54克。
(1)步骤①中,容器A的名称为_____ ;加入6mL水的目的_____ ;
(2)步骤②中,若在蒸馏过程中发现忘加沸石,如何处理_____ ;蒸馏装置的锥形瓶需放入少量冷水并浸入冷水浴中,接收器末端则稍微浸没在冷水中,主要的目的是_____ ;
(3)步骤④中,X最适宜的试剂为_____;
(4)下列说法合理的有_____。
(5)本次实验的产率为_____ 。
 C2H5Br+H2O。同时会产生乙醚、乙烯、Br2等副产物。已知部分物质的物理性质:
C2H5Br+H2O。同时会产生乙醚、乙烯、Br2等副产物。已知部分物质的物理性质:| 物理性质 | 沸点 | 挥发性 | 密度/g•mL-1 | 溶解性 |
| 乙醇 | 78.3 | 易挥发 | 0.713 | 与水任意比互溶,易溶于浓硫酸 |
| 乙醚 | 34.6 | 易挥发 | 0.789 | 微溶于冷水,易溶于乙醇、浓硫酸等 |
| 溴乙烷 | 38.4℃ | 易挥发 | 1.46 | 难溶于冷水,易溶于乙醇等有机溶剂 |


步骤如下:
①向50mL容器A中加入10mL无水乙醇、15mL浓硫酸和6mL水。
②冷至室温后,加入9.27克溴化钠及几粒沸石,进行蒸馏。
③小火加热,约30min后慢慢加大火焰,直至无油状物馏出为止。
④将馏出物倒入分液漏斗中,分出有机层,置于25mL干燥的锥形瓶中。将锥形瓶浸于冰水浴,边振荡边加入约4.5mLX。用分液漏斗分去X液,将溴乙烷倒入蒸馏烧瓶,水浴加热进行蒸馏,收集36-40℃的馏分,产量6.54克。
(1)步骤①中,容器A的名称为
(2)步骤②中,若在蒸馏过程中发现忘加沸石,如何处理
(3)步骤④中,X最适宜的试剂为_____;
| A.接近0℃的冷水 | B.无水乙醇 |
| C.热水 | D.浓硫酸 |
| A.向容器A中投料时,需在不断振荡和冷水冷却下,缓慢依次地加入浓硫酸、乙醇和水 |
| B.萃取分液时,需振摇并放气,操作如右图 |
| C.蒸馏时,若温度计水银球位置偏低,则收集到的产品中可能会带入低沸点的杂质 |
| D.若所得产品略带黄色,可用活性炭脱色,并用玻璃纤维代替滤纸滤去活性炭 |
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
32. 8-羟基喹啉常用作医药中间体,某合成路线如下:
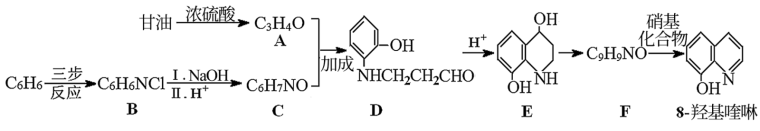
已知: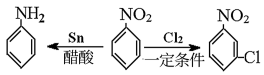 。请回答下列问题:
。请回答下列问题:
(1)写出化合物B中官能团的名称_____ 。
(2)下列说法不正确 的是_____。
(3)设计化合物C6H6经三步反应转变为B的合成路线(用流程图表示,试剂任选)_____ 。
(4)写出A+CD的化学方程式_____ 。
(5)写出所有符合下列条件的化合物D可能的同分异构体的结构简式_____ 。
①能与FeCl3溶液发生显色反应
②1H-NMR谱表明分子中有4种不同化学环境的氢原子
③结构中除了苯环不含有其他环状结构

已知:
 。请回答下列问题:
。请回答下列问题:(1)写出化合物B中官能团的名称
(2)下列说法
| A.化合物E的分子式是C9H11NO2 |
| B.1molD与H2反应最多消耗3molH2 |
| C.化合物C具有两性 |
| D.F8-羟基喹啉,属于氧化反应 |
(4)写出A+CD的化学方程式
(5)写出所有符合下列条件的化合物D可能的同分异构体的结构简式
①能与FeCl3溶液发生显色反应
②1H-NMR谱表明分子中有4种不同化学环境的氢原子
③结构中除了苯环不含有其他环状结构
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:认识化学科学、化学实验基础、化学反应原理、化学与STSE、常见无机物及其应用、有机化学基础、物质结构与性质
试卷题型(共 32题)
题型
数量
单选题
24
多选题
1
解答题
6
计算题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 酸、碱、盐、氧化物的概念及其相互联系 | |
| 2 | 0.94 | 常用仪器及使用 | |
| 3 | 0.94 | 电解质与非电解质 | |
| 4 | 0.94 | 胶体的定义及分类 胶体的性质和应用 | |
| 5 | 0.94 | 常见能量转化形式 石油能源现状及其产品的利用 煤的综合利用 | |
| 6 | 0.94 | 硅的物理性质与用途 明矾的净水作用及原理 化学科学对人类文明发展的意义 | |
| 7 | 0.94 | 四种基本反应类型 氧化还原反应基本概念 | |
| 8 | 0.94 | 化学用语综合判断 原子结构示意图、离子结构示意图 有机物的结构式、结构简式、比例模型、球棍模型、最简式 常见官能团名称、组成及结构 | |
| 9 | 0.85 | 氨水的性质 盐溶液的酸碱性判断 | |
| 10 | 0.85 | 焰色试验 常见阳离子的检验 常见阴离子的检验 | |
| 11 | 0.65 | 烷烃系统命名法 “四同”的相关比较 同分异构体的数目的确定 几组常见同素异形体 | |
| 12 | 0.65 | 离子方程式的正误判断 二氧化硫与其他强氧化剂的反应 硅酸的制备 碳酸氢钠与碱反应 | |
| 13 | 0.65 | 微粒半径大小的比较方法 根据原子结构进行元素种类推断 “位构性”关系理解及应用 | |
| 14 | 0.65 | 乙醇与钠反应 乙醇燃烧的相关计算 乙醛与新制氢氧化铜悬浊液的反应 乙酸具有酸的通性 | |
| 15 | 0.65 | 蔗糖与麦芽糖的水解 糖类生产乙醇 蛋白质组成结构 石油裂化、裂解 | |
| 17 | 0.65 | 原电池正负极判断 原电池电极反应式书写 新型电池 | |
| 18 | 0.65 | 酸碱混合时的定性判断及计算 强电解质与弱电解质 一元强酸与一元弱酸的比较 盐溶液中离子浓度大小的比较 | |
| 19 | 0.94 | 化学反应中能量变化的原因 吸热反应和放热反应 催化剂对化学反应速率的影响 | |
| 20 | 0.65 | 常见分子晶体的结构 晶体的类型与物质熔点、硬度、导电性的关系 | |
| 21 | 0.65 | 氧化还原反应方程式的配平 影响化学反应速率的因素 化学反应速率计算 | |
| 22 | 0.65 | 阿伏加德罗常数的求算 钠与氧气等非金属的反应 盐类水解规律 醇的燃烧 | |
| 23 | 0.65 | 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 24 | 0.85 | 氧化还原反应的应用 物质分离、提纯综合应用 | |
| 25 | 0.65 | 氧化还原反应在生活、生产中的应用 有关铁及其化合物转化的流程题型 常见无机物的制备 | |
| 二、多选题 | |||
| 16 | 0.65 | 依据热化学方程式的计算 影响化学反应速率的因素 化学平衡状态的判断方法 转化率的相关计算及判断 | |
| 三、解答题 | |||
| 26 | 0.65 | 羧酸酯化反应 酯的水解反应机理 有机物的推断 | 有机推断题 |
| 27 | 0.4 | 原子、离子、原子团及其电子式的书写与判断 氧化还原反应方程式的配平 无机综合推断 二氧化硅的化学性质 | 无机推断题 |
| 28 | 0.65 | 化学实验基础操作 实验安全 物质性质实验方案的设计 | 实验探究题 |
| 30 | 0.65 | 温度对化学反应速率的影响 化学平衡的移动及其影响因素 化学反应进行方向的判据 电解池电极反应式及化学方程式的书写与判断 | 原理综合题 |
| 31 | 0.4 | 化学方程式计算中物质的量的运用 乙醇与氢卤酸的取代反应 常见有机物的制备 | 实验探究题 |
| 32 | 0.4 | 醛基的加成反应 有机物的推断 | 有机推断题 |
| 四、计算题 | |||
| 29 | 0.65 | 化学方程式计算中物质的量的运用 氧化还原反应有关计算 几种铁的氧化物的化学性质 | |







