为验证CO与灼热CuO反应的产物,某实验小组利用如下装置进行实验。
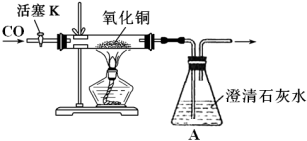
已知:红色的氧化亚铜能与酸发生反应,Cu2O+2H+=Cu2++Cu+H2O。
(1)检查装置气密性的方法是_____ 。
(2)反应结束,取反应管中的少量固体,加入稀硫酸,观察到_____ (填现象),说明反应有Cu2O生成。
(3)下列说法正确的是_____。

已知:红色的氧化亚铜能与酸发生反应,Cu2O+2H+=Cu2++Cu+H2O。
(1)检查装置气密性的方法是
(2)反应结束,取反应管中的少量固体,加入稀硫酸,观察到
(3)下列说法正确的是_____。
| A.本实验必须补充尾气处理装置 |
| B.实验开始时,先加热反应管,再缓缓通入CO |
| C.A中导管口浸入液面以下,以便于观察CO的流速并可防止反应过程中空气进入反应管 |
| D.反应结束后,必须先将A中导管口移出液面,冷却后再停止通CO,以防倒吸 |
更新时间:2021-11-05 15:33:43
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】硫酸铜晶体里结晶水的测定实验中,首先应将晶体放在________ 中研碎,晶体应在_________ 中加热,冷却时应将其放在___________ 中进行,如果不这样冷却则实验结果会_______ (填“偏高”或“偏低”或“无影响”)。此实验至少量______ 次。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某课外活动小组欲利用CuO与NH3的反应研究NH3的某种性质并测定其组成,设计了如图实验装置(夹持装置未画出)进行实验。请回答下列问题:
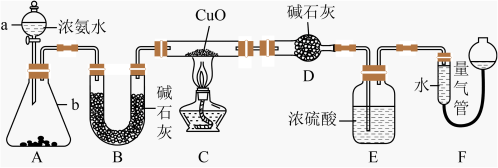
(1)仪器a的名称为_______ ;仪器b中可选择的试剂为_______ 。
(2)实验中观察到装置C中黑色CuO粉末变为红色粉末,量气管有无色无味的气体产生,写出相应的化学方程式:_______ 。
(3)读取气体体积前,应对装置F进行的操作:_______ 。
(4)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢的原子个数比值为_______ (用含m、n字母的代数式表示)。

(1)仪器a的名称为
(2)实验中观察到装置C中黑色CuO粉末变为红色粉末,量气管有无色无味的气体产生,写出相应的化学方程式:
(3)读取气体体积前,应对装置F进行的操作:
(4)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢的原子个数比值为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
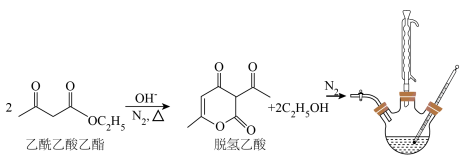
【推荐3】脱氢乙酸是一种重要的有机合成中间体和低毒高效食品防腐剂,实验室以乙酰乙酸乙酯为原料,在OH-的催化作用下制备脱氢乙酸的反应原理和实验装置如图(夹持和加热装置已省略):
Ⅰ.脱氢乙酸的合成
①在N2氛围中,向三颈烧瓶中加入100 mL乙酰乙酸乙酯和0.05 g催化剂,磁力搅拌加热10 min后再升高至某温度,回流一段时间。
②反应结束后,将其改为蒸馏装置,控制温度为80℃左右蒸出乙醇,在三颈烧瓶中得到脱氢乙酸粗产品。
Ⅱ.脱氢乙酸的分离与提纯
将盛有脱氢乙酸粗产品的三颈烧瓶改为下图中的装置B,进行水蒸气蒸馏(夹持和加热装置已省略),蒸出乙酰乙酸乙酯和脱氢乙酸,过滤装置C中的混合物,得白色晶体,再用乙醇洗涤该晶体,干燥后得固体产品56.0 g。
(1)步骤Ⅰ中通入N2的目的是___________ 。
(2)步骤Ⅰ中②过程中不需要用到的仪器为___________ (填字母)。___________ ℃、___________ h、___________ 作催化剂。与其他催化剂相比,所选催化剂使脱氢乙酸产率最高的原因可能为___________ 。___________ ,漏斗的作用为___________ 。
(5)脱氢乙酸的产率约为___________(填字母)。
| 名称 | 相对分子质量 | 性状 | 密度/ | 熔点/℃ | 沸点/℃ | 物理性质 |
| 乙酰乙酸乙酯 | 130 | 无色透明液体 | 1.03 | -39 | 180.8 | 微溶于水,易溶于乙醇等有机溶剂 |
| 脱氢乙酸 | 168 | 白色晶体 | — | 109~111 | 269.9 | 微溶于乙醇和冷水,具有较强的还原性 |
| 乙醇 | 46 | 无色透明液体 | 0.79 | -114.1 | 78.3 | 与水任意比例互溶,易溶于有机溶剂 |
①在N2氛围中,向三颈烧瓶中加入100 mL乙酰乙酸乙酯和0.05 g催化剂,磁力搅拌加热10 min后再升高至某温度,回流一段时间。
②反应结束后,将其改为蒸馏装置,控制温度为80℃左右蒸出乙醇,在三颈烧瓶中得到脱氢乙酸粗产品。
Ⅱ.脱氢乙酸的分离与提纯
将盛有脱氢乙酸粗产品的三颈烧瓶改为下图中的装置B,进行水蒸气蒸馏(夹持和加热装置已省略),蒸出乙酰乙酸乙酯和脱氢乙酸,过滤装置C中的混合物,得白色晶体,再用乙醇洗涤该晶体,干燥后得固体产品56.0 g。
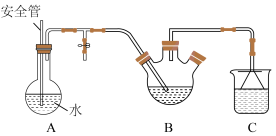
(1)步骤Ⅰ中通入N2的目的是
(2)步骤Ⅰ中②过程中不需要用到的仪器为


(5)脱氢乙酸的产率约为___________(填字母)。
| A.54% | B.64% | C.74% | D.84% |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】I.回答下列问题:
(1)下列实验装置与实验操作正确的是_______

II.实验室里需要纯净的氯化钠溶液,但现在只有混有硫酸钠、碳酸氢铵的氯化钠。某学生设计了如下方案:

如果此方案正确,那么
(2)操作①加热可选择_______ 仪器,加热后产生的气体有刺激气味,写出反应的化学方程式_______
(3)操作②BaCl2溶液是否可改为加硝酸钡溶液?为什么?_______
(4)操作③加Na2CO3的目的是_______
(5)操作④加热煮沸的目的是_______ 。
(6)纯净的NaCl溶液通过_______ (操作)得到NaCl固体。用NaCl固体配制0.1 mol·L-1的NaCl溶液,实验中造成所配溶液浓度偏低的原因可能是_______ 。
A.容量瓶中原来含有少量蒸馏水
B.定容摇匀后少量溶液外流
C.向容量瓶中加水定容时眼睛一直仰视刻度线
(1)下列实验装置与实验操作正确的是

II.实验室里需要纯净的氯化钠溶液,但现在只有混有硫酸钠、碳酸氢铵的氯化钠。某学生设计了如下方案:

如果此方案正确,那么
(2)操作①加热可选择
(3)操作②BaCl2溶液是否可改为加硝酸钡溶液?为什么?
(4)操作③加Na2CO3的目的是
(5)操作④加热煮沸的目的是
(6)纯净的NaCl溶液通过
A.容量瓶中原来含有少量蒸馏水
B.定容摇匀后少量溶液外流
C.向容量瓶中加水定容时眼睛一直仰视刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】Co(CH3COO)2⋅4H2O(乙酸钴)是一种重要的有机化工原料。为探究乙酸钴Co(CH3COO)2的热分解产物,先在低于100℃时使其脱去结晶水,然后用下列装置进行实验(已知CO能与PdCl2溶液反应生成黑色Pd沉淀):

回答下列问题:
(1)通N2的目的是________ 。
(2)澄清石灰水和PdCl2溶液分别用于检验CO2和CO,其中盛放PdCl2溶液的装置是_________ (填字母)。
(3)实验结束时,为防止倒吸,正确的操作是________ 。
(4)装置a中完全反应后得到钴的一种氧化物,固体残留率(固体样品的剩余质量固体样品的起始质量×100%)为45.4%.该氧化物的化学式为_________ 。(相对原子质量:Co-59)

回答下列问题:
(1)通N2的目的是
(2)澄清石灰水和PdCl2溶液分别用于检验CO2和CO,其中盛放PdCl2溶液的装置是
(3)实验结束时,为防止倒吸,正确的操作是
(4)装置a中完全反应后得到钴的一种氧化物,固体残留率(固体样品的剩余质量固体样品的起始质量×100%)为45.4%.该氧化物的化学式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某课外研究小组,用废弃的黄铜(铜锌合金),通过两种途径制取硫酸铜晶体。实验流程如图所示:

(1)操作a为_____ ,该操作中用到的玻璃仪器有烧杯、_____ 、玻璃棒。
(2)浓硫酸是化学实验室里一种常见的酸。
①实验室稀释浓硫酸的操作是:将______________________ ,并用玻璃棒不断搅拌。
②化学实验应高度关注安全问题。若不慎将少量浓硫酸沾到皮肤上,应先用大量水冲洗,再涂_______________ 溶液。
(3)如图是实验室用过氧化氢溶液和二氧化锰制取氧气的装置。

①主要实验操作步骤有:
a.收集气体 b.检查装置气密性 c.将二氧化锰放入锥形瓶中 d.从长颈漏斗中注入过氧化氢溶液
正确的操作顺序是_____ (写字母序号)。
②在实验过程中,某同学因加入的药品量不足,致使集气瓶内剩余少量水。若想集满这瓶氧气,在不拆卸装置和不添加药品的前提下,请帮他想出种解决的方法__________________ 。
(4)操作b的顺序为蒸发浓缩、_____ 过滤、干燥。
(5)下列测定稀硫酸pH的操作正确的是_____ (写字母序号)。
A.将pH试纸直接插入稀硫酸中
B.先将pH试纸用蒸馏水润湿
C.用玻璃棒蘸取少量稀硫酸,滴在pH试纸上
D.根据试纸显示的颜色估算出溶液的pH

(1)操作a为
(2)浓硫酸是化学实验室里一种常见的酸。
①实验室稀释浓硫酸的操作是:将
②化学实验应高度关注安全问题。若不慎将少量浓硫酸沾到皮肤上,应先用大量水冲洗,再涂
(3)如图是实验室用过氧化氢溶液和二氧化锰制取氧气的装置。

①主要实验操作步骤有:
a.收集气体 b.检查装置气密性 c.将二氧化锰放入锥形瓶中 d.从长颈漏斗中注入过氧化氢溶液
正确的操作顺序是
②在实验过程中,某同学因加入的药品量不足,致使集气瓶内剩余少量水。若想集满这瓶氧气,在不拆卸装置和不添加药品的前提下,请帮他想出种解决的方法
(4)操作b的顺序为蒸发浓缩、
(5)下列测定稀硫酸pH的操作正确的是
A.将pH试纸直接插入稀硫酸中
B.先将pH试纸用蒸馏水润湿
C.用玻璃棒蘸取少量稀硫酸,滴在pH试纸上
D.根据试纸显示的颜色估算出溶液的pH
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题:
探究一 设计如图所示装置进行“铁与水反应”的实验。

(1)硬质玻璃管中发生反应的化学方程式为_______________
(2)反应前A中投放碎瓷片的目的是_________________
(3)装置E中的现象是_____________________
探究二 设计如下实验方案确定反应后硬质玻璃管中黑色固体的成分。
(4)待硬质玻璃管B冷却后,取少许其中的固体物质溶于________ 后,将所得溶液分成两份,其中一份滴加几滴KSCN溶液,若溶液变红色,推断硬质玻璃管B中固体物质的成分为_____ (选填序号,下同);若溶液未变红色,推断硬质玻璃管B中固体物质的成分为________ 。
①一定有Fe3O4 ②一定有Fe ③只有Fe3O4 ④只有Fe
探究一 设计如图所示装置进行“铁与水反应”的实验。

(1)硬质玻璃管中发生反应的化学方程式为
(2)反应前A中投放碎瓷片的目的是
(3)装置E中的现象是
探究二 设计如下实验方案确定反应后硬质玻璃管中黑色固体的成分。
(4)待硬质玻璃管B冷却后,取少许其中的固体物质溶于
①一定有Fe3O4 ②一定有Fe ③只有Fe3O4 ④只有Fe
您最近一年使用:0次
【推荐2】亚硫酸钠(Na2SO3)是印染工业中常用的脱氧剂和漂白剂。回答下列问题:
(1)实验室用H2SO4和NaHSO3制取SO2的化学方程式为:___________
(2)SO2可以与H2S反应,请写出其化学方程式:___________ 。
(3)亚硫酸钠易被氧化而变质为Na2SO4,选用下列试剂设计实验方案,检验亚硫酸钠样品氧化变质的程度。仅供选择的试剂:稀盐酸、稀H2SO4、稀HNO3、BaCl2溶液、酸性KMnO4溶液、H2O2溶液
(4)(Ga)与A1同主族,化学性质相似,是制造半导体材料氮化镓的重要原料,其中电解NaGaO2是获得Ga单质的重要方法,如图所示,则阴极的电极反应为:___________ 。若电解获得1molGa,则阳极产生的气体在标准状况下的体积至少为 ___________ L。

(1)实验室用H2SO4和NaHSO3制取SO2的化学方程式为:
(2)SO2可以与H2S反应,请写出其化学方程式:
(3)亚硫酸钠易被氧化而变质为Na2SO4,选用下列试剂设计实验方案,检验亚硫酸钠样品氧化变质的程度。仅供选择的试剂:稀盐酸、稀H2SO4、稀HNO3、BaCl2溶液、酸性KMnO4溶液、H2O2溶液
| 实验编号 | 实验步骤 | 现象 | 结论 |
| I | 取少量样品,加入除氧蒸馏水 | 固体完全溶解,得到无色溶液 | / |
| II | 取实验I的溶液, | 样品存在氧化变质 | |
| III | 另取实验I的溶液, | 样品并未完全氧化变质 |

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】实验室做乙醛和银氨溶液发生银镜反应的实验时:
(1)为产生光亮的银镜,试管应先用______ 溶液煮沸,倒掉煮沸液后再用清水将试管冲洗干净。
(2)配制银氨溶液时向盛有__________ 溶液的试管中逐滴滴加__________ 溶液边滴边振荡直到__________ 为止。有关化学反应的离子方程式为:①_____________________ ;②_________________________ 。
(3)加热时应用________ 加热,产生银镜的化学方程式:____________________ 。
(4)实验室配制银氨溶液时若向AgNO 3 溶液中加入氨水形成银氨溶液时,应防止加入氨水过量,否则容易生成容易爆炸的________ ,试剂本身也失去灵敏性。配制好的银氨溶液不可久置,否则会生成________ ,从溶液中析出这种沉淀,哪怕是用玻璃棒刮擦也会分解发生猛烈的爆炸。
(1)为产生光亮的银镜,试管应先用
(2)配制银氨溶液时向盛有
(3)加热时应用
(4)实验室配制银氨溶液时若向AgNO 3 溶液中加入氨水形成银氨溶液时,应防止加入氨水过量,否则容易生成容易爆炸的
您最近一年使用:0次



