取48.0gFe2O3,一定温度下加热,残留固体47.36g。将该剩余固体溶于足量盐酸,此过程没有气体产生;所得溶液中再加入足量KI溶液。请计算:
(1)生成I2的物质的量_____ 。
(2)若分解产物为Fe3O4,求Fe2O3的分解率_____ 。
(1)生成I2的物质的量
(2)若分解产物为Fe3O4,求Fe2O3的分解率
更新时间:2021-11-05 15:33:43
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】将5.92g固体试样xNa2CO3·yNaHCO3溶于水中,分成两等份,一份加入足量的Ba(OH)2溶液,充分反应后,静置过滤,得5.91g沉淀。另一份逐滴滴加1.0mol/L的稀盐酸,当滴加VmL盐酸时,产生的气体体积恰好达到最大值。求:
(1)该试样的组成为_______ ;
(2)V=_______ mL。
(1)该试样的组成为
(2)V=
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在100mL某浓度的CuSO4溶液中加入一质量为45.0g的铁棒,反应一段时间后,取出洗净,干燥后称量,称得质量变为46.6g。
(1)写出该反应的离子方程式。
(2)反应掉的铁的质量为多少克?
(3)若反应后溶液的体积不变,求所得溶液中FeSO4的物质的量浓度。
(1)写出该反应的离子方程式。
(2)反应掉的铁的质量为多少克?
(3)若反应后溶液的体积不变,求所得溶液中FeSO4的物质的量浓度。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】氨气和氧气在催化剂存在下的反应方程式为4NH3+5O2 4NO+6H2O,完成下列计算:
4NO+6H2O,完成下列计算:
(1)生成1 mol NO消耗氧气的体积为__________ L(标准状况)。
(2)5 mol NH3和5 molO2反应生成4 mol NO,过量的氨溶于产物水中成为氨水,计算该氨水中氨的质量分数。_______
(3)如果没有催化剂,氨氧化生成NO的同时也生成氮气:4NH3+3O2=2N2+6H2O。若4 mol NH3和4 molO2恰好完全反应,计算产物气体中NO的物质的量。_________
 4NO+6H2O,完成下列计算:
4NO+6H2O,完成下列计算:(1)生成1 mol NO消耗氧气的体积为
(2)5 mol NH3和5 molO2反应生成4 mol NO,过量的氨溶于产物水中成为氨水,计算该氨水中氨的质量分数。
(3)如果没有催化剂,氨氧化生成NO的同时也生成氮气:4NH3+3O2=2N2+6H2O。若4 mol NH3和4 molO2恰好完全反应,计算产物气体中NO的物质的量。
您最近一年使用:0次
【推荐2】已知硝酸铵在不同温度下分解会有不同的产物,反应方程式如下,
①NH4NO3 NH3↑+HNO3↑②NH4NO3
NH3↑+HNO3↑②NH4NO3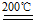 N2O↑+2H2O↑
N2O↑+2H2O↑
③2NH4NO3 2N2↑+O2↑+4X↑④4NH4NO3
2N2↑+O2↑+4X↑④4NH4NO3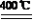 3N2↑+2NO2↑+8H2O↑
3N2↑+2NO2↑+8H2O↑
请回答下列问题:
(1)这四个反应中属于氧化还原反应的有___ 个。
(2)反应③中物质X的化学式是___ 。
(3)反应④中氧化产物和还原产物依次是___ 、___ 。(填化学式)
(4)若反应③生成标准状况下的11.2L氧气,则转移电子数为___ 。
①NH4NO3
 NH3↑+HNO3↑②NH4NO3
NH3↑+HNO3↑②NH4NO3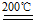 N2O↑+2H2O↑
N2O↑+2H2O↑③2NH4NO3
 2N2↑+O2↑+4X↑④4NH4NO3
2N2↑+O2↑+4X↑④4NH4NO3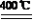 3N2↑+2NO2↑+8H2O↑
3N2↑+2NO2↑+8H2O↑请回答下列问题:
(1)这四个反应中属于氧化还原反应的有
(2)反应③中物质X的化学式是
(3)反应④中氧化产物和还原产物依次是
(4)若反应③生成标准状况下的11.2L氧气,则转移电子数为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】某红色固体粉末可能是 、
、 或二者混合物,为探究其组成,称取
或二者混合物,为探究其组成,称取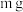 该固体粉末样品,用足量的稀
该固体粉末样品,用足量的稀 充分反应,反应后得到的固体质量为
充分反应,反应后得到的固体质量为 。
。
已知:
(1)若红色固体粉末为纯净物,则
___________ (用含m的最简式表示)。
(2)若 ,计算溶液中
,计算溶液中 与
与 的物质的量之比
的物质的量之比___________ (写出计算过程)。
 、
、 或二者混合物,为探究其组成,称取
或二者混合物,为探究其组成,称取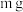 该固体粉末样品,用足量的稀
该固体粉末样品,用足量的稀 充分反应,反应后得到的固体质量为
充分反应,反应后得到的固体质量为 。
。已知:

(1)若红色固体粉末为纯净物,则

(2)若
 ,计算溶液中
,计算溶液中 与
与 的物质的量之比
的物质的量之比
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】准确称取6g铝土矿样品(含Al2O3、Fe2O3、SiO2),放入100mL某浓度的HCl溶液中(SiO2不溶于HCl溶液),充分反应后过滤,向滤液中加入10 mol/L的NaOH溶液,产生沉淀的质量m与加入NaOH溶液的体积的关系如图所示
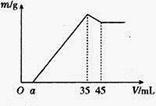
求:
(1)原溶液中c(HCl)=_______ mol/L。
(2)若a=2.6mL,计算各组分的质量:m(Al2O3)=_______ g;m(SiO2)=________ g。

求:
(1)原溶液中c(HCl)=
(2)若a=2.6mL,计算各组分的质量:m(Al2O3)=
您最近一年使用:0次


 Cl2↑+MnCl2+2H2O
Cl2↑+MnCl2+2H2O

