钢铁制品经常进行烤蓝处理,主要目的是在表面生成一层致密的Fe3O4。为了研究烤蓝铁片,把一定量烤蓝铁片加工成均匀粉末,取mg该粉末,放入28.00 mL 1.000mol·L-1的盐酸中,恰好完全反应,生成134.4 mL气体(标准状况)。向反应后的溶液中滴入KSCN溶液,无明显现象。
(1)计算mg样品中n(Fe3O4)=______ mol。
(2)写出具体计算过程∶_______________ 。
(1)计算mg样品中n(Fe3O4)=
(2)写出具体计算过程∶
更新时间:2020-06-20 19:38:29
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】取48.0gFe2O3,一定温度下加热,残留固体47.36g。将该剩余固体溶于足量盐酸,此过程没有气体产生;所得溶液中再加入足量KI溶液。请计算:
(1)生成I2的物质的量_____ 。
(2)若分解产物为Fe3O4,求Fe2O3的分解率_____ 。
(1)生成I2的物质的量
(2)若分解产物为Fe3O4,求Fe2O3的分解率
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】某红色固体粉末可能是 、
、 或二者混合物,为探究其组成,称取
或二者混合物,为探究其组成,称取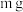 该固体粉末样品,用足量的稀
该固体粉末样品,用足量的稀 充分反应,反应后得到的固体质量为
充分反应,反应后得到的固体质量为 。
。
已知:
(1)若红色固体粉末为纯净物,则
___________ (用含m的最简式表示)。
(2)若 ,计算溶液中
,计算溶液中 与
与 的物质的量之比
的物质的量之比___________ (写出计算过程)。
 、
、 或二者混合物,为探究其组成,称取
或二者混合物,为探究其组成,称取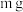 该固体粉末样品,用足量的稀
该固体粉末样品,用足量的稀 充分反应,反应后得到的固体质量为
充分反应,反应后得到的固体质量为 。
。已知:

(1)若红色固体粉末为纯净物,则

(2)若
 ,计算溶液中
,计算溶液中 与
与 的物质的量之比
的物质的量之比
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】铁粉和氧化铁粉末的混合物共13.6g,加入到200mL的稀硫酸中,固体完全溶解,得到标准状况下1.12L 氢气。经测定,反应后的溶液中c (H+) 为0.200mol·L-1,且无Fe3+(忽略反应前后溶液体积变化)。请计算:
(1)原混合物中铁和氧化铁的物质的量之比为_____________ 。
(2)原稀硫酸的物质的量浓度为______________ mol·L-1。
(1)原混合物中铁和氧化铁的物质的量之比为
(2)原稀硫酸的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】请写出简单的计算过程。
(1)在空气中煅烧CoC2O4生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41 g,CO2 体积为1.344 L(标准状况),则钴氧化物的化学式为_____________ 。
(2)将一定量Fe、FeO 和 Fe2O3 的混合物放入25 mL 2 mol·L-1 的HNO3溶液中,反应完全后,无固体剩余,生成 224 mL NO 气体(标准状况),再向反应后的溶液中加入1mol·L-1 的 NaOH 溶液,要使铁元素全部沉淀下来,所加 NaOH 溶液的体积最少是__________________ 。
(3)取Ce(OH)4产品5.000g,加酸溶解后,向其中加入含0.03300molFeSO4的FeSO4溶液使Ce4+全部被还原成Ce3+,再用0.1000mol·L-1的酸性KMnO4标准溶液滴定至终点时,消耗20.00mL标准溶液。则该产品中Ce(OH)4的质量分数为________________ 。(已知氧化性:Ce4+>KMnO4;Ce(OH)4的相对分子质量为208)。
(1)在空气中煅烧CoC2O4生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41 g,CO2 体积为1.344 L(标准状况),则钴氧化物的化学式为
(2)将一定量Fe、FeO 和 Fe2O3 的混合物放入25 mL 2 mol·L-1 的HNO3溶液中,反应完全后,无固体剩余,生成 224 mL NO 气体(标准状况),再向反应后的溶液中加入1mol·L-1 的 NaOH 溶液,要使铁元素全部沉淀下来,所加 NaOH 溶液的体积最少是
(3)取Ce(OH)4产品5.000g,加酸溶解后,向其中加入含0.03300molFeSO4的FeSO4溶液使Ce4+全部被还原成Ce3+,再用0.1000mol·L-1的酸性KMnO4标准溶液滴定至终点时,消耗20.00mL标准溶液。则该产品中Ce(OH)4的质量分数为
您最近一年使用:0次

 )中铁元素的质量分数:取20.0g铁矿石样品,粉碎后加入足量盐酸,充分反应后过滤,向滤液中加入足量氢氧化钠溶液,过滤、洗涤,将所得的沉淀灼烧,冷却后称得固体质量为16.0g。请根据以上信息计算该铁矿石样品中铁元素的质量分数
)中铁元素的质量分数:取20.0g铁矿石样品,粉碎后加入足量盐酸,充分反应后过滤,向滤液中加入足量氢氧化钠溶液,过滤、洗涤,将所得的沉淀灼烧,冷却后称得固体质量为16.0g。请根据以上信息计算该铁矿石样品中铁元素的质量分数

