湖南省2012年高中学生化学竞赛试卷(B卷)
湖南
高二
竞赛
2021-08-04
210次
整体难度:
适中
考查范围:
化学与STSE、竞赛、物质结构与性质、认识化学科学、常见无机物及其应用、化学实验基础、化学反应原理、有机化学基础
一、单选题 添加题型下试题
| A.大力发展火力发电,解决电力紧张问题 |
| B.在屋顶安装太阳能热水器为居民提供生活用热水 |
| C.用石灰对煤燃烧后形成的烟气脱硫,或将煤气化或液化再进行利用 |
| D.用杂草、生活垃圾等有机废弃物发酵产生沼气作家庭燃气 |
| A.金刚石 | B.铝 | C.石墨 | D.铁 |
【知识点】 化学科学对人类文明发展的意义解读
| A.CH4·8H2O | B.CH4 ·7H2O | C.CH4·6H2O | D.CH4·5H2O |
【知识点】 根据晶胞结构确定晶体化学式解读 晶体
( )
| A.3.56 mol/L | B.4.36 mol/L |
| C.5.00 mol/L | D.5.25 mol/L |
A.Na+、SO 、SO 、SO 、K+ 、K+ | B.Na+、Cu2+、Br-、Ba2+ |
C.K+、MnO 、NO 、NO 、Na+ 、Na+ | D.K+、Ca2+、SO 、C1- 、C1- |
【知识点】 限定条件下的离子共存解读
| A.1.8g铵根离子所含的电子数为1.1NA |
| B.1mol乙烷分子中所含共价键数为6 NA |
| C.标准状况下22. 4L乙醇所含的分子数必定为NA |
| D.18.0g重水(D2O)与0.9NA个水分子中所含有的电子数相等 |
【知识点】 阿伏加德罗常数的应用解读

| A.图甲是实验室用大理石与盐酸制取CO2 |
| B.图乙是制取SO2、检验SO2 的漂白性 |
| C.图丙是分离Cl2与KI溶液反应生成的碘 |
| D.图丁是实验室用乙醇和浓硫酸制乙烯 |
【知识点】 二氧化硫的漂白性解读 常见气体的制备与收集解读
| A.①② | B.②③ | C.②③④ | D.①②③④ |
【知识点】 无机综合推断 一元强酸与一元弱酸的比较解读
 =H2O+SO2↑”离子方程式的化学反应最多有
=H2O+SO2↑”离子方程式的化学反应最多有| A.6个 | B.9个 | C.12个 | D.15个 |
| A.将SO2通入少量Ba(NO3)2溶液中: 3SO2 +Ba2+ +NO  +2H2O=BaSO4↓+NO↑+2SO +2H2O=BaSO4↓+NO↑+2SO +4H+ +4H+ |
| B.稀硝酸中加入少量碳酸亚铁:FeCO3 +2H+=Fe2+ +CO2↑+H2O |
| C.硫酸氢铵溶液中滴入足量氢氧化钠溶液: H+ +OH-=H2O |
D.饱和碳酸钠溶液中通入二氧化碳气体: 2Na+ +CO +CO2 +H2O =2NaHCO3↓ +CO2 +H2O =2NaHCO3↓ |
【知识点】 离子方程式的正误判断解读
二、多选题 添加题型下试题
| A.正极反应式:Ag+C1-_ e- =AgCl |
| B.每生成1mol Na2Mn5O10转移2mol电子 |
| C.Na+不断向“水”电池的正极移动 |
| D.AgCl是还原产物 |
三、单选题 添加题型下试题
 2NH3反应,在一定温度下达到平衡时,H2的转化率为25%。若在同一容器中相同温度下充入NH3,欲达到平衡时各成分的百分含量与上述平衡相同,则起始时充入NH3的物质的量和达到平衡时NH3的转化率分别是
2NH3反应,在一定温度下达到平衡时,H2的转化率为25%。若在同一容器中相同温度下充入NH3,欲达到平衡时各成分的百分含量与上述平衡相同,则起始时充入NH3的物质的量和达到平衡时NH3的转化率分别是| A.15mol、25% | B.20mol、50% | C.20mol、75% | D.40mol、80% |
【知识点】 等效平衡理论的综合应用解读 转化率的相关计算及判断解读 化学平衡
四、多选题 添加题型下试题
| A.甲、乙、两、丁四种元素均为短周期元素 |
| B.甲的气态氢化物的稳定性强于乙的气态氢化物 |
| C.甲的含氧酸的酸性弱于丙的含氧酸 |
| D.元素丁形成的化合物比元素乙形成的化合物多 |
【知识点】 元素周期表结构分析解读 元素周期律的应用 元素及其化合物的周期规律
五、单选题 添加题型下试题
 ) 可能为
) 可能为| A.0.45 mol/L | B.0.6 mol/L | C.0.75 mol/L | D.0.9 mol/L |
【知识点】 硝酸的强氧化性解读 Fe、Cu及相关离子的反应解读
六、解答题 添加题型下试题
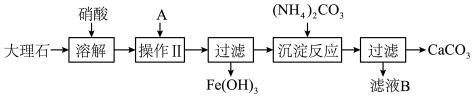
(1)用硝酸溶解大理石时通常控制反应温度不超过70°C,且不使用浓硝酸,原因是
(2)操作II的目的是
(3)写出加入碳酸铵所发生反应的离子方程式
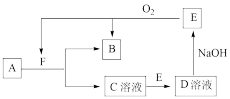
(1)写出它们的化学式:A
(2)在A和F的反应中氧化剂和还原剂的质量比为
(3)A和E能够反应,且产物都为空气的组成成分,请写出该反应的化学方程式:

(1)写出A的化学式
(2)写出下列反应的化学方程式:
反应①:
反应②:
反应③:
反应④:
(3)比较反应①与钠和水反应的现象有什么相同和不同。
相同点:
不同点:
七、填空题 添加题型下试题
(1)反应的离子方程式为
(2)除H+、OH-、H2O外,上述反应后的溶液中一定含有的粒子有_______(填编号)。
| A.Fe2+ | B.Fe3+ | C.Cl- | D.SO | E.H2SO3 |
假设1:只存在Fe3+;
假设2:只存在
假设3:
(4)设计实验方案进行实验。写出实验步骤以及预期现象和结论。
限选实验试剂: 3mol·L-1 H2SO4、l mol·L-1 NaOH、0.01 mol·L-1 KMnO4、20%KSCN、3%H2O2、淀粉- KI溶液、紫色石蕊试液、品红溶液。
| 实验步骤 | 预期现象和结论 |
| 步骤1: | |
| 步骤2: |
八、解答题 添加题型下试题
(1)进行微量实验:如图所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c三个棉球变化如下表。

| 棉球 | 棉球上滴加试剂 | 实验现象 | 解释或结论 |
| a | 棉球变白,微热后又恢复红色 | 解释: 结论:该气体具有漂白性。 | |
| b | 含酚酞的NaOH溶液 | 棉球变为白色 | 离子方程式: |
| c | 棉球变为白色 | 化学方程式: 结论:该气体具有 |

①用此装置模拟工业合成盐酸,则关于试剂选择正确的是
| 溶液A | 固体B | 气体C | |
| a. | 稀硫酸 | Zn | Cl2 |
| b. | 浓盐酸 | MnO2 | H2 |
| c. | 稀硝酸 | Fe | Cl2 |
| d. | 浓盐酸 | KMnO4 | H2 |
九、计算题 添加题型下试题
| tc | 初始 | 2min | 4min | 6min | 8min |
| c(A)(mol·L-1) | 2.50 | 2.20 | 2.00 | 2.00 | 2.20 |
| c(B)(mol·L-1) | 1.56 | 2.16 | 2.56 | 2.56. | 2.16 |
| c(C)(mol·L-1) | 0.39 | 0.54 | 0.64. | 0.64 | 1.54 |
(1)前2min内,v(B)=
(2)6min- 8min若只改变了反应体系中某一种物质的浓度,则应为
a.增大A的浓度 b.减小B的浓度 c.增大C的浓度
则该物质的浓度改变量为
(3)如果在相同条件下,要使该反应从逆反应方向开始进行,且达平衡时与第4min时各物质的物质的量浓度完全相同,则加入B的物质的量浓度的取值范围为
①用水处理此固体,获得60. 2mL气体(在17°C和1.00×105Pa条件下),其中有24. 1mL是氧气,其余的是氙气,水溶液中的XeO3可以氧化30. 0mL。浓度为0. 100 mol/L的Fe2+。
②用KI溶液处理此固体,获得单质碘,此碘需要35.0mL浓度为0.200mol/L的Na2S2O3与之完全反应。
试求:此固体混合物中XeF2和XeF4的物质的量分数
【知识点】 基于氧化还原反应守恒规律的计算解读 氧化还原
试卷分析
试卷题型(共 22题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 化学科学对人类文明发展的意义 能源开发利用新理念 新能源的开发 化学热力学初步 | |
| 2 | 0.65 | 化学科学对人类文明发展的意义 | |
| 3 | 0.65 | 根据晶胞结构确定晶体化学式 晶体 | |
| 4 | 0.65 | 物质的量浓度 物质的量浓度的计算 | |
| 5 | 0.65 | 限定条件下的离子共存 | |
| 6 | 0.65 | 阿伏加德罗常数的应用 | |
| 7 | 0.65 | 二氧化硫的漂白性 常见气体的制备与收集 | |
| 8 | 0.65 | 无机综合推断 一元强酸与一元弱酸的比较 | |
| 9 | 0.85 | 离子方程式的书写 | |
| 10 | 0.65 | 离子方程式的正误判断 | |
| 13 | 0.65 | 等效平衡理论的综合应用 转化率的相关计算及判断 化学平衡 | |
| 15 | 0.4 | 硝酸的强氧化性 Fe、Cu及相关离子的反应 | |
| 二、多选题 | |||
| 11 | 0.65 | 原电池原理 电化学 | |
| 12 | 0.65 | 根据要求书写同分异构体 有机化学 | |
| 14 | 0.65 | 元素周期表结构分析 元素周期律的应用 元素及其化合物的周期规律 | |
| 三、解答题 | |||
| 16 | 0.65 | 硝酸 沉淀的溶解与生成 物质分离、提纯综合应用 金属 | 工业流程题 |
| 17 | 0.65 | 无机综合推断 氨气的结构与性质 二氧化氮 物质成分分析 | 无机推断题 |
| 18 | 0.85 | 乙醇催化氧化 有机物的推断 有机化学 | 有机推断题 |
| 20 | 0.4 | 氯气的制法 二氧化硫的化学性质 综合实验设计与评价 | 实验探究题 |
| 四、填空题 | |||
| 19 | 0.65 | 离子反应在化合物组成的分析、鉴定的应用 铁盐与亚铁盐鉴别试剂的选择 | |
| 五、计算题 | |||
| 21 | 0.65 | 化学平衡的有关计算 化学平衡 | |
| 22 | 0.65 | 基于氧化还原反应守恒规律的计算 氧化还原 | |



