实验室用大理石等原料制取安全无毒的杀菌剂过氧化钙。大理石的主要杂质是氧化铁,以下是提纯大理石的实验步骤:
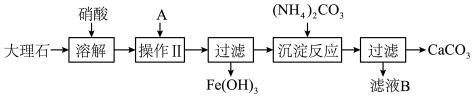
(1)用硝酸溶解大理石时通常控制反应温度不超过70°C,且不使用浓硝酸,原因是___________ 、___________ 。
(2)操作II的目的是___________ ,若A为溶液,则A可以是___________ 。
(3)写出加入碳酸铵所发生反应的离子方程式___________ 。写出滤液B的一种用途:___________ 。

(1)用硝酸溶解大理石时通常控制反应温度不超过70°C,且不使用浓硝酸,原因是
(2)操作II的目的是
(3)写出加入碳酸铵所发生反应的离子方程式
更新时间:2021-08-03 21:06:16
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A—H等8种物质存在如下转化关系下列A~H八种物质存在如下图所示的转化关系(反应条件、部分产物未标出)。已知A是正盐,B能使品红溶液褪色,G是红棕色气体。试回答下列问题:
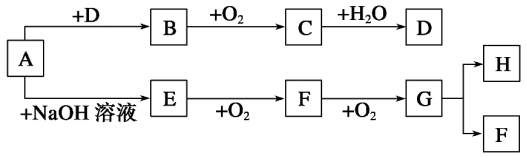
(1)写出下列各物质的化学式:A_______ 、B_______ 。
(2)按要求写出下列反应的有关方程式:
①E→F反应的化学方程式_______ ;
②G→H反应的离子方程式_______ 。
(3)写出H的浓溶液与木炭反应的化学方程式_______ 。
(4)检验D中阴离子的方法是_______ 。
(5)将1.92 g铜粉投入含有0.11molH的溶液中,当铜粉和H恰好完全反应后,产生的气体在标准状况下的体积为_______ mL。

(1)写出下列各物质的化学式:A
(2)按要求写出下列反应的有关方程式:
①E→F反应的化学方程式
②G→H反应的离子方程式
(3)写出H的浓溶液与木炭反应的化学方程式
(4)检验D中阴离子的方法是
(5)将1.92 g铜粉投入含有0.11molH的溶液中,当铜粉和H恰好完全反应后,产生的气体在标准状况下的体积为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】 是常见的汽车尾气催化剂。一种从废
是常见的汽车尾气催化剂。一种从废 纳米催化剂(主要成分及含量:
纳米催化剂(主要成分及含量:
 ,
,
 ,其他杂质
,其他杂质 )中回收金属
)中回收金属 的工艺如图:
的工艺如图:
已知: 能与酸反应,
能与酸反应, 不与酸反应。
不与酸反应。
回答下列问题:
(1)“预处理”时, 经焙烧转化为
经焙烧转化为 ,该操作的主要目的是
,该操作的主要目的是___________ 。
(2)“酸浸”时, 转化为
转化为 ,其离子方程式为
,其离子方程式为___________ 。
(3)“滤液①”和“滤液②”中都含有的主要溶质有___________ (填化学式)。
(4)“粗 ”溶解时,可用稀
”溶解时,可用稀 替代
替代 ,但缺点是
,但缺点是___________ 。
(5)“沉淀”时, 转化为
转化为 沉淀,其化学方程式为
沉淀,其化学方程式为___________ 。
(6)酸性条件下, 能在负载
能在负载 纳米催化剂的电极表面快速转化为
纳米催化剂的电极表面快速转化为 。发生上述转化反应的电极应接电源的
。发生上述转化反应的电极应接电源的___________ 极(填“正”或“负”)。
 是常见的汽车尾气催化剂。一种从废
是常见的汽车尾气催化剂。一种从废 纳米催化剂(主要成分及含量:
纳米催化剂(主要成分及含量:
 ,
,
 ,其他杂质
,其他杂质 )中回收金属
)中回收金属 的工艺如图:
的工艺如图:
已知:
 能与酸反应,
能与酸反应, 不与酸反应。
不与酸反应。回答下列问题:
(1)“预处理”时,
 经焙烧转化为
经焙烧转化为 ,该操作的主要目的是
,该操作的主要目的是(2)“酸浸”时,
 转化为
转化为 ,其离子方程式为
,其离子方程式为(3)“滤液①”和“滤液②”中都含有的主要溶质有
(4)“粗
 ”溶解时,可用稀
”溶解时,可用稀 替代
替代 ,但缺点是
,但缺点是(5)“沉淀”时,
 转化为
转化为 沉淀,其化学方程式为
沉淀,其化学方程式为(6)酸性条件下,
 能在负载
能在负载 纳米催化剂的电极表面快速转化为
纳米催化剂的电极表面快速转化为 。发生上述转化反应的电极应接电源的
。发生上述转化反应的电极应接电源的
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室以废旧磷酸铁锂 电极粉末为原料回收
电极粉末为原料回收 ,其实验过程可表示为
,其实验过程可表示为 磷酸铁锂加入三烧瓶中(装置见下图),滴液漏斗
磷酸铁锂加入三烧瓶中(装置见下图),滴液漏斗 装有
装有 盐酸、
盐酸、 中装有
中装有
 溶液。控制
溶液。控制 ,依次将两种溶液加入三颈烧瓶,充分反应
,依次将两种溶液加入三颈烧瓶,充分反应 后,过滤。
后,过滤。

①实验时应先打开滴液漏斗_______ (填“ ”或“
”或“ ”)。
”)。
②浸出后过滤所得滤渣主要成分为 写出
写出 转化为
转化为 的离子方程式:
的离子方程式:_______ 。
③控制原料 锂的浸出率为
锂的浸出率为 若提高盐酸用量,可使锂浸出率达
若提高盐酸用量,可使锂浸出率达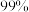 以上,但同时可能存在的缺陷有
以上,但同时可能存在的缺陷有_______ 。
(2)用碳酸钠作沉淀剂从浸出液中回收碳酸锂。有同学建议用“侯氏制碱法”的原理制备 查阅资料发现文献对常温下的
查阅资料发现文献对常温下的 有不同的描述:
有不同的描述:
i.白色固体。ii.尚未从溶液中分离出来。
为探究 的性质,将饱和
的性质,将饱和 溶液与饱和
溶液与饱和 溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。
溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。
①上述现象说明,在该实验条件下
_______ (填“稳定”或“不稳定”)。
②实验中发生反应的离子方程式为_______ 。
(3)盐湖提盐后的浓缩卤水(含 和少量
和少量 )也常用作制备
)也常用作制备 的重要原料。已知:常温时
的重要原料。已知:常温时 的溶解度为:
的溶解度为:
 的溶解度曲线如下图所示。
的溶解度曲线如下图所示。 请补充完整实验方案:向浓缩卤水中边搅拌边缓慢添加石灰乳,
请补充完整实验方案:向浓缩卤水中边搅拌边缓慢添加石灰乳,_______ ,洗涤,低温烘干。 完全沉淀
完全沉淀 可选用的试剂:饱和
可选用的试剂:饱和 溶液、饱和
溶液、饱和 溶液、
溶液、 固体、蒸馏水]。
固体、蒸馏水]。
 电极粉末为原料回收
电极粉末为原料回收 ,其实验过程可表示为
,其实验过程可表示为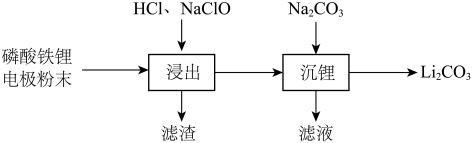
 磷酸铁锂加入三烧瓶中(装置见下图),滴液漏斗
磷酸铁锂加入三烧瓶中(装置见下图),滴液漏斗 装有
装有 盐酸、
盐酸、 中装有
中装有
 溶液。控制
溶液。控制 ,依次将两种溶液加入三颈烧瓶,充分反应
,依次将两种溶液加入三颈烧瓶,充分反应 后,过滤。
后,过滤。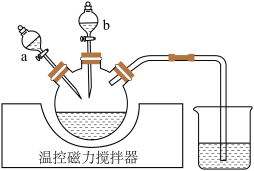


①实验时应先打开滴液漏斗
 ”或“
”或“ ”)。
”)。②浸出后过滤所得滤渣主要成分为
 写出
写出 转化为
转化为 的离子方程式:
的离子方程式:③控制原料
 锂的浸出率为
锂的浸出率为 若提高盐酸用量,可使锂浸出率达
若提高盐酸用量,可使锂浸出率达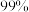 以上,但同时可能存在的缺陷有
以上,但同时可能存在的缺陷有(2)用碳酸钠作沉淀剂从浸出液中回收碳酸锂。有同学建议用“侯氏制碱法”的原理制备
 查阅资料发现文献对常温下的
查阅资料发现文献对常温下的 有不同的描述:
有不同的描述:i.白色固体。ii.尚未从溶液中分离出来。
为探究
 的性质,将饱和
的性质,将饱和 溶液与饱和
溶液与饱和 溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。
溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。①上述现象说明,在该实验条件下

②实验中发生反应的离子方程式为
(3)盐湖提盐后的浓缩卤水(含
 和少量
和少量 )也常用作制备
)也常用作制备 的重要原料。已知:常温时
的重要原料。已知:常温时 的溶解度为:
的溶解度为:
 的溶解度曲线如下图所示。
的溶解度曲线如下图所示。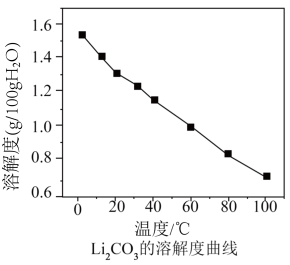
 请补充完整实验方案:向浓缩卤水中边搅拌边缓慢添加石灰乳,
请补充完整实验方案:向浓缩卤水中边搅拌边缓慢添加石灰乳, 完全沉淀
完全沉淀 可选用的试剂:饱和
可选用的试剂:饱和 溶液、饱和
溶液、饱和 溶液、
溶液、 固体、蒸馏水]。
固体、蒸馏水]。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】氯氧化铋(BiOCl)广泛用于彩釉调料、塑料助剂、油漆调色、金属铋生产中,副产品 NaBiO3可作测定锰的氧化剂。工业上常用辉铋矿(主要成分是Bi2S3,还含有少量SiO2 等杂质),制备BiOCl和 NaBiO3(二者都难溶于水),其流程如图:

(1)操作 a 使用的玻璃仪器是_____ ,工业上制备 HCl 的反应原理是:_____ 。
(2)滤渣 I 中的成分为_____ ,分离滤渣 I 中的成分的物理方法是:_____ 。
(3)加入 H2O2 发生反应的离子方程式_____ 。
(4)请从平衡角度解释调 pH 产生滤渣Ⅱ的原因:_____ 。
(5)混合液 II 中加入 Na2CO3粉末,当混合液Ⅱ中_____ (填实验现象)时,说明 BiOCl 的生成已完成。
(6)混合液 II 中加入 NaOH 和 NaClO 发生的离子方程式_____ 。

(1)操作 a 使用的玻璃仪器是
(2)滤渣 I 中的成分为
(3)加入 H2O2 发生反应的离子方程式
(4)请从平衡角度解释调 pH 产生滤渣Ⅱ的原因:
(5)混合液 II 中加入 Na2CO3粉末,当混合液Ⅱ中
(6)混合液 II 中加入 NaOH 和 NaClO 发生的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】以电石渣为主要原料,实现了废物的资源化利用,有较高的应用价值,电石渣呈灰色,并伴有刺鼻的气味,以电石渣[主要成分为Ca(OH)2,含少量MgO,SiO2,Al2O3,碳渣等杂质]为原料制备高纯活性纳米CaCO3的流程如图:
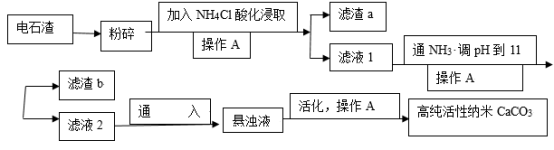
(1)操作A的名称是____ ,加入NH4Cl可以酸化溶液,请用离子方程式来表示可以酸化的原因___
(2)滤渣a中含有___ ,向滤液1中通入NH3调节溶液pH,主要目的是:①使滤液2能吸收更多CO2,②___ 。写出通入CO2生成悬浊液的化学方程式____ 。
(3)流程中可循环利用的物质是___ 和___ 。
(4)电石渣在运输、贮存过程中避免与___ 物质接触。高纯活性纳米CaCO3在生产生活中可用于油墨和造纸等工业的填料,也可用于化妆品、儿童牙膏等日化产品。请写出你知道的CaCO3的其他用途__ (任写两点)。

| 物质 | 开始沉淀pH | 完全沉淀pH |
| Mg(OH)2 | 9.8 | 10.8 |
| Al(OH)3 | 3.2 | 4.7 |
(1)操作A的名称是
(2)滤渣a中含有
(3)流程中可循环利用的物质是
(4)电石渣在运输、贮存过程中避免与
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70%Cu、25%Al、4%Fe 及少量Au、Pt 的合金,并设计出由合金制备硫酸铜和硫酸铝晶体的路线:
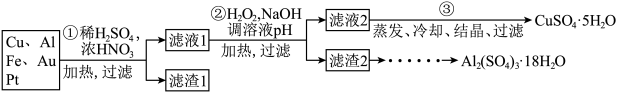
请回答下列问题:
(1)第①步Cu与酸反应的离子方程式___________________ ,得到滤渣1的主要成分为_________ 。
(2)第②步加H2O2的作用是做氧化剂,将溶液中的Fe2+离子氧化为Fe3+,写出该反应的离子方程式_______________________________ ,用H2O2做氧化的优点是__________________ 。
(3)滤渣2的主要成分中Al(OH)3和Fe(OH)3在生产中如何分离两种沉淀,写出反应的离子方程式:_____________________________________________ 。

请回答下列问题:
(1)第①步Cu与酸反应的离子方程式
(2)第②步加H2O2的作用是做氧化剂,将溶液中的Fe2+离子氧化为Fe3+,写出该反应的离子方程式
(3)滤渣2的主要成分中Al(OH)3和Fe(OH)3在生产中如何分离两种沉淀,写出反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】湿法冶炼脆硫铅锑矿(主要成分为Pb4FeSb6S14)制取锑白(Sb2O3)的工艺流程如下图所示。
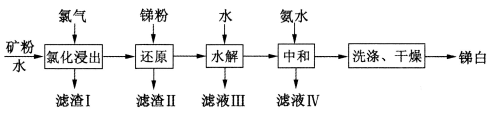
已知:①锑(Sb)为VA族元素,Sb2O3为两性氧化物
②“水解”时锑元素转化为SbOC1沉淀
回答下列问题:
(1)“氯化浸出”后的滤液中含有两种锑的氯化物,分别为SbCl3和_______ 和(填化学式)。滤渣I中所含的反应产物有PbCl2和一种单质,该单质是_______ 。
(2)“还原”是用锑粉还原高价金属离子。其中,Sb将Fe3+转化为Fe2+的离子方程式为_______ ,该转化有利于“水解”时锑铁分离。
(3)滤液Ⅳ的成分是_______ (填化学式)。“中和”时若用NaOH溶液代替氨水,Sb2O3可能会转化为_______ (填离子符号),使锑白的产量降低。
(4)锑白也可用火法冶炼脆硫铅锑矿制取,该法中有焙烧、烧结、还原和吹炼等生产环节。与火法冶炼相比,湿法冶炼的优点有_______ (任写一点)。

已知:①锑(Sb)为VA族元素,Sb2O3为两性氧化物
②“水解”时锑元素转化为SbOC1沉淀
回答下列问题:
(1)“氯化浸出”后的滤液中含有两种锑的氯化物,分别为SbCl3和
(2)“还原”是用锑粉还原高价金属离子。其中,Sb将Fe3+转化为Fe2+的离子方程式为
(3)滤液Ⅳ的成分是
(4)锑白也可用火法冶炼脆硫铅锑矿制取,该法中有焙烧、烧结、还原和吹炼等生产环节。与火法冶炼相比,湿法冶炼的优点有
您最近一年使用:0次
【推荐3】硫酸铜可用作家禽养殖饲料的添加剂。一种以含砷氧化铜矿[含CuO、Cu(OH)2·CuCO3、砷的化合物及铅的化合物]为原料制备饲料级硫酸铜的工艺流程如图所示。回答下列问题:
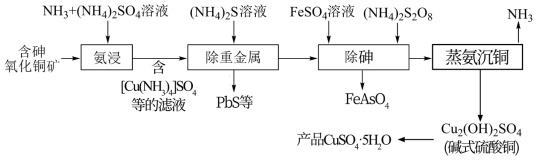
(1)“氨浸”时控制温度为45℃,液固比为1:4,c(NH3)+c(NH )=1 mol·L-1且c(NH3)=c(NH
)=1 mol·L-1且c(NH3)=c(NH )。
)。
①温度不宜超过55℃,这是因为___ 。
②“氨浸”时,Cu(OH)2·CuCO3转化为[Cu(NH3)4]SO4和NH4HCO3的化学方程式为__ 。
③溶液中Cu2+、[Cu(NH3)n]2+(n=1~4)的物质的量分数δ(x)与lgc(NH3)的关系如图所示。
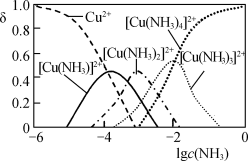
lgc(NH3)=-3时,浓度最大的含铜微粒是__ ,lgc(NH3)由-1→0时,发生反应的离子方程式为__ 。
(2)“除砷”时控制pH=9,AsO 最终转化为FeAsO4沉淀,AsO
最终转化为FeAsO4沉淀,AsO 中As的化合价为
中As的化合价为__ ,该转化过程中每生成1 mol FeAsO4,转移__ mol电子。
(3)“蒸氨沉铜”的尾气可返回__ 工序循环使用,由碱式硫酸铜制取产品硫酸铜晶体的方法:将碱式硫酸铜先溶于硫酸,再__ 、洗涤、干燥。

(1)“氨浸”时控制温度为45℃,液固比为1:4,c(NH3)+c(NH
 )=1 mol·L-1且c(NH3)=c(NH
)=1 mol·L-1且c(NH3)=c(NH )。
)。①温度不宜超过55℃,这是因为
②“氨浸”时,Cu(OH)2·CuCO3转化为[Cu(NH3)4]SO4和NH4HCO3的化学方程式为
③溶液中Cu2+、[Cu(NH3)n]2+(n=1~4)的物质的量分数δ(x)与lgc(NH3)的关系如图所示。

lgc(NH3)=-3时,浓度最大的含铜微粒是
(2)“除砷”时控制pH=9,AsO
 最终转化为FeAsO4沉淀,AsO
最终转化为FeAsO4沉淀,AsO 中As的化合价为
中As的化合价为(3)“蒸氨沉铜”的尾气可返回
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】某不活泼金属X在氯气中燃烧的产物Y溶于盐酸得黄色溶液,蒸发结晶,得到黄色晶体Z,其中X的质量分数为50%。在500mL浓度为0.10mol/L的Y水溶液中投入锌片,反应结束时固体的质量比反应前增加4.95g。则X是_______ ;Y是_______ ;Z是_______ 。推理过程如下:_______ 。
您最近一年使用:0次
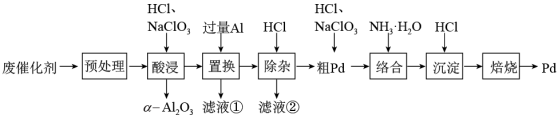
【推荐2】钯(Pd)是一种不活泼金属,性质与铂相似。含钯催化剂不仅在科研和工业生产中用途广泛,而且用量大,因此从废催化剂中回收钯具有巨大的经济效益。已知某废催化剂的主要成分是钯和活性炭,还含有少量铁、镁、铝、硅、铜等杂质元素,提取海绵钯的工艺流程如下:
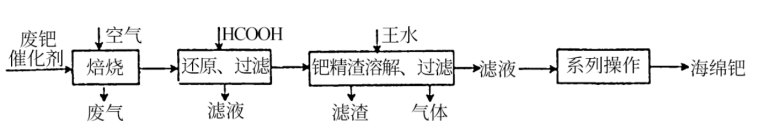
(1)Pd的价电子排布式为4d10,指出它在元素周期表中的位置_______ 。
(2)“焙烧”步骤中,通入的空气一定要足量,理由是_______ 。
(3)写出甲酸还原过程发生反应的化学方程式_______ 。
(4)钯在王水中溶解生成化合物X(由3种元素组成)、种无色有毒的气体Y和水。
①如何配置王水_______ 。
②写出钯与王水反应的化学方程式_______ 。
(5)金属钯具有显著的吸氢性能,其密度为12.0g·cm-3。
①在标准状况下,海绵钯吸收氢气的体积约为其体积的840倍,求海绵钯的吸附容量R=_______ (mL·g-1)、氢气的浓度r=_______ (1molPd吸收氢气的物质的量)。
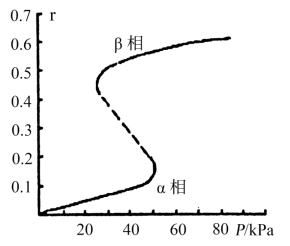
②金属钯中,氢气的r与压强之间的变化关系如图所示,试解释该图的变化趋势_______ 。
(相对原子质量:Pd106.4,理想气体常数R=8.314J·mol-l·K-1)

(1)Pd的价电子排布式为4d10,指出它在元素周期表中的位置
(2)“焙烧”步骤中,通入的空气一定要足量,理由是
(3)写出甲酸还原过程发生反应的化学方程式
(4)钯在王水中溶解生成化合物X(由3种元素组成)、种无色有毒的气体Y和水。
①如何配置王水
②写出钯与王水反应的化学方程式
(5)金属钯具有显著的吸氢性能,其密度为12.0g·cm-3。
①在标准状况下,海绵钯吸收氢气的体积约为其体积的840倍,求海绵钯的吸附容量R=
②金属钯中,氢气的r与压强之间的变化关系如图所示,试解释该图的变化趋势

(相对原子质量:Pd106.4,理想气体常数R=8.314J·mol-l·K-1)
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
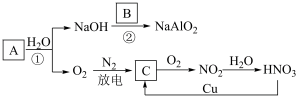
【推荐3】已知A、B均是由两种短周期元素组成的化合物,A中某元素的质量分数为25% ,B的焰色反应呈黄色,C、J、X是同周期的元素的氢化物,X为无色液体,C、J为气体,D是一种不溶于水的白色固体。在一定条件下,它们有如图所示的转化关系。
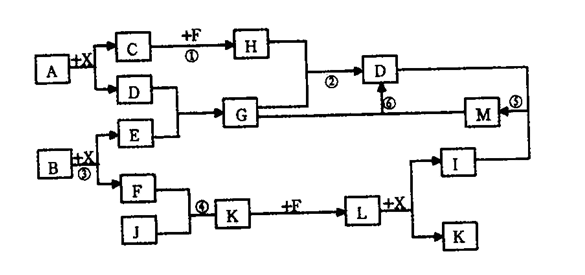
试回答下列问题:
(1)写出化学式:A_______ ,E_______ ,L_______ 。
(2)在反应①~⑥中,属于氧化还原反应的是_______ 。
(3)反应③的化学方程式为_______ 。
(4)写出下列离子反应方程式:
反应②_______ ;
反应⑥_______ 。
(5)将3.4gJ气体与足量的F反应,生成 一种单质和X,恢复到25°C放出a kJ热量,写出该反应的热化学方程式:_______ 。

试回答下列问题:
(1)写出化学式:A
(2)在反应①~⑥中,属于氧化还原反应的是
(3)反应③的化学方程式为
(4)写出下列离子反应方程式:
反应②
反应⑥
(5)将3.4gJ气体与足量的F反应,生成 一种单质和X,恢复到25°C放出a kJ热量,写出该反应的热化学方程式:
您最近一年使用:0次