(1)0.2molNH3的质量为_______ g
(2)配制250mL1.0mol/LH2SO4溶液,需要18mol/LH2SO4溶液体积是___ 。
(3)我国古代四大发明之一的黑火药是由硫粉、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C=K2S+N2↑+3CO2↑,反应中被还原的物质是____ (填化学式);1mol硫参加反应时转移电子数为_____ 。
(4)已知NH3和Cl2可以发生氧化还原反应,配平该方程式:NH3+Cl2=N2+HCl,_______ 。
(2)配制250mL1.0mol/LH2SO4溶液,需要18mol/LH2SO4溶液体积是
(3)我国古代四大发明之一的黑火药是由硫粉、硝酸钾和木炭按一定比例混合而成,爆炸时的反应为S+2KNO3+3C=K2S+N2↑+3CO2↑,反应中被还原的物质是
(4)已知NH3和Cl2可以发生氧化还原反应,配平该方程式:NH3+Cl2=N2+HCl,
更新时间:2021-06-14 10:02:15
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】(1)分子数为0.5NA的CO2的质量是______ g。
(2)在标准状况下,由CO和CO2组成的混合气体4.48L,质量是8g,此混合气体的平均摩尔质量是______ 。
(2)在标准状况下,由CO和CO2组成的混合气体4.48L,质量是8g,此混合气体的平均摩尔质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】在反应X+2Y=R+2M中,已知R、M的摩尔质量之比为22:9。当1.6gX与Y完全反应后,生成4.4gR,则在此反应中,Y、M的质量之比为________
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】(1)从500 mL 0.2 mol/L Na2SO4 溶液中取出10 mL,取出的Na2SO4溶液物质的量浓度为________ mol/L;若将这10 mL溶液用水稀释到100 mL,所得溶液中Na+的物质的量浓度为______ mol/L。
(2)标准状况下,2.4g某气体的体积为672 mL,则此气体的相对分子质量为________ 。
(3)在标准状况下,V L HCl溶于1 L水中,所得溶液的密度为ρg·cm-3,则此溶液的物质的量浓度为:______________ mol/L
(2)标准状况下,2.4g某气体的体积为672 mL,则此气体的相对分子质量为
(3)在标准状况下,V L HCl溶于1 L水中,所得溶液的密度为ρg·cm-3,则此溶液的物质的量浓度为:
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】下图为实验室某浓盐酸试剂瓶上的标签的有关内容。试根据标签上的有关数据回答下列问题:

(1)该浓盐酸中HCl的物质的量浓度为_______________ 。
(2)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400 mol·L-1的稀盐酸,需要量取上述___________ mL浓盐酸进行配制。

(1)该浓盐酸中HCl的物质的量浓度为
(2)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400 mol·L-1的稀盐酸,需要量取上述
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】氮氧化物进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾,因此必须对含有氮氧化物的废气进行处理。
(1)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH=2NaNO2+H2O ①
2NO2+2NaOH=NaNO2+NaNO3+H2O ②
在反应①中,氧化剂是___ ,还原剂是___ 。在反应②中,氧化剂是__ ,还原剂是__ 。
(2)汽车尾气中含有二氧化氮和一氧化碳,消除这两种物质对大气污染的方法是安装催化转化器,使它们发生反应生成氮气和二氧化碳,该反应的化学方程式为___ 。
(3)氨气亦可用来处理氮氧化物。例如,氨气与二氧化氮发生如下反应:6NO2+8NH3=7N2+12H2O。若某工厂排出的尾气中二氧化氮含量为0.5%(体积分数),处理1×103m3(标准状况)这种尾气,需要多少千克氨气___ ?
(1)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH=2NaNO2+H2O ①
2NO2+2NaOH=NaNO2+NaNO3+H2O ②
在反应①中,氧化剂是
(2)汽车尾气中含有二氧化氮和一氧化碳,消除这两种物质对大气污染的方法是安装催化转化器,使它们发生反应生成氮气和二氧化碳,该反应的化学方程式为
(3)氨气亦可用来处理氮氧化物。例如,氨气与二氧化氮发生如下反应:6NO2+8NH3=7N2+12H2O。若某工厂排出的尾气中二氧化氮含量为0.5%(体积分数),处理1×103m3(标准状况)这种尾气,需要多少千克氨气
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】Ⅰ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,该反应中Na2O2 是___________ (填氧化剂、还原剂)
(2)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:__________________ 。
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为__________ mol。
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是______ 。
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+、Br-完全被氧化时,c=__________ (用含a、b的代数式表示)。
(1)干法制备高铁酸钠的主要反应为:2FeSO4 + 6 Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,该反应中Na2O2 是
(2)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为
Ⅱ.已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此时被氧化的离子是
(2)若向含a mol FeI2和b mol FeBr2的溶液中通入c mol Cl2,当I-、Fe2+、Br-完全被氧化时,c=
您最近一年使用:0次
【推荐3】过氧化氢溶液俗称双氧水,有杀菌消毒的作用,医疗上常用它来清洗伤口。双氧水有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称。
(1)配平下列化学反应,并用单线桥表示电子转移的方向和数目:____________ 。


(2)要消除采矿业胶液中的氰化物(如KCN,C为+2价),可经反应
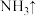 实现,A的化学式为
实现,A的化学式为_______ ,若此反应中有6.72 L(标准状况)气体生成,则转移电子的数目为_______ (用NA表示)。
(3)高锰酸钾也可用于医疗杀菌消毒。根据反应条件可判断氧化剂氧化能力的强弱。例如:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,则MnO2和KMnO4相比,
MnCl2+Cl2↑+2H2O,2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,则MnO2和KMnO4相比,__________ (填化学式)的氧化性强。某强酸性反应体系中,反应物和产物共六种粒子: 、
、 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 只发生了如下过程:
只发生了如下过程: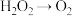 ,则该反应中发生还原反应的过程是
,则该反应中发生还原反应的过程是__________ →__________ ,该反应应选择的酸是__________ (填字母)。
A.盐酸 B.醋酸 C.稀硫酸
(4)用32 mL 0.2 mol/L 溶液,还原含4×10-3 mol
溶液,还原含4×10-3 mol 的溶液,过量的Na2SO3用0.2 mol/L酸性KMnO4溶液氧化(其中KMnO4被还原成Mn2+),共消耗0.8 mL酸性KMnO4溶液,则元素X在还原产物中的化合价是
的溶液,过量的Na2SO3用0.2 mol/L酸性KMnO4溶液氧化(其中KMnO4被还原成Mn2+),共消耗0.8 mL酸性KMnO4溶液,则元素X在还原产物中的化合价是______ (填字母)。
A.+1 B.+2 C.+3 D.+4
(1)配平下列化学反应,并用单线桥表示电子转移的方向和数目:


(2)要消除采矿业胶液中的氰化物(如KCN,C为+2价),可经反应

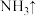 实现,A的化学式为
实现,A的化学式为(3)高锰酸钾也可用于医疗杀菌消毒。根据反应条件可判断氧化剂氧化能力的强弱。例如:MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O,2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,则MnO2和KMnO4相比,
MnCl2+Cl2↑+2H2O,2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,则MnO2和KMnO4相比, 、
、 、
、 、
、 、
、 、
、 。已知该反应中
。已知该反应中 只发生了如下过程:
只发生了如下过程: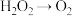 ,则该反应中发生还原反应的过程是
,则该反应中发生还原反应的过程是A.盐酸 B.醋酸 C.稀硫酸
(4)用32 mL 0.2 mol/L
 溶液,还原含4×10-3 mol
溶液,还原含4×10-3 mol 的溶液,过量的Na2SO3用0.2 mol/L酸性KMnO4溶液氧化(其中KMnO4被还原成Mn2+),共消耗0.8 mL酸性KMnO4溶液,则元素X在还原产物中的化合价是
的溶液,过量的Na2SO3用0.2 mol/L酸性KMnO4溶液氧化(其中KMnO4被还原成Mn2+),共消耗0.8 mL酸性KMnO4溶液,则元素X在还原产物中的化合价是A.+1 B.+2 C.+3 D.+4
您最近一年使用:0次
【推荐1】实验室常用KMnO4与浓盐酸反应来制备氯气:2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O,在此反应中:
(1)氧化剂是______ ,氧化产物是______ 。(填化学式)
(2)氧化剂与还原剂的物质的量之比为______ 。
(3)若生成71 g Cl2,则消耗的HCl是______ mol,被氧化的HCl是______ mol,转移的电子的物质的量是______ mol。
(4)将此反应改写成离子方程式______ 。
(1)氧化剂是
(2)氧化剂与还原剂的物质的量之比为
(3)若生成71 g Cl2,则消耗的HCl是
(4)将此反应改写成离子方程式
您最近一年使用:0次
【推荐2】饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: 。请回答下列问题:
。请回答下列问题:
(1)上述反应中,被氧化的元素是___________ ,还原产物是___________ 。
(2)用“双线桥法”表示反应中电子转移的方向和数目:___________ 。

(3)反应中每生成1个 ,转移
,转移___________ 个电子。
(4)请配平下列离子方程式:___________ 。
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________
(5)已知 、
、 、
、 、
、 、
、 均有还原性,它们在酸性溶液中还原性的强弱顺序为:
均有还原性,它们在酸性溶液中还原性的强弱顺序为: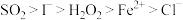 ,则下列反应不能发生的是:___________。
,则下列反应不能发生的是:___________。
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: 。请回答下列问题:
。请回答下列问题:(1)上述反应中,被氧化的元素是
(2)用“双线桥法”表示反应中电子转移的方向和数目:

(3)反应中每生成1个
 ,转移
,转移(4)请配平下列离子方程式:
___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________
(5)已知
 、
、 、
、 、
、 、
、 均有还原性,它们在酸性溶液中还原性的强弱顺序为:
均有还原性,它们在酸性溶液中还原性的强弱顺序为: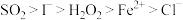 ,则下列反应不能发生的是:___________。
,则下列反应不能发生的是:___________。A.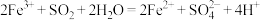 |
B. |
C.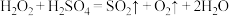 |
D. |
您最近一年使用:0次
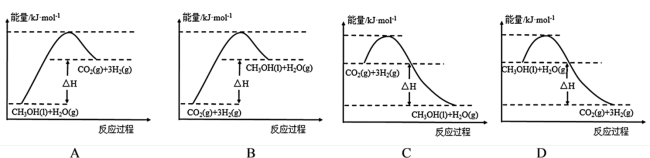
【推荐3】CO2的减排、捕集和利用是人类可持续发展的重要战略之一。利用CO2和H2生成CH3OH来捕集CO2的反应是CO2(g)+3H2(g) CH3OH(l)+H2O(g) △H=-89 kJ·mol-1,回答下列问题:
CH3OH(l)+H2O(g) △H=-89 kJ·mol-1,回答下列问题:
(1)下列有关上述反应的图象合理的是__________ (填标号)。
(2)①某温度下,向某恒容密闭容器中充入0.1 mol CO2(g)和0.3 mol H2(g),充分反应后,放出的热量__________ (填“>”“<”或“=”)8.9 kJ。
②完全燃烧1.6 g甲醇所消耗氧气的物质的量为________ ,转移的电子数为________ NA。
(3)某温度下,将定量的CO2(g)和H2(g)充入2 L恒容密用容器中,经过10 min后,反应达到平衡,图得CO2为0.5 mol、H2为1.2 mol、H2O为0.3 mol。则该条件下达到平衡时CO2的转化率为__________ %,氢气的体积分数ω(H2)=__________ %。
 CH3OH(l)+H2O(g) △H=-89 kJ·mol-1,回答下列问题:
CH3OH(l)+H2O(g) △H=-89 kJ·mol-1,回答下列问题:(1)下列有关上述反应的图象合理的是

(2)①某温度下,向某恒容密闭容器中充入0.1 mol CO2(g)和0.3 mol H2(g),充分反应后,放出的热量
②完全燃烧1.6 g甲醇所消耗氧气的物质的量为
(3)某温度下,将定量的CO2(g)和H2(g)充入2 L恒容密用容器中,经过10 min后,反应达到平衡,图得CO2为0.5 mol、H2为1.2 mol、H2O为0.3 mol。则该条件下达到平衡时CO2的转化率为
您最近一年使用:0次




