实验室常用KMnO4与浓盐酸反应来制备氯气:2KMnO4+16HCl=2MnCl2+2KCl+5Cl2↑+8H2O,在此反应中:
(1)氧化剂是______ ,氧化产物是______ 。(填化学式)
(2)氧化剂与还原剂的物质的量之比为______ 。
(3)若生成71 g Cl2,则消耗的HCl是______ mol,被氧化的HCl是______ mol,转移的电子的物质的量是______ mol。
(4)将此反应改写成离子方程式______ 。
(1)氧化剂是
(2)氧化剂与还原剂的物质的量之比为
(3)若生成71 g Cl2,则消耗的HCl是
(4)将此反应改写成离子方程式
更新时间:2021-03-02 18:24:35
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】(1)取300mL 0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的 I2和 KIO3,则消耗 KMnO4的物质的量的是______ mol。
(2)在 Fe(NO3)3 溶液中加入 Na2SO3 溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是________ ,又变为棕黄色的原因是用离子方程式解释___________________________ .
(3)在 100mLFeBr2 溶液中通入标况下2.24LCl2,溶液溶液中有1/4的Br- 被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为_________________ 。
(4)将Al、Al2O3和Al(OH)3的混合物恰好与NaOH溶液反应,反应后溶液中溶质的化学式_________ 。向反应后的溶液中通入过量CO2,反应的离子方程式为 ______ 。
(5)三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式___________ ,反应中生成0.2mol HNO3,转移的电子数目为_______ 。
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是________
(2)在 Fe(NO3)3 溶液中加入 Na2SO3 溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是
(3)在 100mLFeBr2 溶液中通入标况下2.24LCl2,溶液溶液中有1/4的Br- 被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为
(4)将Al、Al2O3和Al(OH)3的混合物恰好与NaOH溶液反应,反应后溶液中溶质的化学式
(5)三氟化氮(NF3)是一种无色,无味的气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,请根据要求回答下列问题:
①写出该反应的化学方程式
②NF3无色、无臭,但一旦在空气中泄漏,还是易于发现,判断该气体泄漏时的现象是
您最近一年使用:0次
【推荐2】分类法是进行化学研究的重要方法。不同的标准可以把物质和反应分为不同的类别。回答下列问题:
(1)现有九种物质:①铜;②小苏打;③硫酸铁;④二氧化碳;⑤葡萄糖;⑥熔融氯化钠;⑦氢氧化铁胶体;⑧浓硫酸;⑨液氨;上述物质中,属于能导电的纯净物是___________ (填序号);属于非电解质的是___________ (填序号);③在水中的电离方程式为___________ 。
(2)下列物质属于如图所示化学概念交叉部分(阴影部分)的是___________ (填标号)。

A. B.HCl C.
B.HCl C. (乙醇) D.NaCl E.Hg
(乙醇) D.NaCl E.Hg
(3)氧化还原反应是一类重要化学反应,在生产生活中有重要应用。
①工业上,用 溶液“腐蚀”覆铜板制作印刷电路板,写出对应的离子方程式
溶液“腐蚀”覆铜板制作印刷电路板,写出对应的离子方程式___________ 。
②完善下面的化学方程式,并配平___________ 。

③利用盐酸酸化淀粉的KI溶液检验食盐中的碘元素( )。写出发生反应的离子方程式
)。写出发生反应的离子方程式___________ 。
(4)在20.00ml 溶液中加入0.195g锌粉,恰好完全反应,则还原产物可能是___________
溶液中加入0.195g锌粉,恰好完全反应,则还原产物可能是___________
(1)现有九种物质:①铜;②小苏打;③硫酸铁;④二氧化碳;⑤葡萄糖;⑥熔融氯化钠;⑦氢氧化铁胶体;⑧浓硫酸;⑨液氨;上述物质中,属于能导电的纯净物是
(2)下列物质属于如图所示化学概念交叉部分(阴影部分)的是

A.
 B.HCl C.
B.HCl C. (乙醇) D.NaCl E.Hg
(乙醇) D.NaCl E.Hg(3)氧化还原反应是一类重要化学反应,在生产生活中有重要应用。
①工业上,用
 溶液“腐蚀”覆铜板制作印刷电路板,写出对应的离子方程式
溶液“腐蚀”覆铜板制作印刷电路板,写出对应的离子方程式②完善下面的化学方程式,并配平

③利用盐酸酸化淀粉的KI溶液检验食盐中的碘元素(
 )。写出发生反应的离子方程式
)。写出发生反应的离子方程式(4)在20.00ml
 溶液中加入0.195g锌粉,恰好完全反应,则还原产物可能是___________
溶液中加入0.195g锌粉,恰好完全反应,则还原产物可能是___________A. | B. | C. | D.V |
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】铜与浓硝酸反应的方程式为:
(1)在该反应中,被还原的元素是_______ ,氧化产物是_______ 。
(2)在方程式标出电子转移的方向和数目_______ 。
(3)若有32g铜参与反应,被还原的硝酸有_______ mol。

(1)在该反应中,被还原的元素是
(2)在方程式标出电子转移的方向和数目
(3)若有32g铜参与反应,被还原的硝酸有
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)在反应2KMnO4+16HBr=5Br2+2MnBr2+2KBr+8H2O中,还原剂是 。
(2)浓盐酸在反应___KClO3+___HCl→___KCl+___ClO2+___Cl2+___ ____ (补充完整此项化学式及化学计量数)中显示出来的性质是 。
(3)在一定条件下,PbO2与Cr3+反应,产物是Cr2O72-和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为 。
(2)浓盐酸在反应___KClO3+___HCl→___KCl+___ClO2+___Cl2+___ ____ (补充完整此项化学式及化学计量数)中显示出来的性质是 。
(3)在一定条件下,PbO2与Cr3+反应,产物是Cr2O72-和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】将10 g铁置于40 mL某浓度的硝酸中,再微热充分反应后,共收集到1792 mL混合气体,溶液里还残留4.4 g固体(标准状况)。求:
(1)反应被还原的硝酸与未被还原的硝酸的物质的量
(2)原硝酸溶液的物质的量浓度
(3)混合气体的组成成分及其体积比
(1)反应被还原的硝酸与未被还原的硝酸的物质的量
(2)原硝酸溶液的物质的量浓度
(3)混合气体的组成成分及其体积比
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】硝酸铵是一种常用的化肥,其工业生产流程如图,请回答下列问题。
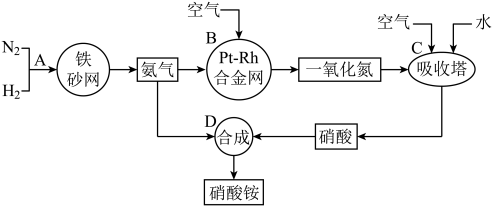
(1)写出反应容器B中发生反应的化学方程式:____ 。
(2)吸收塔C中通入空气的目的是___ ;C、D两个反应容器中发生的反应,属于氧化还原反应的是___ (填反应容器代号)。
(3)浓硝酸一般保存在棕色试剂瓶里,并放置在阴凉处,用化学方程式解释原因:___ 。
(4)碳与浓硝酸反应的化学方程式是_____ 。
(5)将128g铜置于一定量的浓硝酸中并微热。当铜片完全消失时,共收集到NO2和NO的混合气体44.8L(标准状况)。
①写出上述过程中,有关反应的离子方程式:____ 、____ 。
②完成该反应至少需要量取10mol·L-1的浓硝酸_____ mL。
③混合气体中NO2的体积为____ L,NO的体积为____ L(均为标准状况下)。
④将收集上述气体的容器倒扣在盛有水的水槽中,并向其中缓慢通入O2使其充分反应,若要使溶液恰好充满容器,则理论上需要参加反应的O2的物质的量为____ mol。

(1)写出反应容器B中发生反应的化学方程式:
(2)吸收塔C中通入空气的目的是
(3)浓硝酸一般保存在棕色试剂瓶里,并放置在阴凉处,用化学方程式解释原因:
(4)碳与浓硝酸反应的化学方程式是
(5)将128g铜置于一定量的浓硝酸中并微热。当铜片完全消失时,共收集到NO2和NO的混合气体44.8L(标准状况)。
①写出上述过程中,有关反应的离子方程式:
②完成该反应至少需要量取10mol·L-1的浓硝酸
③混合气体中NO2的体积为
④将收集上述气体的容器倒扣在盛有水的水槽中,并向其中缓慢通入O2使其充分反应,若要使溶液恰好充满容器,则理论上需要参加反应的O2的物质的量为
您最近一年使用:0次
【推荐3】(1) 铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由下表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1 L 2.2 mol·L-1 NaOH溶液和1 mol O2,则两种气体的分子式及物质的量分别为_______ ,生成硫酸铜的物质的量为________ 。
(2)水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置,加入适量稀H2SO4,待MnO(OH)2与I-完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:O2 MnO(OH)2
MnO(OH)2 I2
I2 S4O
S4O
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:__________ 。
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水样的溶解氧,消耗0.010 00 mol·L-1Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧(以mg·L-1表示),写出计算过程________ 。
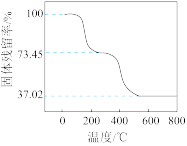
(3)为确定碱式碳酸铝镁[MgaAlb(OH)c(CO3)d·xH2O]的组成,进行如下实验:①准确称取3.390 g样品与足量稀盐酸充分反应,生成CO2 0.560 L(已换算成标准状况下)。②另取一定量样品在空气中加热,样品的固体残留率( )随温度的变化如图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。根据以上实验数据计算碱式碳酸铝镁样品中的n(OH-)∶n(CO
)随温度的变化如图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。根据以上实验数据计算碱式碳酸铝镁样品中的n(OH-)∶n(CO )=
)=________ 。(写出计算过程)
| 硫 | 氢 | Y | |
| X | 硫 | Z |
(2)水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置,加入适量稀H2SO4,待MnO(OH)2与I-完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:O2
 MnO(OH)2
MnO(OH)2 I2
I2 S4O
S4O
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水样的溶解氧,消耗0.010 00 mol·L-1Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧(以mg·L-1表示),写出计算过程
(3)为确定碱式碳酸铝镁[MgaAlb(OH)c(CO3)d·xH2O]的组成,进行如下实验:①准确称取3.390 g样品与足量稀盐酸充分反应,生成CO2 0.560 L(已换算成标准状况下)。②另取一定量样品在空气中加热,样品的固体残留率(
 )随温度的变化如图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。根据以上实验数据计算碱式碳酸铝镁样品中的n(OH-)∶n(CO
)随温度的变化如图所示(样品在270 ℃时已完全失去结晶水,600 ℃以上残留固体为金属氧化物的混合物)。根据以上实验数据计算碱式碳酸铝镁样品中的n(OH-)∶n(CO )=
)=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】ClO2是一 种消毒、 杀菌效率高、二次污染小的水处理剂,实验室可通过以下反应制得:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2 ↑+2H2O 。试回答下列问题。
(1)该反应中氧化产物的化学式是______________________
(2)若反应共产生了4. 48L气体(标准状况),则反应转移电子的物质的量为__________ ,消耗还原剂的物质的量为________
(3)标准状况下44. 8mL的ClO2气体恰好能与50mL0. 1mol/L的Na2SO3溶液完全反应生成Na2SO4,氯元素在产物中的化合价为_________ ,此过程说明 ClO2具有_______ (填 “氧化”或“还原”)性。
(1)该反应中氧化产物的化学式是
(2)若反应共产生了4. 48L气体(标准状况),则反应转移电子的物质的量为
(3)标准状况下44. 8mL的ClO2气体恰好能与50mL0. 1mol/L的Na2SO3溶液完全反应生成Na2SO4,氯元素在产物中的化合价为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】以石英砂(主要成分为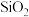 )为原料,经三步反应制得高纯硅,其中第一步反应的化学方程式如下。
)为原料,经三步反应制得高纯硅,其中第一步反应的化学方程式如下。
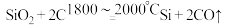
(1)作还原剂的物质是_______ ,碳元素的化合价_______ (填“升高”或“降低”)。
(2)若反应中消耗了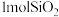 ,则生成
,则生成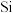 的物质的量为
的物质的量为_______  ,转移电子的物质的量为
,转移电子的物质的量为_______  。
。
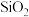 )为原料,经三步反应制得高纯硅,其中第一步反应的化学方程式如下。
)为原料,经三步反应制得高纯硅,其中第一步反应的化学方程式如下。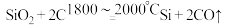
(1)作还原剂的物质是
(2)若反应中消耗了
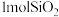 ,则生成
,则生成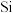 的物质的量为
的物质的量为 ,转移电子的物质的量为
,转移电子的物质的量为 。
。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】根据所学知识,回答下列问题:
(1)常温常压下,HCl气体溶于水形成的盐酸溶液,其溶质质量分数为
 ,密度为
,密度为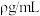 ,该溶液浓度为
,该溶液浓度为 。
。(2)“可燃冰”是由水和甲烷在一定条件下形成的类冰结晶化合物.
 “可燃冰”(
“可燃冰”( )的物质的量与
)的物质的量与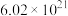 个水分子的物质的量相等,则该“可燃冰”的摩尔质量为
个水分子的物质的量相等,则该“可燃冰”的摩尔质量为(3)过氧化钠可用作呼吸面罩供氧剂,其原理可用方程式
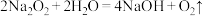 ,
,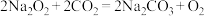 表示。若生成标况下
表示。若生成标况下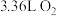 ,转移电子的数目为
,转移电子的数目为(4)现有
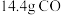 和
和 的混合气体,在标准状况下所占的体积约为
的混合气体,在标准状况下所占的体积约为 。将混合气体依次通过如图装置,最后收集在气球中,气球中收集到的气体在标况下的体积为
。将混合气体依次通过如图装置,最后收集在气球中,气球中收集到的气体在标况下的体积为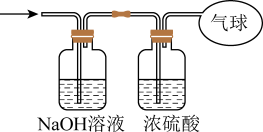
您最近一年使用:0次


 g,则溶液中的阳离子一定有
g,则溶液中的阳离子一定有 g,则溶液中的阳离子一定有
g,则溶液中的阳离子一定有

