ClO2是一 种消毒、 杀菌效率高、二次污染小的水处理剂,实验室可通过以下反应制得:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2 ↑+2H2O 。试回答下列问题。
(1)该反应中氧化产物的化学式是______________________
(2)若反应共产生了4. 48L气体(标准状况),则反应转移电子的物质的量为__________ ,消耗还原剂的物质的量为________
(3)标准状况下44. 8mL的ClO2气体恰好能与50mL0. 1mol/L的Na2SO3溶液完全反应生成Na2SO4,氯元素在产物中的化合价为_________ ,此过程说明 ClO2具有_______ (填 “氧化”或“还原”)性。
(1)该反应中氧化产物的化学式是
(2)若反应共产生了4. 48L气体(标准状况),则反应转移电子的物质的量为
(3)标准状况下44. 8mL的ClO2气体恰好能与50mL0. 1mol/L的Na2SO3溶液完全反应生成Na2SO4,氯元素在产物中的化合价为
20-21高一上·全国·阶段练习 查看更多[1]
(已下线)【南昌新东方】2019 南大附中 高一上第二次月考
更新时间:2020-04-18 11:11:20
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】过量铁粉与稀硝酸反应的方程式为:
Fe+HNO3(稀)→Fe(NO3)2+NO↑+H2O
(1)请写出上述反应配平的离子方程式__________________ ;
(2)标准状况下,当生成2.24L NO气体时,转移电子的物质的量为________ ,有____ mol氧化剂被还原。
Fe+HNO3(稀)→Fe(NO3)2+NO↑+H2O
(1)请写出上述反应配平的离子方程式
(2)标准状况下,当生成2.24L NO气体时,转移电子的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】(1)有一真空瓶质量为m1,该瓶充入空气后质量为m2。在相同状况下,若改为充入某气体A时,总质量为m3。已知空气相对分子质量为29,则A的相对分子质量是_______________
(2)把一定量铁粉放入氯化铁溶液中,完全反应后,得到溶液中Fe2+和Fe3+的浓度恰好相等。则已反应的Fe3+和未反应的Fe3+的物质的量之比为___________
(3)已知铜和稀硝酸反应方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,则被氧化的物质与被还原的物质质量比为___________
(4)A、B两个烧瓶中分别装80mL 3.0 mol/L的盐酸和NaOH溶液,再分别加等质量的铝粉,在相同状况下产生的气体的体积比为A:B=2:5,则加入铝粉的质量为___________
(2)把一定量铁粉放入氯化铁溶液中,完全反应后,得到溶液中Fe2+和Fe3+的浓度恰好相等。则已反应的Fe3+和未反应的Fe3+的物质的量之比为
(3)已知铜和稀硝酸反应方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,则被氧化的物质与被还原的物质质量比为
(4)A、B两个烧瓶中分别装80mL 3.0 mol/L的盐酸和NaOH溶液,再分别加等质量的铝粉,在相同状况下产生的气体的体积比为A:B=2:5,则加入铝粉的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题。
(1)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+C+S=K2S+2NO2↑+CO2↑,其中被还原的元素是___________ ,还原剂是___________ 。
(2)已知铜在常温下能被稀HNO3溶解,反应为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
①请将上述反应改写成离子方程式:___________ 。
②氧化剂是___________ 。
③用单线桥法标出该反应的电子转移情况:___________ 。
④在参加反应的硝酸中,起氧化作用的HNO3与起酸性作用的HNO3的分子个数之比为___________ 。
(1)火药是中国的“四大发明”之一,永远值得炎黄子孙骄傲,也永远会激励着我们去奋发图强。黑火药在发生爆炸时,发生如下的反应:2KNO3+C+S=K2S+2NO2↑+CO2↑,其中被还原的元素是
(2)已知铜在常温下能被稀HNO3溶解,反应为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
①请将上述反应改写成离子方程式:
②氧化剂是
③用单线桥法标出该反应的电子转移情况:
④在参加反应的硝酸中,起氧化作用的HNO3与起酸性作用的HNO3的分子个数之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】向Fe和Fe2O3组成的3.84g混合物中加入120mL某浓度的盐酸,恰好完全反应,生成672mLH2(标准状况下);向反应后的溶液中滴加几滴KSCN溶液,溶液无明显变化。
(1)原混合物中Fe的质量为___ g。
(2)所用盐酸的物质的量浓度为___ mol/L。
(1)原混合物中Fe的质量为
(2)所用盐酸的物质的量浓度为
您最近一年使用:0次
【推荐2】锌与100mL18.5mol·L-1的浓硫酸充分反应后,锌完全溶解,同时生成气体甲33.6L(标准状况)。将反应后的溶液稀释至1L,测得溶液的c(H+)=0.1mol·L-1。请计算:
(1)反应中共消耗H2SO4的物质的量为__ 。
(2)反应中共消耗Zn的质量为__ 。
(3)气体的成分及物质的量之比为__ 。
(1)反应中共消耗H2SO4的物质的量为
(2)反应中共消耗Zn的质量为
(3)气体的成分及物质的量之比为
您最近一年使用:0次
【推荐3】向27.2gCu和Cu2O的固体混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成4.48LNO(标准状况)和Cu(NO3)2,在所得溶液中加入1.0mol•L-1的NaOH溶液1.0L,此时溶液中的溶质为NaNO3,铜离子已完全沉淀,沉淀质量为39.2g。(提示:Cu2O稀硝酸反应的方程式为:3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O)
(1)在上述Cu2O与硝酸的反应中,硝酸表现出的性质有______ 。
(2)计算原固体混合物Cu2O中Cu与的物质的量之比_____ 。
(3)计算原硝酸溶液的物质的量浓度_____ 。
(1)在上述Cu2O与硝酸的反应中,硝酸表现出的性质有
(2)计算原固体混合物Cu2O中Cu与的物质的量之比
(3)计算原硝酸溶液的物质的量浓度
您最近一年使用:0次
【推荐1】高铁酸盐也是常用的水处理剂。高铁酸钠(Na2FeO4)可用如下反应制备:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,若生成2mol Na2FeO4,则反应中电子转移的物质的量为________ mol。高铁酸盐可将水体中的Mn2+氧化为MnO2进行除去,若氧化含Mn2+1mg的水体样本,需要1.2mg·L-1高铁酸钾________ L。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】根据所学知识,回答下列问题:
(1)常温常压下,HCl气体溶于水形成的盐酸溶液,其溶质质量分数为
 ,密度为
,密度为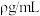 ,该溶液浓度为
,该溶液浓度为 。
。(2)“可燃冰”是由水和甲烷在一定条件下形成的类冰结晶化合物.
 “可燃冰”(
“可燃冰”( )的物质的量与
)的物质的量与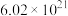 个水分子的物质的量相等,则该“可燃冰”的摩尔质量为
个水分子的物质的量相等,则该“可燃冰”的摩尔质量为(3)过氧化钠可用作呼吸面罩供氧剂,其原理可用方程式
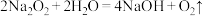 ,
,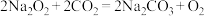 表示。若生成标况下
表示。若生成标况下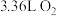 ,转移电子的数目为
,转移电子的数目为(4)现有
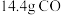 和
和 的混合气体,在标准状况下所占的体积约为
的混合气体,在标准状况下所占的体积约为 。将混合气体依次通过如图装置,最后收集在气球中,气球中收集到的气体在标况下的体积为
。将混合气体依次通过如图装置,最后收集在气球中,气球中收集到的气体在标况下的体积为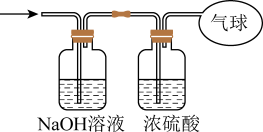
您最近一年使用:0次



