根据所学知识,回答下列问题:
(1)常温常压下,HCl气体溶于水形成的盐酸溶液,其溶质质量分数为
 ,密度为
,密度为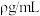 ,该溶液浓度为
,该溶液浓度为 。
。(2)“可燃冰”是由水和甲烷在一定条件下形成的类冰结晶化合物.
 “可燃冰”(
“可燃冰”( )的物质的量与
)的物质的量与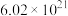 个水分子的物质的量相等,则该“可燃冰”的摩尔质量为
个水分子的物质的量相等,则该“可燃冰”的摩尔质量为(3)过氧化钠可用作呼吸面罩供氧剂,其原理可用方程式
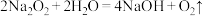 ,
,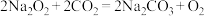 表示。若生成标况下
表示。若生成标况下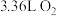 ,转移电子的数目为
,转移电子的数目为(4)现有
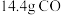 和
和 的混合气体,在标准状况下所占的体积约为
的混合气体,在标准状况下所占的体积约为 。将混合气体依次通过如图装置,最后收集在气球中,气球中收集到的气体在标况下的体积为
。将混合气体依次通过如图装置,最后收集在气球中,气球中收集到的气体在标况下的体积为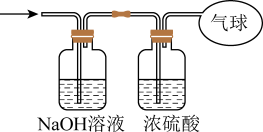
更新时间:2024-03-30 17:51:27
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】将30g MnO2的质量分数为76.6%的软锰矿石与足量的浓度为12 molL-1的浓盐酸完全反应(杂质不参加反应),试计算:
(1)参加反应的浓盐酸的体积的大小(结果保留3位小数)。____________
(2)在标准状况下,生成Cl2的体积的大小________ (结果保留1位小数,已知软锰矿石与浓盐酸反应的化学方程式为MnO2+4HCl(浓) =MnCl2+Cl2↑+2H2O)。
(1)参加反应的浓盐酸的体积的大小(结果保留3位小数)。
(2)在标准状况下,生成Cl2的体积的大小
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】填写下列空白:
(1)含有 个
个 的
的 ,则
,则 的物质的量为
的物质的量为_______ 。
(2)_______  中含有的氧原子数与标准状况下
中含有的氧原子数与标准状况下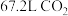 中含有的氧原子数相等。
中含有的氧原子数相等。
(3)同温同压下, 和
和 体积比为4∶3,它们的质量之比为
体积比为4∶3,它们的质量之比为_______ 。
(4)已知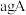 和
和 恰好完全反应生成
恰好完全反应生成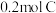 和
和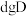 ,则C的摩尔质量为
,则C的摩尔质量为_______ 。
(1)含有
 个
个 的
的 ,则
,则 的物质的量为
的物质的量为(2)
 中含有的氧原子数与标准状况下
中含有的氧原子数与标准状况下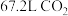 中含有的氧原子数相等。
中含有的氧原子数相等。(3)同温同压下,
 和
和 体积比为4∶3,它们的质量之比为
体积比为4∶3,它们的质量之比为(4)已知
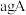 和
和 恰好完全反应生成
恰好完全反应生成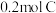 和
和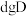 ,则C的摩尔质量为
,则C的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】125g黄铜(铜锌合金)粉末可以跟250g硫酸溶液恰好完全反应,称得未溶物质量为92.5g。(可能涉及到元素的相对原子质量:Zn65 H1 S32 O16 Cu64)
(1)写出该反应的化学方程式_______ 。
(2)若将反应后的溶液蒸发1g水,温度降到室温,溶液正好饱和。求在室温时硫酸锌的溶解度_______ 。
(1)写出该反应的化学方程式
(2)若将反应后的溶液蒸发1g水,温度降到室温,溶液正好饱和。求在室温时硫酸锌的溶解度
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】根据阿伏加 德罗常数回答下列问题
(1)在0.5mol CO2中含___ 个O原子,含___ 个e-。
(2)同温同压下,同质量的氨气和硫化氢气体体积比为____ ,其中含有的氢原子数目比为____ 。
(3)___ mol H2SO4分子与1.806×1024个H2O分子含有相同的氧原子数?
(4)12.4g Na2R含Na+ 0.4mol,则Na2R的摩尔质量为___ ,R的相对原子质量为___ 。
(1)在0.5mol CO2中含
(2)同温同压下,同质量的氨气和硫化氢气体体积比为
(3)
(4)12.4g Na2R含Na+ 0.4mol,则Na2R的摩尔质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】Ⅰ.(1)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为________ 。
(2)在25 ℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为______________ 。
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为________ 。
Ⅱ.在标准状况下,将aLNH3完全溶于水得到VmL氨水,溶液的密度为ρ g·cm-3,计算该溶液的浓度(用以上字母表示)。
(1)该溶液的物质的量浓度________________
(2)该溶液的质量分数_________________________
Ⅲ.有两份溶液,其中所含溶质相同,设其摩尔质量为M g·mol-1。根据下表信息,回答有关问题:
(1)取等质量两份溶液混合,则所得混合液中溶质的质量分数w3=________ 。(用以上字母表示)
(2)若有w1>w2,取等体积的两份溶液混合,设所得混合液中溶质的质量分数为w4,若ρ1>ρ2,则w3___ w4;若ρ1<ρ2,w3______ w4(填“>”“<”或“=”)。
(2)在25 ℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为
Ⅱ.在标准状况下,将aLNH3完全溶于水得到VmL氨水,溶液的密度为ρ g·cm-3,计算该溶液的浓度(用以上字母表示)。
(1)该溶液的物质的量浓度
(2)该溶液的质量分数
Ⅲ.有两份溶液,其中所含溶质相同,设其摩尔质量为M g·mol-1。根据下表信息,回答有关问题:
| 溶质的质量分数 | 溶液的密度(g·cm-3) | |
| 第一份溶液 | w1 | ρ1 |
| 第二份溶液 | w2 | ρ2 |
(1)取等质量两份溶液混合,则所得混合液中溶质的质量分数w3=
(2)若有w1>w2,取等体积的两份溶液混合,设所得混合液中溶质的质量分数为w4,若ρ1>ρ2,则w3
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】计算题
(1)12.4 g Na2X含有0.4 mol Na+,Na2X的摩尔质量为_____ 。
(2)相同状况下,一定体积的气态氢化物H2X的质量是等体积NH3的2倍。则X的相对原子质量为_____ 。
(3)0.05 mol的硫酸钠中含有的氧原子数,与_____ g NaCl中所含有的Na+数目相同。
(4)若XY2分子中X、Y两元素质量比是3:16,则X、Y两元素分别为_____ 和_____ (填元素名称)。
(5)0.5 L 0.5 mol/L FeCl3溶液中的Cl−的物质的量浓度为_____ 。
(6)质量分数为49%,密度为1.84 g/mL的某浓硫酸,溶质的物质的量浓度为__________ 。
(7)a个X原子的总质量为b g,则X的相对原子质量可表示为_____ 。
(1)12.4 g Na2X含有0.4 mol Na+,Na2X的摩尔质量为
(2)相同状况下,一定体积的气态氢化物H2X的质量是等体积NH3的2倍。则X的相对原子质量为
(3)0.05 mol的硫酸钠中含有的氧原子数,与
(4)若XY2分子中X、Y两元素质量比是3:16,则X、Y两元素分别为
(5)0.5 L 0.5 mol/L FeCl3溶液中的Cl−的物质的量浓度为
(6)质量分数为49%,密度为1.84 g/mL的某浓硫酸,溶质的物质的量浓度为
(7)a个X原子的总质量为b g,则X的相对原子质量可表示为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】Ⅰ.根据下列各题中所给出的数据,可分别求出其“溶液的溶质质量分数”或“溶液的物质的量浓度”,试判断并求解。
(1)已知某NaOH溶液V L中含有n个OH-,可求出此溶液的_______ 为________ 。
(2)已知某NaOH溶液中Na+与H2O的个数之比为1∶a,则可求出此溶液的_______ 为_________ 。
Ⅱ.常温下,10.0 mL 1.0 mol/L的H2SO4溶液,加水稀释到500 mL,所得H2SO4溶液的浓度为________ mol/L;蒸发浓缩,使溶液的体积为2.5 mL,所得H2SO4溶液的浓度为______ mol/L。
(1)已知某NaOH溶液V L中含有n个OH-,可求出此溶液的
(2)已知某NaOH溶液中Na+与H2O的个数之比为1∶a,则可求出此溶液的
Ⅱ.常温下,10.0 mL 1.0 mol/L的H2SO4溶液,加水稀释到500 mL,所得H2SO4溶液的浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)已知KMnO4与浓盐酸反应如下:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
①作还原剂的物质是___ 。
②若反应中每生成5molCl2,转移电子数目为___ 。
(2)19g某二价金属氯化物(ACl2)中含有0.4molCl-,则ACl2的相对分子质量是___ ;ACl2的化学式是____ 。
(3)将适量铁粉加到三氯化铁溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是___ 。
①作还原剂的物质是
②若反应中每生成5molCl2,转移电子数目为
(2)19g某二价金属氯化物(ACl2)中含有0.4molCl-,则ACl2的相对分子质量是
(3)将适量铁粉加到三氯化铁溶液中,完全反应后,溶液中的Fe3+和Fe2+浓度相等,则已反应的Fe3+和未反应的Fe3+的物质的量之比是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】(1)现有8种物质:① ②
② ③浓硫酸④铝⑤
③浓硫酸④铝⑤ 胶体 ⑥蔗糖溶液⑦
胶体 ⑥蔗糖溶液⑦ ⑧
⑧ 上述物质中属于电解质的有
上述物质中属于电解质的有_______ (选填序号);写出②的溶液与⑤反应的离子方程式_______
(2)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,研究人员提出,在碱性条件下可以用铝粉处理
的浓度,研究人员提出,在碱性条件下可以用铝粉处理 ,发生反应的化学方程式为:
,发生反应的化学方程式为: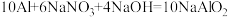
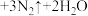 ,该反应中,还原剂为
,该反应中,还原剂为_______ ,若反应过程中转移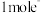 ,则生成标准状况下
,则生成标准状况下 的体积为
的体积为_______  。
。
(3)在含有一定量 和
和 溶质的溶液中,逐滴滴入一定浓度的稀盐酸,产生
溶质的溶液中,逐滴滴入一定浓度的稀盐酸,产生 的物质的量与滴入盐酸的量的关系如图,回答下列问题:
的物质的量与滴入盐酸的量的关系如图,回答下列问题:
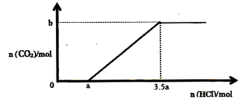
① 点发生反应的离子方程式为
点发生反应的离子方程式为_______
② 与
与 物质的量之比为
物质的量之比为_______
③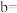
_______ (用含 的代数式表示)
的代数式表示)
(4)现有密度为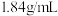 ,浓度为
,浓度为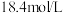 的浓硫酸,则该溶液中溶质的质量分数为
的浓硫酸,则该溶液中溶质的质量分数为_______
 ②
② ③浓硫酸④铝⑤
③浓硫酸④铝⑤ 胶体 ⑥蔗糖溶液⑦
胶体 ⑥蔗糖溶液⑦ ⑧
⑧ 上述物质中属于电解质的有
上述物质中属于电解质的有(2)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,研究人员提出,在碱性条件下可以用铝粉处理
的浓度,研究人员提出,在碱性条件下可以用铝粉处理 ,发生反应的化学方程式为:
,发生反应的化学方程式为: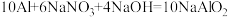
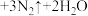 ,该反应中,还原剂为
,该反应中,还原剂为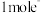 ,则生成标准状况下
,则生成标准状况下 的体积为
的体积为 。
。(3)在含有一定量
 和
和 溶质的溶液中,逐滴滴入一定浓度的稀盐酸,产生
溶质的溶液中,逐滴滴入一定浓度的稀盐酸,产生 的物质的量与滴入盐酸的量的关系如图,回答下列问题:
的物质的量与滴入盐酸的量的关系如图,回答下列问题:
①
 点发生反应的离子方程式为
点发生反应的离子方程式为②
 与
与 物质的量之比为
物质的量之比为③
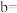
 的代数式表示)
的代数式表示)(4)现有密度为
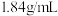 ,浓度为
,浓度为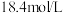 的浓硫酸,则该溶液中溶质的质量分数为
的浓硫酸,则该溶液中溶质的质量分数为
您最近一年使用:0次


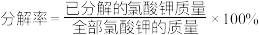 )
) ,该溶液中溶质的物质的量浓度是
,该溶液中溶质的物质的量浓度是 的稀氢氧化钠溶液100mL,需要40%氢氧化钠溶液的体积是
的稀氢氧化钠溶液100mL,需要40%氢氧化钠溶液的体积是 ,氢氧化钠的物质的量浓度是
,氢氧化钠的物质的量浓度是 钠钾合金溶于
钠钾合金溶于 水,生成氢气的(在标准状况下)体积为
水,生成氢气的(在标准状况下)体积为 ;
;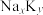 的形式表示):
的形式表示): 的物质的量浓度为
的物质的量浓度为

