计算填空:
(1)40%氢氧化钠溶液的密度为1.525 ,该溶液中溶质的物质的量浓度是
,该溶液中溶质的物质的量浓度是_______ 。
(2)配制0.1 的稀氢氧化钠溶液100mL,需要40%氢氧化钠溶液的体积是
的稀氢氧化钠溶液100mL,需要40%氢氧化钠溶液的体积是_______ 。
(3)将14.4g氢氧化钠固体溶于水配成100mL溶液,其密度为1.219 ,氢氧化钠的物质的量浓度是
,氢氧化钠的物质的量浓度是_______ 。
(1)40%氢氧化钠溶液的密度为1.525
 ,该溶液中溶质的物质的量浓度是
,该溶液中溶质的物质的量浓度是(2)配制0.1
 的稀氢氧化钠溶液100mL,需要40%氢氧化钠溶液的体积是
的稀氢氧化钠溶液100mL,需要40%氢氧化钠溶液的体积是(3)将14.4g氢氧化钠固体溶于水配成100mL溶液,其密度为1.219
 ,氢氧化钠的物质的量浓度是
,氢氧化钠的物质的量浓度是
更新时间:2023-03-24 17:46:46
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】根据所学知识,回答下列问题:
(1)含0.1NA个 的
的 中有
中有______ 个电子。
(2)氢原子物质的量相等的 和
和 的物质的量之比为
的物质的量之比为______ 。
(3)将8.0g 溶于水配成500mL溶液,则所得溶液的物质的量浓度为
溶于水配成500mL溶液,则所得溶液的物质的量浓度为______ 。
(4)现有16.0g CO和 的混合气体,在标准状况下其体积为8.96L。请回答下列问题:
的混合气体,在标准状况下其体积为8.96L。请回答下列问题:
①混合气体中碳原子的个数为______ (用NA表示阿伏加德罗常数的值)。
②将混合气体依次通过如图所示装置,最后收集在气球中(体积在标准状况下测定)。
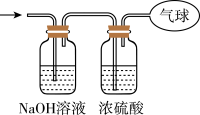
A.气球中收集到的气体的摩尔质量为______ 。
B.气球的体积为______ 。
(1)含0.1NA个
 的
的 中有
中有(2)氢原子物质的量相等的
 和
和 的物质的量之比为
的物质的量之比为(3)将8.0g
 溶于水配成500mL溶液,则所得溶液的物质的量浓度为
溶于水配成500mL溶液,则所得溶液的物质的量浓度为(4)现有16.0g CO和
 的混合气体,在标准状况下其体积为8.96L。请回答下列问题:
的混合气体,在标准状况下其体积为8.96L。请回答下列问题:①混合气体中碳原子的个数为
②将混合气体依次通过如图所示装置,最后收集在气球中(体积在标准状况下测定)。

A.气球中收集到的气体的摩尔质量为
B.气球的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】在标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g。则:
(1)混合气体的密度是_______ 。 (结果保留两位小数)
(2)CO和CO2的物质的量之比是________ 。
(3)CO的体积分数是________ ,CO的质量分数是________ 。
(4)混合气体中所含氧原子的物质的量是_________ ,所含碳原子的物质的量是_________ 。
(5)混合气体的平均摩尔质量是_________ ,对氢气的相对密度是__________ 。
(1)混合气体的密度是
(2)CO和CO2的物质的量之比是
(3)CO的体积分数是
(4)混合气体中所含氧原子的物质的量是
(5)混合气体的平均摩尔质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】实验室常用的浓盐酸密度为1.08 g·mL-1,质量分数为36.5 %。
(1)此浓盐酸的物质的量浓度为__________________ 。
(2)取此浓盐酸50 mL,用蒸馏水稀释为200 mL,稀释后盐酸的物质的量浓度为_____ 。
(3)将13 g 锌投入足量的上述实验所得的稀盐酸中,充分反应后,求:(写出计算过程)
①放出的H2在标准状况下的体积____________ 。
②将生成的H2 通过足量的灼热CuO,求生成铜的质量_________ (假设氢气在反应中没有损失)。
(1)此浓盐酸的物质的量浓度为
(2)取此浓盐酸50 mL,用蒸馏水稀释为200 mL,稀释后盐酸的物质的量浓度为
(3)将13 g 锌投入足量的上述实验所得的稀盐酸中,充分反应后,求:(写出计算过程)
①放出的H2在标准状况下的体积
②将生成的H2 通过足量的灼热CuO,求生成铜的质量
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】1.15 g金属钠与水反应,得到100 mL溶液,试计算:
(1)生成的气体在标准状况下的体积_____________ ;
(2)反应后所得溶液的物质的量浓度______________ 。
(1)生成的气体在标准状况下的体积
(2)反应后所得溶液的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】I.(1)标准状况下VmLCH4气体所含a个氢原子则NA=_________ 。
(2)相同条件下等质量的CO和CO2气体的体积之比_____ ,密度之比_____ 。
(3)100mL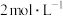 的硫酸铝溶液中c(Al3+)=
的硫酸铝溶液中c(Al3+)=__________ ,5mL该溶液中 的数目
的数目_____ 。(设阿伏加 德罗常数为NA)
II.乙酸是实验室常用的一种化学试剂,某乙酸试剂瓶上标签的部分内容如图所示。利用标签提供的信息,回答下列问题:
(1)乙酸的摩尔质量为__________ 。
(2)若该乙酸溶液的密度为 ,则此乙酸溶液的物质的量浓度表达式为
,则此乙酸溶液的物质的量浓度表达式为_________ 。
(3)某实验中要用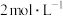 的乙酸溶液200mL,则需用
的乙酸溶液200mL,则需用_______ 量取上述乙酸溶液______ mL进行稀释。
(2)相同条件下等质量的CO和CO2气体的体积之比
(3)100mL
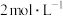 的硫酸铝溶液中c(Al3+)=
的硫酸铝溶液中c(Al3+)= 的数目
的数目II.乙酸是实验室常用的一种化学试剂,某乙酸试剂瓶上标签的部分内容如图所示。利用标签提供的信息,回答下列问题:
| 乙酸 化学式:CH3COOH 分析纯(500mL) 溶质的质量分数:36% |
(2)若该乙酸溶液的密度为
 ,则此乙酸溶液的物质的量浓度表达式为
,则此乙酸溶液的物质的量浓度表达式为(3)某实验中要用
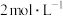 的乙酸溶液200mL,则需用
的乙酸溶液200mL,则需用
您最近一年使用:0次



