将30g MnO2的质量分数为76.6%的软锰矿石与足量的浓度为12 molL-1的浓盐酸完全反应(杂质不参加反应),试计算:
(1)参加反应的浓盐酸的体积的大小(结果保留3位小数)。____________
(2)在标准状况下,生成Cl2的体积的大小________ (结果保留1位小数,已知软锰矿石与浓盐酸反应的化学方程式为MnO2+4HCl(浓) =MnCl2+Cl2↑+2H2O)。
(1)参加反应的浓盐酸的体积的大小(结果保留3位小数)。
(2)在标准状况下,生成Cl2的体积的大小
更新时间:2019/12/15 11:08:38
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】完成下列填空:
(1)0.25 mol CO2在标准状况下的体积为________ ,含有的原子数目为________ 。
(2)0.98 g物质H2A中约含有6.02×1021个分子,则该物质的物质的量为________ ,H2A的摩尔质量为__________ ,A的相对原子质量为________ 。
(3)40 g的碳酸钙与足量的盐酸反应制备CO2,消耗盐酸__________ mol,标准状况下生成CO2 __________ L。
(1)0.25 mol CO2在标准状况下的体积为
(2)0.98 g物质H2A中约含有6.02×1021个分子,则该物质的物质的量为
(3)40 g的碳酸钙与足量的盐酸反应制备CO2,消耗盐酸
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题
(1)8 g CH4在标准状况下所占的体积约为_______ L。
(2)20g重水(D2O)中所含中子数目为_______ 。
(3)10.8g R2O5中氧原子数目为3.01×1023 ,则元素R的相对原子质量为_______ 。
(4)向10.0mL1.00mol·L-1 Na2CO3溶液加水稀释至100mL溶液,此时溶液中Na+的物质的量浓度为_______ 。
(5)实验室常用邻苯二甲酸氢钾(KHC8H4O4)来标定氢氧化钠溶液的浓度,其操作过程为:准确称取4.080g邻苯二甲酸氢钾,加水配成溶液,向溶液中加入1~2滴指示剂,用氢氧化钠溶液滴定至终点,消耗氢氧化钠溶液19.60mL。该氢氧化钠溶液的物质的量浓度为_______ 。(已知:KHC8H4O4+NaOH=KNaC8H4O4+H2O)
(6)100g质量分数为46%的酒精(CH3CH2OH)溶液中氧原子的物质的量为_______ 。
(1)8 g CH4在标准状况下所占的体积约为
(2)20g重水(D2O)中所含中子数目为
(3)10.8g R2O5中氧原子数目为3.01×1023 ,则元素R的相对原子质量为
(4)向10.0mL1.00mol·L-1 Na2CO3溶液加水稀释至100mL溶液,此时溶液中Na+的物质的量浓度为
(5)实验室常用邻苯二甲酸氢钾(KHC8H4O4)来标定氢氧化钠溶液的浓度,其操作过程为:准确称取4.080g邻苯二甲酸氢钾,加水配成溶液,向溶液中加入1~2滴指示剂,用氢氧化钠溶液滴定至终点,消耗氢氧化钠溶液19.60mL。该氢氧化钠溶液的物质的量浓度为
(6)100g质量分数为46%的酒精(CH3CH2OH)溶液中氧原子的物质的量为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】物质的量是高中化学常用的物理量,请完成以下有关计算。
(1)2mol水中含有_______ mol氢原子。
(2)在0. 5molNa2SO4中含有Na+的数目是_______ 个。
(3)标准状况下,11. 2L氖气中含分子的物质的量_______ mol。
(4)11. 2gFe与足量的稀硫酸反应得到氢气在标准状况下的体积是_______ L。
(5)含0. 4molAl3+的Al2(SO4)3中所含SO 的物质的量是
的物质的量是_______ mol。
(6)已知3.01×1023个X气体分子的质量为32g,则X气体的摩尔质量_______ 。
(7)9. 8g硫酸溶解在水中配成100mL溶液,则H+的物质的量浓度_______ 。
(1)2mol水中含有
(2)在0. 5molNa2SO4中含有Na+的数目是
(3)标准状况下,11. 2L氖气中含分子的物质的量
(4)11. 2gFe与足量的稀硫酸反应得到氢气在标准状况下的体积是
(5)含0. 4molAl3+的Al2(SO4)3中所含SO
 的物质的量是
的物质的量是(6)已知3.01×1023个X气体分子的质量为32g,则X气体的摩尔质量
(7)9. 8g硫酸溶解在水中配成100mL溶液,则H+的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】向20mL某浓度的AlCl3溶液中滴加2mol·L-1的NaOH溶液时,所得沉淀的质量与加入NaOH溶液的体积之间的关系如图所示:
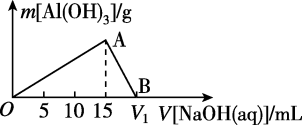
(1)图中A点的意义是________________ 。
(2)最大沉淀质量为________________ 。
(3)图中V1的值为________________ 。
(4)所用AlCl3溶液的物质的量浓度为________________ 。
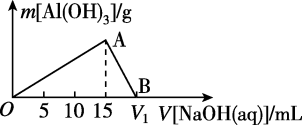
(1)图中A点的意义是
(2)最大沉淀质量为
(3)图中V1的值为
(4)所用AlCl3溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】无机化合物 A 和 NaH 都是重要的还原剂,遇水都强烈反应。一定条件下,2.4g NaH 与气体 B 反应生成 3.9g 化合物 A 和 2.24L(已折算成标准状况)的 H2。已知气体 B 可使湿润红色石蕊试纸变蓝。请回答下列问题:
(1)B 的化学式是_____ 。
(2)NaH 与气体 B 反应生成化合物 A 的化学方程式_____ 。该反应中 A 是_____ 。
A.氧化产物 B.还原产物 C.既不是氧化产物也不是还原产物
(3)0.1molA 与足量盐酸发生非氧化还原反应最多消耗 HCl_____ mol
(4)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,同时得到混合气体, 测得其平均摩尔质量为 25 g/mol,写出该反应的化学方程式_____ 。
(1)B 的化学式是
(2)NaH 与气体 B 反应生成化合物 A 的化学方程式
A.氧化产物 B.还原产物 C.既不是氧化产物也不是还原产物
(3)0.1molA 与足量盐酸发生非氧化还原反应最多消耗 HCl
(4)在高温下氢化钠(NaH)可将四氯化钛(TiC14)还原成金属钛,同时得到混合气体, 测得其平均摩尔质量为 25 g/mol,写出该反应的化学方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】(1)标准状况下,1体积水可溶解V体积HCl气体,所得溶液的密度为ρg/cm3,则所得溶液溶质的质量分数表示为______ ,溶质的物质的量浓度表示为_____
(2)若以ω1和ω2分别表示浓度为a mol/L和b mol/L硫酸溶液的溶质的质量分数,且知2a=b,则下列推断正确的是(硫酸溶液的密度比纯水的大)上(填序号)_______________
A.2ω1=ω2
B.ω1<ω2
C.ω2>2ω1
D.ω1<ω2<2ω1
(3)已知98%的浓硫酸的物质的量浓度为18. 4mol/L,则49%的硫酸的物质的量浓度______ 9.2mol/L.(填“>”,“=”或“<”)
(2)若以ω1和ω2分别表示浓度为a mol/L和b mol/L硫酸溶液的溶质的质量分数,且知2a=b,则下列推断正确的是(硫酸溶液的密度比纯水的大)上(填序号)
A.2ω1=ω2
B.ω1<ω2
C.ω2>2ω1
D.ω1<ω2<2ω1
(3)已知98%的浓硫酸的物质的量浓度为18. 4mol/L,则49%的硫酸的物质的量浓度
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】现有m g某X2气体,它的摩尔质量为M g/mol,阿伏加 德罗常数用NA表示,则:
(1)该气体的物质的量为________ mol。
(2)一个X原子的质量_________ g。
(3)该气体在标准状况下的体积为________ L。
(4)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为________ mol·L-1。
(5)该气体溶于1L水中(不考虑反应,常温下水的密度为1g/cm3),所得溶液的密度为ρg/cm3,则该溶液的物质的量浓度为__________ mol·L-1。
(1)该气体的物质的量为
(2)一个X原子的质量
(3)该气体在标准状况下的体积为
(4)该气体溶于水后形成VL溶液,其溶液的物质的量浓度为
(5)该气体溶于1L水中(不考虑反应,常温下水的密度为1g/cm3),所得溶液的密度为ρg/cm3,则该溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】请根据物质的量相关计算填空:
(1)在标准状况下,1.6 g 某氧化物RO3体积为0.448L,则R的相对原子量为________ 。
(2)已知Wg气体A含有a个分子,那么在标准状况下,bg气体A所占的体积是________ 。(其中阿伏加 德罗常数用NA表示)
(3)标准状况下,密度为0.75g/L的NH3与CH4组成的混合气体中,NH3的体积分数为________ 。
(4)VmLAl2(SO4)3溶液中含Al3+ ag,取V/5 mL溶液稀释到VmL,则稀释后溶液中的SO42-的物质的量浓度是______________ 。
(5)10 mL 0.1 mol·L-1 BaCl2溶液恰好能分别使相同体积的硫酸铁、硫酸铜两种溶液中的SO42-完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是____________ 。
(1)在标准状况下,1.6 g 某氧化物RO3体积为0.448L,则R的相对原子量为
(2)已知Wg气体A含有a个分子,那么在标准状况下,bg气体A所占的体积是
(3)标准状况下,密度为0.75g/L的NH3与CH4组成的混合气体中,NH3的体积分数为
(4)VmLAl2(SO4)3溶液中含Al3+ ag,取V/5 mL溶液稀释到VmL,则稀释后溶液中的SO42-的物质的量浓度是
(5)10 mL 0.1 mol·L-1 BaCl2溶液恰好能分别使相同体积的硫酸铁、硫酸铜两种溶液中的SO42-完全转化成沉淀,则硫酸铁、硫酸铜两种溶液的物质的量浓度之比是
您最近一年使用:0次



