钠及其化合物在生产和生活中有广泛的应用。钠钾合金可用作核反应堆的传热介质。 钠钾合金溶于
钠钾合金溶于 水,生成氢气的(在标准状况下)体积为
水,生成氢气的(在标准状况下)体积为 ;
;
(1)该过程中转移的电子数目为_______ 个。
(2)确定该钠钾合金的组成(用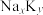 的形式表示):
的形式表示):_______ 。
(3)如果所得溶液的体积仍为 ,则溶液中
,则溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
 钠钾合金溶于
钠钾合金溶于 水,生成氢气的(在标准状况下)体积为
水,生成氢气的(在标准状况下)体积为 ;
;(1)该过程中转移的电子数目为
(2)确定该钠钾合金的组成(用
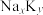 的形式表示):
的形式表示):(3)如果所得溶液的体积仍为
 ,则溶液中
,则溶液中 的物质的量浓度为
的物质的量浓度为
更新时间:2023-06-22 06:22:14
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】将70 g过氧化钠和氧化钠的混合物跟98 g水充分反应后,所得氢氧化钠溶液的质量分数为50%。计算原混合物中过氧化钠和氧化钠的质量各为多少克?
您最近一年使用:0次
【推荐2】取100 mL的Na2CO3和Na2SO4混合溶液,加入适量Ba(OH)2溶液100 mL后,恰好完全反应,过滤、干燥后得到14.51 g白色沉淀,再用过量稀硝酸处理沉淀,最后减少到4.66 g,并有气体放出。
计算:
(1)原混合液中Na2SO4的物质的量______ 。
(2)产生的气体在标准状况下的体积______ 。
计算:
(1)原混合液中Na2SO4的物质的量
(2)产生的气体在标准状况下的体积
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】将标准状况下的HCl气体4.48 L溶于水配成100 mL溶液,然后与足量的铁屑充分反应。计算:
(1)所得盐酸的物质的量浓度_______ 。
(2)将生成的FeCl2配成400 mL溶液,此溶液中FeCl2的物质的量浓度是_______ 。
(1)所得盐酸的物质的量浓度
(2)将生成的FeCl2配成400 mL溶液,此溶液中FeCl2的物质的量浓度是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】(1)0.2molNH3的质量为___ g,氢原子的物质的量为___ mol。
(2)1.6g某气体含有3.01×1022个分子,该气体的摩尔质量为___ g/mol。
(3)把2.0mol·L-1Na2SO4溶液和1.0mol·L-1H2SO4溶液等体积混合(假设混合后溶液的体积等于混合前两种溶液的体积之和),则SO 的物质的量浓度为
的物质的量浓度为___ mol·L-1。
(2)1.6g某气体含有3.01×1022个分子,该气体的摩尔质量为
(3)把2.0mol·L-1Na2SO4溶液和1.0mol·L-1H2SO4溶液等体积混合(假设混合后溶液的体积等于混合前两种溶液的体积之和),则SO
 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
【推荐2】回答下列问题:
(1)有H2SO4、FeSO4、Fe2(SO4)3的混合溶液100mL,已知溶液中的各阳离子的物质的量浓度相等, 的物质的量浓度为3.0mol/L,则c(H+)=
的物质的量浓度为3.0mol/L,则c(H+)=____ 。
(2)已知反应KClO3+6HCl(浓)=KCl+3Cl2+3H2O。
①用双线桥表示电子得失的数目与方向____ 。
②还原产物____ ;发生氧化反应的是____ 。
③若有标准状况下336mL的氯气生成,则有____ mol电子转移。
(1)有H2SO4、FeSO4、Fe2(SO4)3的混合溶液100mL,已知溶液中的各阳离子的物质的量浓度相等,
 的物质的量浓度为3.0mol/L,则c(H+)=
的物质的量浓度为3.0mol/L,则c(H+)=(2)已知反应KClO3+6HCl(浓)=KCl+3Cl2+3H2O。
①用双线桥表示电子得失的数目与方向
②还原产物
③若有标准状况下336mL的氯气生成,则有
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】物质的量是高中化学常用的物理量,请完成以下有关计算。
(1)将3.22g芒硝(Na2SO4·10H2O)溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为___ g。
(2)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L人造空气的质量是4.8g,其中氧气和氦气的分子数之比是___ ,氧气的质量是___ 。
(3)25.4g某二价金属A的氯化物中含有0.4molCl-,则A的摩尔质量为___ 。
(4)现有M、N两种气态化合物,其摩尔质量之比为2:1,将M、N两种气体分别溶于水(M、N与水均不反应)配成溶液,当两种溶液的质量分数相同时,其密度分别为d1和d2,则两种溶液的物质的量浓度之比为___ 。
(1)将3.22g芒硝(Na2SO4·10H2O)溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为
(2)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状况下,11.2L人造空气的质量是4.8g,其中氧气和氦气的分子数之比是
(3)25.4g某二价金属A的氯化物中含有0.4molCl-,则A的摩尔质量为
(4)现有M、N两种气态化合物,其摩尔质量之比为2:1,将M、N两种气体分别溶于水(M、N与水均不反应)配成溶液,当两种溶液的质量分数相同时,其密度分别为d1和d2,则两种溶液的物质的量浓度之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐1】食品包装中的铁系脱氧剂由还原铁粉、氯化钠和炭粉等组成,利用铁的吸氧腐蚀除去氧气,主要反应有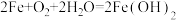 ,
,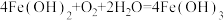 。已知某脱氧剂中含有2.24g还原铁粉,请计算:
。已知某脱氧剂中含有2.24g还原铁粉,请计算:
(1)还原铁粉的物质的量是_______ mol。
(2)若还原铁粉完全转化为Fe(OH)3,则转移电子的物质的量是_______ mol。
(3)在25 和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理_______ mL包装盒中的空气。
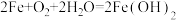 ,
,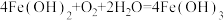 。已知某脱氧剂中含有2.24g还原铁粉,请计算:
。已知某脱氧剂中含有2.24g还原铁粉,请计算:(1)还原铁粉的物质的量是
(2)若还原铁粉完全转化为Fe(OH)3,则转移电子的物质的量是
(3)在25
 和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
和101kPa的条作下,气体摩尔体积约为24.5L/mol,空气中氧气的体积分数约为21%,则该脱氧剂理论上最多能处理
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】一种由CuO和KHC2O4溶液反应得到的蓝色结晶[KaCub(C2O4)c·dH2O]。为测定其组成,进行了如下实验:
步骤1:称取3.5400g该晶体,加入过量稀硫酸,待样品完全溶解后加入适量水,配制成100mL溶液A。
步骤2:量取20.00mLA溶液,滴加0.2000mol·L-1KMnO4溶液至恰好完全反应时,消耗KMnO4溶液8.00mL。
步骤3:另取20.00mLA溶液,加入足量NaOH溶液,充分反应后,经过滤、洗涤、灼烧、称重,得到黑色固体粉末0.16g。
已知:步骤2中发生反应如下,请配平:___ 。
 + H2C2O4+ H+= Mn2++ CO2↑+ H2O
+ H2C2O4+ H+= Mn2++ CO2↑+ H2O
(1)3.5400g该样品中含n( )=
)=___ mol。
(2)3.5400g该样品中含n(Cu2+)=___ mol。
(3)通过计算确定该蓝色晶体的化学式(计算过程)___ 。
步骤1:称取3.5400g该晶体,加入过量稀硫酸,待样品完全溶解后加入适量水,配制成100mL溶液A。
步骤2:量取20.00mLA溶液,滴加0.2000mol·L-1KMnO4溶液至恰好完全反应时,消耗KMnO4溶液8.00mL。
步骤3:另取20.00mLA溶液,加入足量NaOH溶液,充分反应后,经过滤、洗涤、灼烧、称重,得到黑色固体粉末0.16g。
已知:步骤2中发生反应如下,请配平:
 + H2C2O4+ H+= Mn2++ CO2↑+ H2O
+ H2C2O4+ H+= Mn2++ CO2↑+ H2O(1)3.5400g该样品中含n(
 )=
)=(2)3.5400g该样品中含n(Cu2+)=
(3)通过计算确定该蓝色晶体的化学式(计算过程)
您最近一年使用:0次

 。当有
。当有 电子发生转移时,理论上生成氯气的体积(标准状况)为
电子发生转移时,理论上生成氯气的体积(标准状况)为 的质量为
的质量为

