实验室可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下: 。当有
。当有 电子发生转移时,理论上生成氯气的体积(标准状况)为
电子发生转移时,理论上生成氯气的体积(标准状况)为_______ ,发生反应的 的质量为
的质量为_______ 。
 。当有
。当有 电子发生转移时,理论上生成氯气的体积(标准状况)为
电子发生转移时,理论上生成氯气的体积(标准状况)为 的质量为
的质量为
更新时间:2022-11-24 15:22:07
|
相似题推荐
计算题
|
适中
(0.65)
解题方法
【推荐1】锌与100mL 18.4mol/L的浓硫酸充分反应后,锌完全溶解,同时生成混合气体31.36L (标准状况)。将反应后的溶液稀释至1L,测得溶液的c(H+ )=0.08mol/L。请计算:
(1)反应中共消耗Zn的质量为_______ g;
(2)气体的物质的量之比为n____ : n____ =______ 。
(1)反应中共消耗Zn的质量为
(2)气体的物质的量之比为n
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】实验室要确定一瓶NaOH的浓度,进行了下列试验:取25.00mLNaOH于锥形瓶中,加入2滴酚酞溶液,在搅拌条件下,向锥形瓶中慢慢滴加0.2000mol/L盐酸溶液。当锥形瓶中溶液由红色变成无色时,记录消耗盐酸溶液的体积为25.25mL。计算NaOH物质的量浓度___ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】一般情况下,较强的氧化剂如:MnO2、KMnO4、KClO3、Ca(ClO)2等氧化浓盐酸时,有如下反应规律:氧化剂+浓盐酸→金属氯化物+水+氯气。实验室通常用该原理制取少量Cl2。
(1)将214.5gCa(ClO)2放入500mL12.0mol/L的浓盐酸中,生成的Cl2在标准状况下的体积为39.2L。若反应前后溶液的体积保持不变,计算反应后溶液中HCl的物质的量浓度。_______
(2)漂白粉是 Ca(ClO)2、CaCl2 、Ca(OH)2 、H2O 和 CaO 的混合物。漂白粉放出的氯气具有漂白作用,叫有效氯。通常用有效氯表示漂白粉的纯度。漂白粉中的有效氯含量常用滴定碘法进行测定,即在一定量的漂白粉中加入过量的KI ,加H2SO4酸化,有效氯与I-作用析出等量的I2,析出的I2以淀粉指示剂立即用Na2S2O3标准溶液滴定。若测定漂白粉中有效氯时用盐酸酸化,则盐酸的浓度应小于_______ mol/L,否则测定的有效氯将_______ (选填“偏高”、“偏低”或“不变”)。
(1)将214.5gCa(ClO)2放入500mL12.0mol/L的浓盐酸中,生成的Cl2在标准状况下的体积为39.2L。若反应前后溶液的体积保持不变,计算反应后溶液中HCl的物质的量浓度。
(2)漂白粉是 Ca(ClO)2、CaCl2 、Ca(OH)2 、H2O 和 CaO 的混合物。漂白粉放出的氯气具有漂白作用,叫有效氯。通常用有效氯表示漂白粉的纯度。漂白粉中的有效氯含量常用滴定碘法进行测定,即在一定量的漂白粉中加入过量的KI ,加H2SO4酸化,有效氯与I-作用析出等量的I2,析出的I2以淀粉指示剂立即用Na2S2O3标准溶液滴定。若测定漂白粉中有效氯时用盐酸酸化,则盐酸的浓度应小于
您最近一年使用:0次
【推荐1】CO2的减排、捕集和利用是人类可持续发展的重要战略之一。利用CO2和H2生成CH3OH来捕集CO2的反应是CO2(g)+3H2(g) CH3OH(l)+H2O(g) △H=-89 kJ·mol-1,回答下列问题:
CH3OH(l)+H2O(g) △H=-89 kJ·mol-1,回答下列问题:
(1)下列有关上述反应的图象合理的是__________ (填标号)。
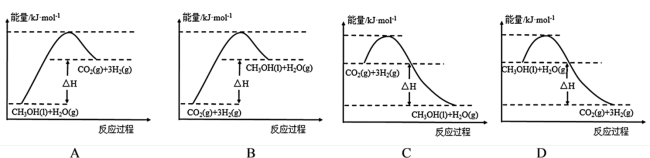
(2)①某温度下,向某恒容密闭容器中充入0.1 mol CO2(g)和0.3 mol H2(g),充分反应后,放出的热量__________ (填“>”“<”或“=”)8.9 kJ。
②完全燃烧1.6 g甲醇所消耗氧气的物质的量为________ ,转移的电子数为________ NA。
(3)某温度下,将定量的CO2(g)和H2(g)充入2 L恒容密用容器中,经过10 min后,反应达到平衡,图得CO2为0.5 mol、H2为1.2 mol、H2O为0.3 mol。则该条件下达到平衡时CO2的转化率为__________ %,氢气的体积分数ω(H2)=__________ %。
 CH3OH(l)+H2O(g) △H=-89 kJ·mol-1,回答下列问题:
CH3OH(l)+H2O(g) △H=-89 kJ·mol-1,回答下列问题:(1)下列有关上述反应的图象合理的是

(2)①某温度下,向某恒容密闭容器中充入0.1 mol CO2(g)和0.3 mol H2(g),充分反应后,放出的热量
②完全燃烧1.6 g甲醇所消耗氧气的物质的量为
(3)某温度下,将定量的CO2(g)和H2(g)充入2 L恒容密用容器中,经过10 min后,反应达到平衡,图得CO2为0.5 mol、H2为1.2 mol、H2O为0.3 mol。则该条件下达到平衡时CO2的转化率为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】钠及其化合物在生产和生活中有广泛的应用。钠钾合金可用作核反应堆的传热介质。 钠钾合金溶于
钠钾合金溶于 水,生成氢气的(在标准状况下)体积为
水,生成氢气的(在标准状况下)体积为 ;
;
(1)该过程中转移的电子数目为_______ 个。
(2)确定该钠钾合金的组成(用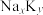 的形式表示):
的形式表示):_______ 。
(3)如果所得溶液的体积仍为 ,则溶液中
,则溶液中 的物质的量浓度为
的物质的量浓度为_______ 。
 钠钾合金溶于
钠钾合金溶于 水,生成氢气的(在标准状况下)体积为
水,生成氢气的(在标准状况下)体积为 ;
;(1)该过程中转移的电子数目为
(2)确定该钠钾合金的组成(用
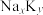 的形式表示):
的形式表示):(3)如果所得溶液的体积仍为
 ,则溶液中
,则溶液中 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
【推荐3】饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: 。请回答下列问题:
。请回答下列问题:
(1)上述反应中,被氧化的元素是___________ ,还原产物是___________ 。
(2)用“双线桥法”表示反应中电子转移的方向和数目:___________ 。

(3)反应中每生成1个 ,转移
,转移___________ 个电子。
(4)请配平下列离子方程式:___________ 。
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________
(5)已知 、
、 、
、 、
、 、
、 均有还原性,它们在酸性溶液中还原性的强弱顺序为:
均有还原性,它们在酸性溶液中还原性的强弱顺序为: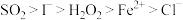 ,则下列反应不能发生的是:___________。
,则下列反应不能发生的是:___________。
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,其化学方程式为:
,其化学方程式为: 。请回答下列问题:
。请回答下列问题:(1)上述反应中,被氧化的元素是
(2)用“双线桥法”表示反应中电子转移的方向和数目:

(3)反应中每生成1个
 ,转移
,转移(4)请配平下列离子方程式:
___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________
(5)已知
 、
、 、
、 、
、 、
、 均有还原性,它们在酸性溶液中还原性的强弱顺序为:
均有还原性,它们在酸性溶液中还原性的强弱顺序为: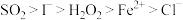 ,则下列反应不能发生的是:___________。
,则下列反应不能发生的是:___________。A.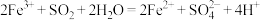 |
B. |
C.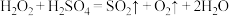 |
D. |
您最近一年使用:0次



