名校
解题方法
1 . 移取20.00 两种一元弱酸
两种一元弱酸 和
和 的混合溶液,滴加0.1
的混合溶液,滴加0.1 的
的 至反应终点,消耗25
至反应终点,消耗25 。再取相同的上述溶液,加入50
。再取相同的上述溶液,加入50 ,0.02
,0.02
 的强碱性溶液,待其反应完成后,将溶液酸化,加入30
的强碱性溶液,待其反应完成后,将溶液酸化,加入30 0.2
0.2
 溶液,将剩余的
溶液,将剩余的 和
和 歧化生成的
歧化生成的 和
和 全部还原至
全部还原至 ,剩余的
,剩余的 溶液用上述
溶液用上述 溶液在酸性条件下反应至终点消耗18.5
溶液在酸性条件下反应至终点消耗18.5 。
。
已知:
① 在强碱性条件下还原产物为
在强碱性条件下还原产物为 ;
; 在酸性条件发生歧化反应;
在酸性条件发生歧化反应;
② 具有还原性,酸性条件下被氧化为
具有还原性,酸性条件下被氧化为 ,
, 不能被酸性高锰酸钾氧化
不能被酸性高锰酸钾氧化
(1)加入 的强碱性溶液发生的有电子转移的离子反应方程式为
的强碱性溶液发生的有电子转移的离子反应方程式为_______ 。
(2)酸化后 歧化发生离子反应方程式为
歧化发生离子反应方程式为_______ 。
(3)加入 溶液后发生反应的离子方程式为
溶液后发生反应的离子方程式为_______ 。
(4)则溶液中的 的浓度为
的浓度为_______ ; 的浓度为
的浓度为_______ 。
(5)若溶液酸化后将 过滤除掉,其它操作不变,则测得的
过滤除掉,其它操作不变,则测得的 浓度将
浓度将_______ (填“偏大”、“偏小”或“不变”)。
 两种一元弱酸
两种一元弱酸 和
和 的混合溶液,滴加0.1
的混合溶液,滴加0.1 的
的 至反应终点,消耗25
至反应终点,消耗25 。再取相同的上述溶液,加入50
。再取相同的上述溶液,加入50 ,0.02
,0.02
 的强碱性溶液,待其反应完成后,将溶液酸化,加入30
的强碱性溶液,待其反应完成后,将溶液酸化,加入30 0.2
0.2
 溶液,将剩余的
溶液,将剩余的 和
和 歧化生成的
歧化生成的 和
和 全部还原至
全部还原至 ,剩余的
,剩余的 溶液用上述
溶液用上述 溶液在酸性条件下反应至终点消耗18.5
溶液在酸性条件下反应至终点消耗18.5 。
。已知:
①
 在强碱性条件下还原产物为
在强碱性条件下还原产物为 ;
; 在酸性条件发生歧化反应;
在酸性条件发生歧化反应;②
 具有还原性,酸性条件下被氧化为
具有还原性,酸性条件下被氧化为 ,
, 不能被酸性高锰酸钾氧化
不能被酸性高锰酸钾氧化(1)加入
 的强碱性溶液发生的有电子转移的离子反应方程式为
的强碱性溶液发生的有电子转移的离子反应方程式为(2)酸化后
 歧化发生离子反应方程式为
歧化发生离子反应方程式为(3)加入
 溶液后发生反应的离子方程式为
溶液后发生反应的离子方程式为(4)则溶液中的
 的浓度为
的浓度为 的浓度为
的浓度为(5)若溶液酸化后将
 过滤除掉,其它操作不变,则测得的
过滤除掉,其它操作不变,则测得的 浓度将
浓度将
您最近一年使用:0次
名校
解题方法
2 . 按要求回答问题。
(1)NaH能与水剧烈反应生成氢气,生成的 标准状况下体积为2.24L时,转移电子的数目
标准状况下体积为2.24L时,转移电子的数目___________ 。
(2)AlN用于电子仪器。AlN中常混有少量碳,将一定量含杂质碳的AlN样品置于密闭反应器中,通入0.18mol的 ,在高温下充分反应后测得气体的密度为
,在高温下充分反应后测得气体的密度为 (已折算成标准状况,AlN不跟
(已折算成标准状况,AlN不跟 反应),则所得气体的摩尔质量为
反应),则所得气体的摩尔质量为___________  ,该样品中含杂质碳
,该样品中含杂质碳___________ g。
(3)取x g铜镁合金完全溶于10mol/L100mL的浓硝酸中,反应过程中硝酸被还原产生6720mL的 气体和896mL的
气体和896mL的 气体(都已折算到标准状态),在反应后的溶液中加入1mol/L氢氧化钠溶液,生成沉淀质量为18.80g,则x等于
气体(都已折算到标准状态),在反应后的溶液中加入1mol/L氢氧化钠溶液,生成沉淀质量为18.80g,则x等于___________ g,消耗NaOH溶液的体积是___________ mL。
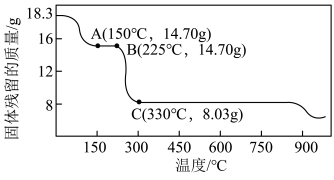
(4)钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。草酸钴是制备钴的氧化物的重要原料,如图为二水合草酸钴( )(M=183g/mol)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物,通过计算确定B点剩余固体的化学成分为
)(M=183g/mol)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物,通过计算确定B点剩余固体的化学成分为___________ (填化学式),取C点固体用足量的浓盐酸完全溶解可得到黄绿色气体,写出以上反应的离子反应方程式___________ 。
(1)NaH能与水剧烈反应生成氢气,生成的
 标准状况下体积为2.24L时,转移电子的数目
标准状况下体积为2.24L时,转移电子的数目(2)AlN用于电子仪器。AlN中常混有少量碳,将一定量含杂质碳的AlN样品置于密闭反应器中,通入0.18mol的
 ,在高温下充分反应后测得气体的密度为
,在高温下充分反应后测得气体的密度为 (已折算成标准状况,AlN不跟
(已折算成标准状况,AlN不跟 反应),则所得气体的摩尔质量为
反应),则所得气体的摩尔质量为 ,该样品中含杂质碳
,该样品中含杂质碳(3)取x g铜镁合金完全溶于10mol/L100mL的浓硝酸中,反应过程中硝酸被还原产生6720mL的
 气体和896mL的
气体和896mL的 气体(都已折算到标准状态),在反应后的溶液中加入1mol/L氢氧化钠溶液,生成沉淀质量为18.80g,则x等于
气体(都已折算到标准状态),在反应后的溶液中加入1mol/L氢氧化钠溶液,生成沉淀质量为18.80g,则x等于(4)钴及其化合物广泛应用于磁性材料、电池材料及超硬材料等领域。草酸钴是制备钴的氧化物的重要原料,如图为二水合草酸钴(
 )(M=183g/mol)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物,通过计算确定B点剩余固体的化学成分为
)(M=183g/mol)在空气中受热的质量变化曲线,曲线中300℃及以上所得固体均为钴氧化物,通过计算确定B点剩余固体的化学成分为
您最近一年使用:0次
2023高三·全国·专题练习
3 . 从含铜丰富的自然资源黄铜矿(CuFeS2)冶炼铜的工艺流程如下:
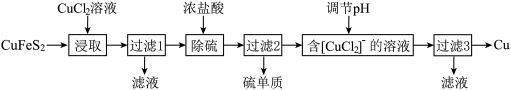
已知:CuFeS2+3CuCl2=4CuCl+FeCl2+2S。过滤3所得滤液中可以循环使用的物质有_______ ,为保持流程持续循环,每生成1molCu,理论上需补充CuCl2的物质的量为_______ 。

已知:CuFeS2+3CuCl2=4CuCl+FeCl2+2S。过滤3所得滤液中可以循环使用的物质有
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
4 . 铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由表中所示两种元素组成,气体的相对分子质量都小于50,为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗 溶液和
溶液和 ,则两种气体的分子式及物质的量分别为
,则两种气体的分子式及物质的量分别为_______ ,生成的硫酸铜的物质的量为_______ 。
 溶液和
溶液和 ,则两种气体的分子式及物质的量分别为
,则两种气体的分子式及物质的量分别为| 碳 | 氮 | 氧 | |
| 硅 | 硫 | 氯 |
您最近一年使用:0次
2023高三·全国·专题练习
5 . MnO2又名黑锰矿,主要用于生产优质软磁铁氧体。MnO2的合成方法按制备工艺中所用原料的不同,分为固相合成和液相合成。已知:MnO2不溶于水,其中锰的价态有+2价,也可能有+3价和+4价。请回答下列问题:

若③中收集到672mL(标准状况下)的H2,则理论上可以得到_______ gMn3O4。

若③中收集到672mL(标准状况下)的H2,则理论上可以得到
您最近一年使用:0次
2023高三·全国·专题练习
6 . 取300mL0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是_______ mol。
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
7 . 用酸性高锰酸钾溶液滴定法可测定双氧水中H2O2的含量:H2O2+KMnO4+H2SO4→MnSO4+K2SO4+O2↑+H2O(未配平),若滴定中消耗0.50mol/L的高锰酸钾溶液40.00mL,则此双氧水溶液中溶质的质量为_______ g。
您最近一年使用:0次
2023高三·全国·专题练习
8 . 反应2LiBH4=2LiH+2B+3H2↑,生成22.4LH2(标准状况)时,转移电子的物质的量为_______ mol。
您最近一年使用:0次
2023高三·全国·专题练习
9 . 二氧化铈(CeO2)是一种重要的稀土氧化物,在平板电视显示屏中有着重要的应用CeO2在稀硫酸和H2O2的作用下可生成Ce3+,H2O2在该反应中作_______ (填“氧化”“还原”)剂,每有1molH2O2参加反应,转移电子的物质的量为_______ 。
您最近一年使用:0次
2023高三·全国·专题练习
10 . NaCN超标的电镀废水可用两段氧化法处理(HCN、HOCN中N元素的化合价相同):
①NaCN与NaClO反应,生成NaOCN和NaCl
②NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
处理100 m3含NaCN 10.3mg/L的废水,实际至少需NaClO_______ g(实际用量应为理论值的4倍),才能使NaCN含量低于0.5 mg/L,达到排放标准。
①NaCN与NaClO反应,生成NaOCN和NaCl
②NaOCN与NaClO反应,生成Na2CO3、CO2、NaCl和N2
处理100 m3含NaCN 10.3mg/L的废水,实际至少需NaClO
您最近一年使用:0次



