从含铜丰富的自然资源黄铜矿(CuFeS2)冶炼铜的工艺流程如下:
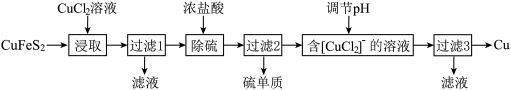
已知:CuFeS2+3CuCl2=4CuCl+FeCl2+2S。过滤3所得滤液中可以循环使用的物质有_______ ,为保持流程持续循环,每生成1molCu,理论上需补充CuCl2的物质的量为_______ 。

已知:CuFeS2+3CuCl2=4CuCl+FeCl2+2S。过滤3所得滤液中可以循环使用的物质有
2023高三·全国·专题练习 查看更多[1]
(已下线)考点08 物质的量在化学方程式计算中的应用(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
更新时间:2023-08-11 10:31:16
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】(1)标准状况下,相同质量的(1)O2(2)CO2(3)H2O其中,体积最大的是___ ,原子数最多的是___ ,分子数最多的是____ ;
(2)常温常压下,相同体积的SO2和O2,质量之比为___ ,所含氧原子数之比为___ 。
(2)常温常压下,相同体积的SO2和O2,质量之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】钢铁是最重要、用量最大的金属材料之一。完成下列计算:
51.生产1吨含铁96%的生铁,至少需要氧化铁含量70%的赤铁矿(杂质不含铁)_____ 吨。(计算结果保留2位小数)
52.工业炼铁用一氧化碳还原氧化铁时会发生如下一系列反应:
3Fe2O3+CO=2Fe3O4+CO2
Fe3O4+CO=3FeO+CO2
FeO+CO=Fe+CO2
某次实验中,用CO还原4.80 g氧化铁,当固体质量变成4.56 g时,测得此固体中只存在2种氧化物。通过计算确定此固体可能的成分和它们的物质的量之比_____ 。
53.为了测定某碳素钢(假设只含铁和碳)的含碳量,将10.000 g钢样完全溶解于过量的热浓硝酸中,产生了0.300 mol气体(假设气体全部逸出,N2O4已折算为NO2)。气体用50.00 mL 12.00 mol/L的NaOH溶液完全吸收后,只生成两种盐,溶液蒸干后得到不含结晶水的固体32.664 g。计算:
(1)钢样的含碳量_____ 。
(2)参加反应的硝酸的物质的量_____ 。
51.生产1吨含铁96%的生铁,至少需要氧化铁含量70%的赤铁矿(杂质不含铁)
52.工业炼铁用一氧化碳还原氧化铁时会发生如下一系列反应:
3Fe2O3+CO=2Fe3O4+CO2
Fe3O4+CO=3FeO+CO2
FeO+CO=Fe+CO2
某次实验中,用CO还原4.80 g氧化铁,当固体质量变成4.56 g时,测得此固体中只存在2种氧化物。通过计算确定此固体可能的成分和它们的物质的量之比
53.为了测定某碳素钢(假设只含铁和碳)的含碳量,将10.000 g钢样完全溶解于过量的热浓硝酸中,产生了0.300 mol气体(假设气体全部逸出,N2O4已折算为NO2)。气体用50.00 mL 12.00 mol/L的NaOH溶液完全吸收后,只生成两种盐,溶液蒸干后得到不含结晶水的固体32.664 g。计算:
(1)钢样的含碳量
(2)参加反应的硝酸的物质的量
您最近一年使用:0次
计算题
|
适中
(0.64)
【推荐1】计算:将足量的铜屑加入到浓度均为2mol/L的HNO3和H2SO4的混合溶液100ml中,充分反应后,求溶液中Cu2+浓度(假设溶液体积不变)。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】兴趣小组用莫尔盐[化学式为(NH4)XFe(SO4)2·6H2O(Fe为+2价)]测定KMnO4溶液的物质的量浓度的过程如下:
①称取19.6g莫尔盐配成100mL溶液。
②量取10.00mL KMnO4溶液,向其中加入足量的H2SO4进行酸化,向酸化后的溶液中逐滴滴加莫尔盐溶液,反应完全时消耗莫尔盐溶液的体积20.00mL,所发生反应的离子方程式如下:8H++5Fe2++ =5Fe3++Mn2++4H2O请回答下列问题:
=5Fe3++Mn2++4H2O请回答下列问题:
(1)(NH4)XFe(SO4)2·6H2O中x=_______ ,c(Fe2+)=__________
(2)计算KMnO4溶液的物质的量浓度,写出计算过程__________ 。
①称取19.6g莫尔盐配成100mL溶液。
②量取10.00mL KMnO4溶液,向其中加入足量的H2SO4进行酸化,向酸化后的溶液中逐滴滴加莫尔盐溶液,反应完全时消耗莫尔盐溶液的体积20.00mL,所发生反应的离子方程式如下:8H++5Fe2++
 =5Fe3++Mn2++4H2O请回答下列问题:
=5Fe3++Mn2++4H2O请回答下列问题:(1)(NH4)XFe(SO4)2·6H2O中x=
(2)计算KMnO4溶液的物质的量浓度,写出计算过程
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐3】将32.64g铜粉与140 mL 一定量浓硝酸恰好完全反应,铜完全溶解,反应后收集到的气体在标准状况下的体积为11.2 L。(反应中只产生NO或NO2 )请回答:
(1)NO的物质的量为___________ mol
(2)待产生的气体全部释放后,向溶液中加入v mL a mol/L的 NaOH 溶液,恰好使溶液中的 Cu2+ 全部沉淀,则原硝酸的浓度为_____________ 。
(3)欲使铜与硝酸反应生成的气体在溶液中完全转化为NaNO3,至少需要加入30%的双氧水的质量是___ g
(1)NO的物质的量为
(2)待产生的气体全部释放后,向溶液中加入v mL a mol/L的 NaOH 溶液,恰好使溶液中的 Cu2+ 全部沉淀,则原硝酸的浓度为
(3)欲使铜与硝酸反应生成的气体在溶液中完全转化为NaNO3,至少需要加入30%的双氧水的质量是
您最近一年使用:0次



