名校
解题方法
1 . 为了测定某铜银合金成分,将30.0g合金溶于80mL 浓硝酸中,待反应完全后,收集到6.72L气体(气体中没有
浓硝酸中,待反应完全后,收集到6.72L气体(气体中没有 )(已换算成标准状况),并测得溶液中氢离子浓度为
)(已换算成标准状况),并测得溶液中氢离子浓度为 。假设反应后溶液的体积仍为80mL,试计算(已知Ag可与
。假设反应后溶液的体积仍为80mL,试计算(已知Ag可与 反应):
反应):
(1)合金中铜的质量为___________ 克。
(2)产生的气体中NO与 的体积比是
的体积比是___________ 。
(3) 与NO体积比为2∶1的混合气体用氢氧化钠溶液吸收,所得溶液中
与NO体积比为2∶1的混合气体用氢氧化钠溶液吸收,所得溶液中 和
和 物质的量之比是
物质的量之比是___________ 。( ,
, )
)
(4)习惯命名法为新戊烷的物质其系统命名法为:___________ 。
 浓硝酸中,待反应完全后,收集到6.72L气体(气体中没有
浓硝酸中,待反应完全后,收集到6.72L气体(气体中没有 )(已换算成标准状况),并测得溶液中氢离子浓度为
)(已换算成标准状况),并测得溶液中氢离子浓度为 。假设反应后溶液的体积仍为80mL,试计算(已知Ag可与
。假设反应后溶液的体积仍为80mL,试计算(已知Ag可与 反应):
反应):(1)合金中铜的质量为
(2)产生的气体中NO与
 的体积比是
的体积比是(3)
 与NO体积比为2∶1的混合气体用氢氧化钠溶液吸收,所得溶液中
与NO体积比为2∶1的混合气体用氢氧化钠溶液吸收,所得溶液中 和
和 物质的量之比是
物质的量之比是 ,
, )
)(4)习惯命名法为新戊烷的物质其系统命名法为:
您最近一年使用:0次
名校
解题方法
2 . 将20.0 g铜镁合金完全溶解于140 mL某浓度的硝酸中,得到NO2和NO的混合气体8.96 L(标准状况),当向反应后的溶液中加入320 mL 4.0 mol/L NaOH溶液时,金属离子全部转化为沉淀,测得沉淀的质量为37 g。通过计算回答下列问题:
(1)该合金中铜与镁的物质的量之比是_______ 。
(2)该硝酸中HNO3的物质的量浓度是_______ mol/L。
(3)NO2和NO的混合气体中,NO2的体积分数是_______ 。
(4)若将混合气体与水混合完全转化为硝酸,则需要通入的氧气(标准状况)的体积为_______ L。
(1)该合金中铜与镁的物质的量之比是
(2)该硝酸中HNO3的物质的量浓度是
(3)NO2和NO的混合气体中,NO2的体积分数是
(4)若将混合气体与水混合完全转化为硝酸,则需要通入的氧气(标准状况)的体积为
您最近一年使用:0次
解题方法
3 . 某稀硫酸和稀硝酸的混合溶液500mL,平均分成两等份。向第一份中逐渐加入铜粉,最多能溶解9.6g铜粉。向第二份中逐渐加入铁粉,产生气体的量随加入铁粉质量的变化如图所示(假设硝酸只被还原为 气体)。
气体)。

已知:不考虑溶液混合时体积和温度变化。
回答下列问题:
(1)在第一份溶液中,反应进行时:
①发生反应的离子方程式为_______ 。
②被消耗完全的离子为_______ (填离子符号)。
(2)在第二份溶液中:
①从反应开始至反应结束的过程中,产生的气体有_______ (填化学式),所得气体的总体积为_______ L(标准状况下)。
②检验a点溶液中金属离子的方法为_______ 。
③a→b的化学方程式为_______ 。
④c点溶液中,
_______  。
。
(3)原混合溶液中,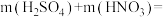
_______ g。
 气体)。
气体)。
已知:不考虑溶液混合时体积和温度变化。
回答下列问题:
(1)在第一份溶液中,反应进行时:
①发生反应的离子方程式为
②被消耗完全的离子为
(2)在第二份溶液中:
①从反应开始至反应结束的过程中,产生的气体有
②检验a点溶液中金属离子的方法为
③a→b的化学方程式为
④c点溶液中,

 。
。(3)原混合溶液中,
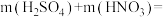
您最近一年使用:0次
2023-03-20更新
|
722次组卷
|
2卷引用:河南省豫北名校2022-2023学年高一下学期第一次联考化学试题
2023高三·全国·专题练习
解题方法
4 . 铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由表中所示两种元素组成,气体的相对分子质量都小于50,为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗 溶液和
溶液和 ,则两种气体的分子式及物质的量分别为
,则两种气体的分子式及物质的量分别为_______ ,生成的硫酸铜的物质的量为_______ 。
 溶液和
溶液和 ,则两种气体的分子式及物质的量分别为
,则两种气体的分子式及物质的量分别为| 碳 | 氮 | 氧 | |
| 硅 | 硫 | 氯 |
您最近一年使用:0次
解题方法
5 . SO2在生产生活中有重要的应用,处理不当会造成环境污染。回答下列问题:
(1)标准状况下16.0gSO2的体积为______ L,与______ molH2O中所含氧原子数相等。
(2)为测定某工厂废气中SO2的含量,课外小组的同学将废气样品经过管道通入密闭容器中的100mL0.1000mol•L-1的酸性高锰酸钾溶液。反应原理为:5SO2+2MnO +2H2O=5SO
+2H2O=5SO +2Mn2++4H+。
+2Mn2++4H+。
①该反应中被还原的元素是_____ 。
②100mL该酸性高锰酸钾溶液恰好完全反应时,转移电子的数目为______ 。
③若通入管道的废气样品为am3时,酸性高锰酸钾溶液恰好褪色,则该废气样品中SO2的含量为______ g•m-3(用含a的表达式表示,假定样品中其它气体均不参与反应,SO2可被溶液充分吸收)。
④实验需240mL0.500mol•L-1的硫酸溶液,使用的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、_____ ;需用量筒量取密度为1.84g•cm-3,质量分数为98%的浓硫酸_____ mL;若定容时俯视刻度线,则所配溶液的浓度______ (填“偏高”、“偏低”或“不变”)。
(1)标准状况下16.0gSO2的体积为
(2)为测定某工厂废气中SO2的含量,课外小组的同学将废气样品经过管道通入密闭容器中的100mL0.1000mol•L-1的酸性高锰酸钾溶液。反应原理为:5SO2+2MnO
 +2H2O=5SO
+2H2O=5SO +2Mn2++4H+。
+2Mn2++4H+。①该反应中被还原的元素是
②100mL该酸性高锰酸钾溶液恰好完全反应时,转移电子的数目为
③若通入管道的废气样品为am3时,酸性高锰酸钾溶液恰好褪色,则该废气样品中SO2的含量为
④实验需240mL0.500mol•L-1的硫酸溶液,使用的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管、
您最近一年使用:0次
名校
解题方法
6 .  是一种棕黑色粉末,难溶于水,可用作强氧化剂和电极制造等。实验室由
是一种棕黑色粉末,难溶于水,可用作强氧化剂和电极制造等。实验室由 溶液氧化碱性
溶液氧化碱性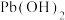 法制备
法制备 的步骤如下:
的步骤如下:

反应原理: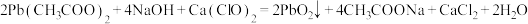 为测定产品(只含
为测定产品(只含 和PbO)中
和PbO)中 、PbO的物质的量之比,称取产品0.5194g,加入20.00mL 0.2500
、PbO的物质的量之比,称取产品0.5194g,加入20.00mL 0.2500
 溶液(
溶液( 还原为
还原为 ,
, 被氧化为
被氧化为 )搅拌使其充分反应,然后用氨水中和,过滤、洗涤除去
)搅拌使其充分反应,然后用氨水中和,过滤、洗涤除去 ,滤液酸化后用0.0400
,滤液酸化后用0.0400
 标准溶液滴定至终点(
标准溶液滴定至终点( 还原为
还原为 ,
, 被氧化为
被氧化为 ),消耗标准溶液10.00mL。计算产品中
),消耗标准溶液10.00mL。计算产品中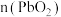 与
与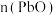 物质的量之比
物质的量之比______ (写出计算过程)。
 是一种棕黑色粉末,难溶于水,可用作强氧化剂和电极制造等。实验室由
是一种棕黑色粉末,难溶于水,可用作强氧化剂和电极制造等。实验室由 溶液氧化碱性
溶液氧化碱性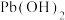 法制备
法制备 的步骤如下:
的步骤如下:
反应原理:
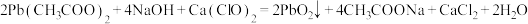 为测定产品(只含
为测定产品(只含 和PbO)中
和PbO)中 、PbO的物质的量之比,称取产品0.5194g,加入20.00mL 0.2500
、PbO的物质的量之比,称取产品0.5194g,加入20.00mL 0.2500
 溶液(
溶液( 还原为
还原为 ,
, 被氧化为
被氧化为 )搅拌使其充分反应,然后用氨水中和,过滤、洗涤除去
)搅拌使其充分反应,然后用氨水中和,过滤、洗涤除去 ,滤液酸化后用0.0400
,滤液酸化后用0.0400
 标准溶液滴定至终点(
标准溶液滴定至终点( 还原为
还原为 ,
, 被氧化为
被氧化为 ),消耗标准溶液10.00mL。计算产品中
),消耗标准溶液10.00mL。计算产品中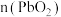 与
与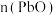 物质的量之比
物质的量之比
您最近一年使用:0次
名校
7 . 向27.2gCu和Cu2O的混合溶液中加入某浓度的稀硝酸0.5L,固体完全溶解,生成NO和Cu(NO3)2。在所得溶液中加入1.0mol/LNaOH溶液1.0L,得到39.2g沉淀,且此时溶液呈中性。请回答:
(1)生成的NO气体在标况下的体积为_____ L。
(2)所加稀硝酸的物质的量浓度为_____ mol/L。
(1)生成的NO气体在标况下的体积为
(2)所加稀硝酸的物质的量浓度为
您最近一年使用:0次
2023高三·全国·专题练习
8 . MnO2又名黑锰矿,主要用于生产优质软磁铁氧体。MnO2的合成方法按制备工艺中所用原料的不同,分为固相合成和液相合成。已知:MnO2不溶于水,其中锰的价态有+2价,也可能有+3价和+4价。请回答下列问题:

若③中收集到672mL(标准状况下)的H2,则理论上可以得到_______ gMn3O4。

若③中收集到672mL(标准状况下)的H2,则理论上可以得到
您最近一年使用:0次
2023高三·全国·专题练习
9 . 取300mL0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是_______ mol。
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
10 . 用酸性高锰酸钾溶液滴定法可测定双氧水中H2O2的含量:H2O2+KMnO4+H2SO4→MnSO4+K2SO4+O2↑+H2O(未配平),若滴定中消耗0.50mol/L的高锰酸钾溶液40.00mL,则此双氧水溶液中溶质的质量为_______ g。
您最近一年使用:0次



