已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
(1)该“84消毒液”的物质的量浓度约为_______ mol·L-1。
(2)该同学参阅该“84消毒液”的配方,欲用NaCIO固体配制480mL含NaCIO质量分数为25%的消毒液。下列说法正确的是_______。
(3)84消毒液与洁厕灵(主要成分是盐酸)混合后使用,就会对人体产生严重的危害,发生的反应如下: ,取100mL上述稀释过的84消毒液与足量洁厕灵混合,产生氯气的体积在标准状况下约为
,取100mL上述稀释过的84消毒液与足量洁厕灵混合,产生氯气的体积在标准状况下约为_______ L(保留两位有效数字)。
(4)写出与Cl-具有相同电子数的正离子、负离子、分子各一种:_______ 、_______ 、_______ 。
| 84消毒液 有效成分:NaClO 规格:1000mL 质量分数:25% 密度:1.192g·cm-3 |
(2)该同学参阅该“84消毒液”的配方,欲用NaCIO固体配制480mL含NaCIO质量分数为25%的消毒液。下列说法正确的是_______。
| A.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制 |
| B.需要称量NaClO固体的质量为149.0g |
| C.将NaCIO固体于烧杯中溶解后,应立即将溶液转移到容量瓶中 |
| D.配制好的溶液可置于容量瓶中保存 |
 ,取100mL上述稀释过的84消毒液与足量洁厕灵混合,产生氯气的体积在标准状况下约为
,取100mL上述稀释过的84消毒液与足量洁厕灵混合,产生氯气的体积在标准状况下约为(4)写出与Cl-具有相同电子数的正离子、负离子、分子各一种:
更新时间:2024-02-17 16:38:48
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】溶液的浓度在生产生活中用途广泛,请填空
(1)100mL硫酸钠溶液中n(Na+)=0.2mol,则其中c( )=
)=______ 。
(2)某溶液中含有离子: 、
、 、
、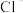 、
、 ,测得
,测得 、
、 和
和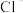 的物质的量浓度依次为:0.2mol∙L﹣1、0.25mol∙L﹣1、0.4mol∙L﹣1,则c(
的物质的量浓度依次为:0.2mol∙L﹣1、0.25mol∙L﹣1、0.4mol∙L﹣1,则c( )=
)=______ .
(3)有等体积的NaCl、CaCl2、AlCl3三种溶液,分别与足量的AgNO3溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为___ 。
(4)VmLAl2(SO4)3溶液中含 ag,取0.5VmL溶液稀释到2VmL,则稀释后溶液中
ag,取0.5VmL溶液稀释到2VmL,则稀释后溶液中 的物质的量浓度是
的物质的量浓度是______ mol/L。
(1)100mL硫酸钠溶液中n(Na+)=0.2mol,则其中c(
 )=
)=(2)某溶液中含有离子:
 、
、 、
、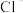 、
、 ,测得
,测得 、
、 和
和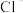 的物质的量浓度依次为:0.2mol∙L﹣1、0.25mol∙L﹣1、0.4mol∙L﹣1,则c(
的物质的量浓度依次为:0.2mol∙L﹣1、0.25mol∙L﹣1、0.4mol∙L﹣1,则c( )=
)=(3)有等体积的NaCl、CaCl2、AlCl3三种溶液,分别与足量的AgNO3溶液反应,若生成沉淀的质量相等,则三种溶液中所含溶质的物质的量浓度之比为
(4)VmLAl2(SO4)3溶液中含
 ag,取0.5VmL溶液稀释到2VmL,则稀释后溶液中
ag,取0.5VmL溶液稀释到2VmL,则稀释后溶液中 的物质的量浓度是
的物质的量浓度是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求完成下列问题。
(1)现需配制0.1mol/LNaOH溶液450mL。
①该实验要用的玻璃仪器有:烧杯、玻璃棒、胶头滴管、_______ 。
②根据计算得知,所需NaOH的质量为_______ 。
③下列操作对溶液浓度的影响(填写“偏高”、“偏低”或“无影响”)
i.定容时,俯视容量瓶的刻度线,所配制的溶液浓度_______ ;
ii.溶液未冷却至室温就移液和定容,所配制的溶液浓度_______ 。
(2)①10.6g的Na2CO3含有_______ mol氧原子。
②标准状况下6.72LNH3分子中所含原子总数与_______ gH2O所含原子总数相等。
③14.2gNa2SO4溶于水,配制成500mL的溶液,该溶液中钠离子的物质的量浓度c=_______ mol/L。
(1)现需配制0.1mol/LNaOH溶液450mL。
①该实验要用的玻璃仪器有:烧杯、玻璃棒、胶头滴管、
②根据计算得知,所需NaOH的质量为
③下列操作对溶液浓度的影响(填写“偏高”、“偏低”或“无影响”)
i.定容时,俯视容量瓶的刻度线,所配制的溶液浓度
ii.溶液未冷却至室温就移液和定容,所配制的溶液浓度
(2)①10.6g的Na2CO3含有
②标准状况下6.72LNH3分子中所含原子总数与
③14.2gNa2SO4溶于水,配制成500mL的溶液,该溶液中钠离子的物质的量浓度c=
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】现有由硝酸钾、硝酸铵、硝酸镁组成的无土栽培液0.2 L,部分离子的浓度如下表所示:
(1)该混合溶液中硝酸镁的物质的量浓度为_______ ,将该混合溶液加水稀释至体积为1 L,稀释后溶液中NO 的物质的量浓度为
的物质的量浓度为_______ 。
(2)混合液中硝酸铵的物质的量为_______ ,硝酸钾的质量为_______ 。
(3)向该溶液中加入_______ mol NaOH可以使Mg2+完全沉淀,写出该反应的化学方程式_______
| 离子种类 | NH | Mg2+ | NO |
| 离子的物质的量浓度( mol·L-1) | 0.2 | 0.1 | 0.6 |
(1)该混合溶液中硝酸镁的物质的量浓度为
 的物质的量浓度为
的物质的量浓度为(2)混合液中硝酸铵的物质的量为
(3)向该溶液中加入
您最近一年使用:0次
【推荐1】在一个氧化还原反应的体系中,共有KCl、Cl2、H2SO4、H2O、KMnO4、MnSO4、K2SO4七种物质:
(1)该反应中,化合价升高的反应物是__ ,化合价没有发生变化的反应物是__ 。
(2)写出一个包含上述七种物质的氧化还原反应方程式(不需配平):__ 。
(3)1molKMnO4在反应中___ (填“得到”或“失去”)__ mol电子。
(4)如果在反应后的溶液中加入NaBiO3,溶液又变紫红色。则氧化性的强弱关系为:NaBiO3__ KMnO4(填“大于”或“小于”)。
(1)该反应中,化合价升高的反应物是
(2)写出一个包含上述七种物质的氧化还原反应方程式(不需配平):
(3)1molKMnO4在反应中
(4)如果在反应后的溶液中加入NaBiO3,溶液又变紫红色。则氧化性的强弱关系为:NaBiO3
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】根据反应MnO2+4HCl(浓) Cl2↑+MnCl2+2H2O,回答下列问题:
Cl2↑+MnCl2+2H2O,回答下列问题:
①试用双线桥表示出上述氧化还原反应的变化情况:__________
②87gMnO2和足量浓盐酸在加热的条件下反应,在标准状况下,收集到的氯气的体积为___________ L.
③含4molHCl的浓盐酸与足量MnO2在加热的条件下反应,在标准状况下,收集到氯气的体积_____ 22.4L(填“>”“=”或“<”)
 Cl2↑+MnCl2+2H2O,回答下列问题:
Cl2↑+MnCl2+2H2O,回答下列问题:①试用双线桥表示出上述氧化还原反应的变化情况:
②87gMnO2和足量浓盐酸在加热的条件下反应,在标准状况下,收集到的氯气的体积为
③含4molHCl的浓盐酸与足量MnO2在加热的条件下反应,在标准状况下,收集到氯气的体积
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】现有以下物质:ⅰ. 、ⅱ.酒精、ⅲ.
、ⅱ.酒精、ⅲ. 、ⅳ.
、ⅳ. 、ⅴ.
、ⅴ. 溶液、ⅵ.食醋、ⅶ.
溶液、ⅵ.食醋、ⅶ. 、ⅷ.
、ⅷ. 、ⅸ.烧碱溶液、ⅹ.液氯。
、ⅸ.烧碱溶液、ⅹ.液氯。
回答下列问题:
(1)以上物质属于电解质的有_______ (填编号,下同),能导电的有_______ 。
(2)写出物质ⅷ的电离方程式:________ 。
(3)物质ⅴ和物质ⅸ混合后发生反应的离子方程式为________ 。
(4)向 物质ⅸ中通入一定量的物质ⅲ,充分反应后再向溶液中逐滴滴入
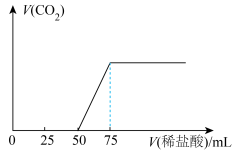
物质ⅸ中通入一定量的物质ⅲ,充分反应后再向溶液中逐滴滴入 的稀盐酸,产生气体体积(标准状况下)与所加稀盐酸体积之间的关系如图所示,通入物质ⅲ后形成溶液的溶质成分是
的稀盐酸,产生气体体积(标准状况下)与所加稀盐酸体积之间的关系如图所示,通入物质ⅲ后形成溶液的溶质成分是_______ (填化学式),原 物质ix的浓度为
物质ix的浓度为______ 。
(5)物质ⅳ是一种新型净水剂。制取物质ⅳ时所发生的反应如下: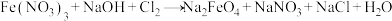
①配平上述反应的化学方程式并用“双线桥”表示电子转移情况:________ 。
②该反应中 是
是________ (填“氧化剂”“还原剂”“氧化产物”或“还原产物”)。
③生成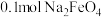 时,转移电子的数自为
时,转移电子的数自为____  (
( 表示阿伏加德罗常数的值),消耗
表示阿伏加德罗常数的值),消耗___ 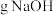 。
。
 、ⅱ.酒精、ⅲ.
、ⅱ.酒精、ⅲ. 、ⅳ.
、ⅳ. 、ⅴ.
、ⅴ. 溶液、ⅵ.食醋、ⅶ.
溶液、ⅵ.食醋、ⅶ. 、ⅷ.
、ⅷ. 、ⅸ.烧碱溶液、ⅹ.液氯。
、ⅸ.烧碱溶液、ⅹ.液氯。回答下列问题:
(1)以上物质属于电解质的有
(2)写出物质ⅷ的电离方程式:
(3)物质ⅴ和物质ⅸ混合后发生反应的离子方程式为
(4)向
 物质ⅸ中通入一定量的物质ⅲ,充分反应后再向溶液中逐滴滴入
物质ⅸ中通入一定量的物质ⅲ,充分反应后再向溶液中逐滴滴入 的稀盐酸,产生气体体积(标准状况下)与所加稀盐酸体积之间的关系如图所示,通入物质ⅲ后形成溶液的溶质成分是
的稀盐酸,产生气体体积(标准状况下)与所加稀盐酸体积之间的关系如图所示,通入物质ⅲ后形成溶液的溶质成分是 物质ix的浓度为
物质ix的浓度为
(5)物质ⅳ是一种新型净水剂。制取物质ⅳ时所发生的反应如下:
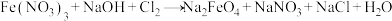
①配平上述反应的化学方程式并用“双线桥”表示电子转移情况:
②该反应中
 是
是③生成
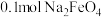 时,转移电子的数自为
时,转移电子的数自为 (
( 表示阿伏加德罗常数的值),消耗
表示阿伏加德罗常数的值),消耗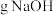 。
。
您最近一年使用:0次
【推荐1】钪及其化合物具有许多优良的性能,在宇航、电子、超导等方面有着广泛的应用。从钛白工业废酸(含钪、钛、铁、锰等离子)中提取氧化钪(Sc2O3)的一种流程如图:
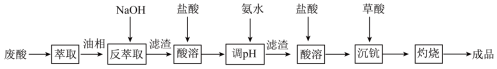
回答下列问题:
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合的实验操作是___________ 。
(2)钪锰矿石中含铁元素,其中Fe2+易被氧化为Fe3+的原因是___________ 。(从原子结构角度解释)

回答下列问题:
(1)洗涤“油相”可除去大量的钛离子。洗涤水是用93%的硫酸、27.5%的双氧水和水按一定比例混合而成。混合的实验操作是
(2)钪锰矿石中含铁元素,其中Fe2+易被氧化为Fe3+的原因是
您最近一年使用:0次
【推荐2】我国科学家通过测量SiO2中26Al和16Be两种元素的比例确定“北京人”年龄,这种测量方法叫“铝铍测年法”,完成下列填空:
(1)写出Be的核外电子排布式___ ,Be所在的周期中,最外层有2个未成对电子的元素的符号有___ 、___ 。
(2)Al和Be具有相似的化学性质,铝原子核外有___ 种不同运动状态的电子,写出BeCl2水解反应的化学方程式:___ 。
(3)研究表明26Al可以衰变为26Mg。请从原子结构角度解释这两种元素金属性强弱关系___ 。
(4)比较Al3+、S2﹣和Cl﹣半径由大到小的顺序___ ;这3种元素最高价氧化物对应的水化物中酸性最强的是___ (写名称),Al2O3是离子化合物,而AlCl3是共价化合物。工业制铝时,电解Al2O3而不电解AlCl3的原因是___ 。
(1)写出Be的核外电子排布式
(2)Al和Be具有相似的化学性质,铝原子核外有
(3)研究表明26Al可以衰变为26Mg。请从原子结构角度解释这两种元素金属性强弱关系
(4)比较Al3+、S2﹣和Cl﹣半径由大到小的顺序
您最近一年使用:0次
【推荐3】A、B、C、D、代表4种元素,请完成下列问题:
(1)A元素的负一价离子的电子层结构与氩相同,B元素的正一价离子的电子层结构与氙相同,A、B形成的化合物的化学式为____________ .
(2)C元素的正三价离子的3d轨道为半充满状态,C元素的符号为_________ .在同期表中位置_________ ,其基态原子的价电子排布图为____________ .
(3)D元素基态原子的M层全充满,N层没有成对电子,只有1个未成对电子,其硫酸盐逐滴加入氨水生成难溶物的离子方程式为__________________________ ,继续添加氨水,难溶物溶解,得到深蓝色溶液的离子方程为_______________________ ,写出阳离子的结构式____________ .
(1)A元素的负一价离子的电子层结构与氩相同,B元素的正一价离子的电子层结构与氙相同,A、B形成的化合物的化学式为
(2)C元素的正三价离子的3d轨道为半充满状态,C元素的符号为
(3)D元素基态原子的M层全充满,N层没有成对电子,只有1个未成对电子,其硫酸盐逐滴加入氨水生成难溶物的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学按下列步骤配制500mL 0.200mol·L-1 Na2CO3溶液,请回答有关问题。
(6)你认为按上述步骤配制的Na2CO3溶液的浓度是否为0.200mol·L-1,请说明理由。________
| 实验步骤 | 有关问题 |
| (1)计算所需Na2CO3的质量 | 需要Na2CO3的质量为 |
| (2)称量Na2CO3固体 | 称量过程中主要用到的仪器是 |
| (3)将Na2CO3加入100mL烧杯中 | 为加快溶解速率,可采取的措施是 |
| (4)将烧杯中的溶液转移至500mL容量瓶中 | 为防止溶液溅出,应采取的措施是 |
| (5)向容量瓶中加蒸馏水至刻度线 | 在进行此操作时应注意的问题是 |
(6)你认为按上述步骤配制的Na2CO3溶液的浓度是否为0.200mol·L-1,请说明理由。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】邻苯二甲酸氢钾(摩尔质量为204 )常用作
)常用作 测定的缓冲剂,现需要用0.1
测定的缓冲剂,现需要用0.1 邻苯二甲酸氢钾溶液和0.1
邻苯二甲酸氢钾溶液和0.1 盐酸配成
盐酸配成 缓冲液。回答下列问题:
缓冲液。回答下列问题:
(1)欲用邻苯二甲酸氢钾固体配制480 0.1
0.1 的邻苯二甲酸氢钾溶液。除烧杯、量筒、玻璃棒之外,还需要用到的玻璃仪器有
的邻苯二甲酸氢钾溶液。除烧杯、量筒、玻璃棒之外,还需要用到的玻璃仪器有_________ 。
(2)在配制邻苯二甲酸氢钾溶液时,下列说法正确的是_________ 。
a.溶解邻苯二甲酸氢钾后直接转移到容量瓶中
b.容量瓶用蒸馏水洗净烘干后才能用于溶液配制
c.配制过程中未用蒸馏水洗涤溶解后的烧杯和玻璃棒会导致溶液浓度偏低
d.需要称量邻苯二甲酸氢钾固体的质量为9.8g
e.定容时仰视环形刻度线会导致浓度偏低
(3)用密度1.1 、质量分数为18%的盐酸配制250
、质量分数为18%的盐酸配制250 0.1
0.1 的稀盐酸,需要量取
的稀盐酸,需要量取_________  浓盐酸,选用
浓盐酸,选用_________  量筒。
量筒。
(4)若向该换缓冲溶液中加入少量的酸,则该溶液还会保持 ,请用离子方程式说明原因
,请用离子方程式说明原因_________ 。(邻苯二甲酸为二元弱酸,可用 来代替)
来代替)
 )常用作
)常用作 测定的缓冲剂,现需要用0.1
测定的缓冲剂,现需要用0.1 邻苯二甲酸氢钾溶液和0.1
邻苯二甲酸氢钾溶液和0.1 盐酸配成
盐酸配成 缓冲液。回答下列问题:
缓冲液。回答下列问题:(1)欲用邻苯二甲酸氢钾固体配制480
 0.1
0.1 的邻苯二甲酸氢钾溶液。除烧杯、量筒、玻璃棒之外,还需要用到的玻璃仪器有
的邻苯二甲酸氢钾溶液。除烧杯、量筒、玻璃棒之外,还需要用到的玻璃仪器有(2)在配制邻苯二甲酸氢钾溶液时,下列说法正确的是
a.溶解邻苯二甲酸氢钾后直接转移到容量瓶中
b.容量瓶用蒸馏水洗净烘干后才能用于溶液配制
c.配制过程中未用蒸馏水洗涤溶解后的烧杯和玻璃棒会导致溶液浓度偏低
d.需要称量邻苯二甲酸氢钾固体的质量为9.8g
e.定容时仰视环形刻度线会导致浓度偏低
(3)用密度1.1
 、质量分数为18%的盐酸配制250
、质量分数为18%的盐酸配制250 0.1
0.1 的稀盐酸,需要量取
的稀盐酸,需要量取 浓盐酸,选用
浓盐酸,选用 量筒。
量筒。(4)若向该换缓冲溶液中加入少量的酸,则该溶液还会保持
 ,请用离子方程式说明原因
,请用离子方程式说明原因 来代替)
来代替)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学是一门以实验为基础的学科,化学所取得的丰硕成果,是与实验的重要作用分不开的。结合下列实验装置图回答问题:
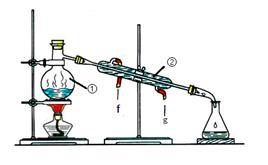
I II
(1)写出上述图中仪器的名称:①_______ ;②______ ;
(2)若利用装置I分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物,还缺少的仪器有__________ ,将仪器补充完整后进行的实验操作的名称为_____ ;实验时仪器②中冷却水的进口为_______ (选填“f”或“g”)。
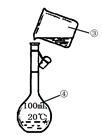
(3)现需配制250 mL 0.2 mol·L-1 NaCl溶液,装置II是某同学转移溶液的示意图,图中有两处错误分别是_______ ,_______ 。


I II
(1)写出上述图中仪器的名称:①
(2)若利用装置I分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物,还缺少的仪器有
(3)现需配制250 mL 0.2 mol·L-1 NaCl溶液,装置II是某同学转移溶液的示意图,图中有两处错误分别是
您最近一年使用:0次



