现有以下物质:ⅰ. 、ⅱ.酒精、ⅲ.
、ⅱ.酒精、ⅲ. 、ⅳ.
、ⅳ. 、ⅴ.
、ⅴ. 溶液、ⅵ.食醋、ⅶ.
溶液、ⅵ.食醋、ⅶ. 、ⅷ.
、ⅷ. 、ⅸ.烧碱溶液、ⅹ.液氯。
、ⅸ.烧碱溶液、ⅹ.液氯。
回答下列问题:
(1)以上物质属于电解质的有_______ (填编号,下同),能导电的有_______ 。
(2)写出物质ⅷ的电离方程式:________ 。
(3)物质ⅴ和物质ⅸ混合后发生反应的离子方程式为________ 。
(4)向 物质ⅸ中通入一定量的物质ⅲ,充分反应后再向溶液中逐滴滴入
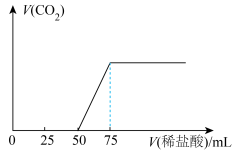
物质ⅸ中通入一定量的物质ⅲ,充分反应后再向溶液中逐滴滴入 的稀盐酸,产生气体体积(标准状况下)与所加稀盐酸体积之间的关系如图所示,通入物质ⅲ后形成溶液的溶质成分是
的稀盐酸,产生气体体积(标准状况下)与所加稀盐酸体积之间的关系如图所示,通入物质ⅲ后形成溶液的溶质成分是_______ (填化学式),原 物质ix的浓度为
物质ix的浓度为______ 。
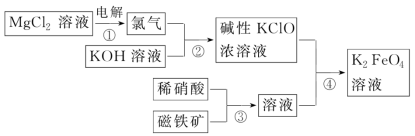
(5)物质ⅳ是一种新型净水剂。制取物质ⅳ时所发生的反应如下: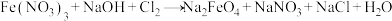
①配平上述反应的化学方程式并用“双线桥”表示电子转移情况:________ 。
②该反应中 是
是________ (填“氧化剂”“还原剂”“氧化产物”或“还原产物”)。
③生成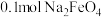 时,转移电子的数自为
时,转移电子的数自为____  (
( 表示阿伏加德罗常数的值),消耗
表示阿伏加德罗常数的值),消耗___ 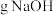 。
。
 、ⅱ.酒精、ⅲ.
、ⅱ.酒精、ⅲ. 、ⅳ.
、ⅳ. 、ⅴ.
、ⅴ. 溶液、ⅵ.食醋、ⅶ.
溶液、ⅵ.食醋、ⅶ. 、ⅷ.
、ⅷ. 、ⅸ.烧碱溶液、ⅹ.液氯。
、ⅸ.烧碱溶液、ⅹ.液氯。回答下列问题:
(1)以上物质属于电解质的有
(2)写出物质ⅷ的电离方程式:
(3)物质ⅴ和物质ⅸ混合后发生反应的离子方程式为
(4)向
 物质ⅸ中通入一定量的物质ⅲ,充分反应后再向溶液中逐滴滴入
物质ⅸ中通入一定量的物质ⅲ,充分反应后再向溶液中逐滴滴入 的稀盐酸,产生气体体积(标准状况下)与所加稀盐酸体积之间的关系如图所示,通入物质ⅲ后形成溶液的溶质成分是
的稀盐酸,产生气体体积(标准状况下)与所加稀盐酸体积之间的关系如图所示,通入物质ⅲ后形成溶液的溶质成分是 物质ix的浓度为
物质ix的浓度为
(5)物质ⅳ是一种新型净水剂。制取物质ⅳ时所发生的反应如下:
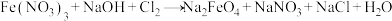
①配平上述反应的化学方程式并用“双线桥”表示电子转移情况:
②该反应中
 是
是③生成
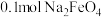 时,转移电子的数自为
时,转移电子的数自为 (
( 表示阿伏加德罗常数的值),消耗
表示阿伏加德罗常数的值),消耗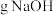 。
。
更新时间:2024-01-30 13:46:34
|
相似题推荐
【推荐1】在铜跟稀硝酸的反应中,如果有1 mol硝酸被还原,则被氧化的铜的物质的量为_______ mol。若将产生的气体(NO)和一定量的O2混合通入水中,恰好完全溶解,求需要O2_______ L。(气体的体积都按标况下计算)
您最近一年使用:0次
【推荐2】钠及其化合物在生产、生活中有着重要的应用。
(1)钠是一种银白色的金属,取2.3g钠块在干燥空气中放置一段时间后,其表面会失去金属光泽生成 ,此时固体质量为2.46g,则原钠块中已被氧化的钠为
,此时固体质量为2.46g,则原钠块中已被氧化的钠为_______ mol;再将该钠块在干燥空气中充分加热,会得到浅黄色的_______ (填化学式)粉末;经过上述两步实验后,最终得到的粉末的质量应为_______ g。
(2)某课外小组为了验证 和
和 的稳定性,设计如下图所示的实验装置
的稳定性,设计如下图所示的实验装置

①为使实验更具有说服力,你认为在试管A中最好放物质_______ (填化学式),在AB试管中能发生的反应的化学方程式为_______ 。
②实验时,C、D两个烧杯中的现象分别是_______ ,可以证明碳酸钠比碳酸氢钠稳定。
(1)钠是一种银白色的金属,取2.3g钠块在干燥空气中放置一段时间后,其表面会失去金属光泽生成
 ,此时固体质量为2.46g,则原钠块中已被氧化的钠为
,此时固体质量为2.46g,则原钠块中已被氧化的钠为(2)某课外小组为了验证
 和
和 的稳定性,设计如下图所示的实验装置
的稳定性,设计如下图所示的实验装置
①为使实验更具有说服力,你认为在试管A中最好放物质
②实验时,C、D两个烧杯中的现象分别是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】
| 化学式 | FeO | Fe2O3 | Fe3O4 |
| 俗名 | - | ① | ② |
| 颜色状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体(有磁性) |
| 溶解性 | 难溶于水 | 难溶于水 | 难溶于水 |
| 铁元素的化合价 | ③ | ④ | ⑤ |
| 稳定性 | 不稳定 | 稳定 | 稳定 |
| 类别 | 碱性氧化物 | 碱性氧化物 | 特殊氧化物 |
| 与H+反应的离子方程式 | ⑥ | ⑦ | ⑧ |
| 与CO反应的通式 | FexOy+yCO xFe+yCO2 xFe+yCO2 | ||
| 用途 | 用作油漆、涂料、油墨和橡胶的红色颜料 | ||
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某同学设计如下实验方案,来分离NaCl和BaCl2两种固体混合物,供选试剂:Na2SO4溶液、Na2CO3溶液、K2CO3溶液、盐酸

(1)操作②的名称是_______________________
(2)试剂a是__________________ ,试剂b是____________________
(3) 加入试剂b所发生反应的离子方程式为____________________________________________ 。

(1)操作②的名称是
(2)试剂a是
(3) 加入试剂b所发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】硫的多种化合物在工业中有重要的应用。
(1)连二亚硫酸钠(Na2S2O4)又称保险粉,是最适合木浆造纸的漂白剂,其水溶液性质不稳定,有极强的还原性。
①Na2S2O4中S元素的化合价为________ 。
②Na2S2O4暴露于空气中易吸收氧气和水蒸气而变质,发生反应时,当氧化剂和还原剂的物质的量之比为1∶2时,产物为________ (填化学式)。
③将甲酸和NaOH溶液混合,再通入SO2气体,会得到保险粉,此时甲酸被氧化为CO2,SO2气体被还原成Na2S2O4。该反应的化学方程式为______________
(2)铬会造成环境污染。某酸性废水中含有Cr2O72-,处理时可用焦亚硫酸钠(Na2S2O5)将Cr2O72-转化为毒性较低的Cr3+,再调节pH至8,使铬元素沉降,分离出污泥后测得废水中Cr3+浓度为0.52 mg·L-1,达到排放标准。
①Na2S2O5参加反应的离子方程式为_________
②处理后的废水中Cr3+的物质的量浓度为________ mol·L-1。
(1)连二亚硫酸钠(Na2S2O4)又称保险粉,是最适合木浆造纸的漂白剂,其水溶液性质不稳定,有极强的还原性。
①Na2S2O4中S元素的化合价为
②Na2S2O4暴露于空气中易吸收氧气和水蒸气而变质,发生反应时,当氧化剂和还原剂的物质的量之比为1∶2时,产物为
③将甲酸和NaOH溶液混合,再通入SO2气体,会得到保险粉,此时甲酸被氧化为CO2,SO2气体被还原成Na2S2O4。该反应的化学方程式为
(2)铬会造成环境污染。某酸性废水中含有Cr2O72-,处理时可用焦亚硫酸钠(Na2S2O5)将Cr2O72-转化为毒性较低的Cr3+,再调节pH至8,使铬元素沉降,分离出污泥后测得废水中Cr3+浓度为0.52 mg·L-1,达到排放标准。
①Na2S2O5参加反应的离子方程式为
②处理后的废水中Cr3+的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】物质的类别和核心元素的化合价是研究物质化学性质的两个重要角度。硫元素的价类二维图如图所示(其中h、g的阳离子均为 ),请回答下列问题:
),请回答下列问题:

(1)e的化学式是___________ 。
(2)实验室常用g和f的浓溶液制备气体c,写出其化学方程式___________ 。
(3)将气体c通入a的水溶液,溶液变浑浊,用化学方程式解释___________ ,体现了c的___________ 性。
(4)过量的铜与f的浓溶液在加热条件下可以发生,化学方程式为___________ ,反应后铜片有剩余,为使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如 溶液),则该反应的离子方程式为
溶液),则该反应的离子方程式为___________ 。
 ),请回答下列问题:
),请回答下列问题:
(1)e的化学式是
(2)实验室常用g和f的浓溶液制备气体c,写出其化学方程式
(3)将气体c通入a的水溶液,溶液变浑浊,用化学方程式解释
(4)过量的铜与f的浓溶液在加热条件下可以发生,化学方程式为
 溶液),则该反应的离子方程式为
溶液),则该反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据所学知识回答下列问题:
(1)氢化钠(NaH)可在野外作生氢剂,NaH中氢元素显 价。NaH用作生氢剂时的化学反应原理为NaH+H2O=NaOH+H2↑。该反应中体现了NaH的
价。NaH用作生氢剂时的化学反应原理为NaH+H2O=NaOH+H2↑。该反应中体现了NaH的_______ (填“氧化性”、“还原性”或“氧化性和还原性”)。
(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,反应原理为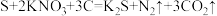 。
。
①该反应中,每生成7gN2,消耗S的质量为_______ g。
②还原产物为_______ (填化学式)。
③若将产生的气体全部通入足量的澄清石灰水中,发生反应的离子方程式为_______ 。
(3)含重铬酸根离子( )的工业废水有毒,必须经过处理达标后才能排放。工业上常用绿矾(FeSO4∙7H2O)作处理剂,发生反应的离子方程式为
)的工业废水有毒,必须经过处理达标后才能排放。工业上常用绿矾(FeSO4∙7H2O)作处理剂,发生反应的离子方程式为 。
。
① 中Cr元素的化合价为
中Cr元素的化合价为_______ 。
②还原性:Fe2+_______ (填“>”、“<”或“=”)Cr3+。
③该反应中,每生成33.6gFe3+,转移的电子数目为_______ 。
(1)氢化钠(NaH)可在野外作生氢剂,NaH中氢元素显
 价。NaH用作生氢剂时的化学反应原理为NaH+H2O=NaOH+H2↑。该反应中体现了NaH的
价。NaH用作生氢剂时的化学反应原理为NaH+H2O=NaOH+H2↑。该反应中体现了NaH的(2)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭粉按一定比例混合而成的,反应原理为
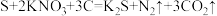 。
。①该反应中,每生成7gN2,消耗S的质量为
②还原产物为
③若将产生的气体全部通入足量的澄清石灰水中,发生反应的离子方程式为
(3)含重铬酸根离子(
 )的工业废水有毒,必须经过处理达标后才能排放。工业上常用绿矾(FeSO4∙7H2O)作处理剂,发生反应的离子方程式为
)的工业废水有毒,必须经过处理达标后才能排放。工业上常用绿矾(FeSO4∙7H2O)作处理剂,发生反应的离子方程式为 。
。①
 中Cr元素的化合价为
中Cr元素的化合价为②还原性:Fe2+
③该反应中,每生成33.6gFe3+,转移的电子数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】金属冶炼和处理常涉及氧化还原反应。
(1)由下列物质冶炼相应金属时采用电解法的是________ 。
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)辉铜矿(Cu2S)可用于火法炼铜:Cu2S+O2 2Cu+SO2,该反应的氧化剂是
2Cu+SO2,该反应的氧化剂是_______ ,当1mol O2发生反应时,还原剂所失电子的物质的量为________ mol。
(3)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有__________ 。
a.KCl b. KClO3 c. MnO2 d. Mg
书写出铝热反应的方程式:________________________________ 。
(4)反应TiCl4+2Mg 2MgCl2+Ti在Ar气氛中进行的理由是:
2MgCl2+Ti在Ar气氛中进行的理由是:___________ 。
(1)由下列物质冶炼相应金属时采用电解法的是
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)辉铜矿(Cu2S)可用于火法炼铜:Cu2S+O2
 2Cu+SO2,该反应的氧化剂是
2Cu+SO2,该反应的氧化剂是(3)用铝粉和Fe2O3做铝热反应实验,需要的试剂还有
a.KCl b. KClO3 c. MnO2 d. Mg
书写出铝热反应的方程式:
(4)反应TiCl4+2Mg
 2MgCl2+Ti在Ar气氛中进行的理由是:
2MgCl2+Ti在Ar气氛中进行的理由是:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】黑火药是我国古代四大发明之一,它的爆炸反应为:2KNO3+3C+S K2S+N2↑+3CO2↑
K2S+N2↑+3CO2↑
完成下列填空:
(1)上述反应中的还原剂为___ ,还原产物有___ ,当有1molKNO3参加反应时,转移电子的数目为___ 。
(2)KNO3晶体类型是___ ,其晶体中存在的化学键有___ 。
(3)硫原子的核外电子排布式为___ ,原子核外有___ 种不同能量的电子。将SO2和Cl2分别通入品红溶液中,产生的现象是___ ;若将SO2和Cl2等体积混合后再缓缓通入品红溶液,发现品红溶液___ ,其原因是___ 。
(4)S、C和N三种元素的原子半径从小到大的顺序是___ ;K2S溶液中除OH-外其它各离子物质的量浓度的大小顺序为___ 。
(5)下列事实能说明碳与硫两元素非金属性相对强弱的有___ 。
a.同温同浓度溶液pH:Na2CO3>Na2SO4
b.酸性:H2SO3>H2CO3
c.CS2中碳元素为+4价,硫元素为-2价
d.分解温度:CH4>H2S
 K2S+N2↑+3CO2↑
K2S+N2↑+3CO2↑完成下列填空:
(1)上述反应中的还原剂为
(2)KNO3晶体类型是
(3)硫原子的核外电子排布式为
(4)S、C和N三种元素的原子半径从小到大的顺序是
(5)下列事实能说明碳与硫两元素非金属性相对强弱的有
a.同温同浓度溶液pH:Na2CO3>Na2SO4
b.酸性:H2SO3>H2CO3
c.CS2中碳元素为+4价,硫元素为-2价
d.分解温度:CH4>H2S
您最近一年使用:0次

 CuCl2。反应中每生成1 mol CuCl2,消耗Cu的物质的量是
CuCl2。反应中每生成1 mol CuCl2,消耗Cu的物质的量是