一种生产高铁酸钾的流程如图所示,写出下列反应的离子方程式
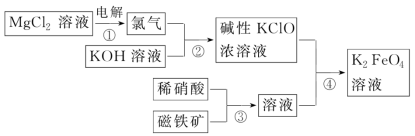
(1)反应①:_______
(2)反应②:_______
(3)反应③:_______
(4)反应④:_______

(1)反应①:
(2)反应②:
(3)反应③:
(4)反应④:
更新时间:2022-11-11 22:17:57
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】 在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与
在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与 反应,其化学方程式是
反应,其化学方程式是 。已知:稀
。已知:稀 溶液几乎无色。
溶液几乎无色。
(1)X的化学式是___________ 。
(2)用双线桥法标出,上述反应中电子转移的方向和数目___________ 。
(3)上述反应中的还原剂为___________ (填化学式),被还原的元素是___________ (填元素符号)。
(4)向酸性 溶液中滴入过量双氧水,观察到的现象是
溶液中滴入过量双氧水,观察到的现象是___________ ,反应后溶液的pH___________ (填“增大”“减小”或“不变”)。
(5)0.2mol 参加上述反应,转移电子
参加上述反应,转移电子___________ mol。
 在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与
在实验、医疗、化工等方面有广泛的应用。酸性高锰酸钾溶液可与 反应,其化学方程式是
反应,其化学方程式是 。已知:稀
。已知:稀 溶液几乎无色。
溶液几乎无色。(1)X的化学式是
(2)用双线桥法标出,上述反应中电子转移的方向和数目
(3)上述反应中的还原剂为
(4)向酸性
 溶液中滴入过量双氧水,观察到的现象是
溶液中滴入过量双氧水,观察到的现象是(5)0.2mol
 参加上述反应,转移电子
参加上述反应,转移电子
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铜、铬、锰均为过渡元素,其单质及化合物在工业,科技和生产中有着广泛的应用。
(1)Cu2S可用作制防污涂料、污水处理剂、催化剂等。
①灼烧Cu2S时,铜的焰色为________ (填序号)。
A.黄色B.砖红色C.紫色D.绿色
②用CuS、Cu2S处理酸性废水中的Cr2O 时发生的反应(未配平)如下
时发生的反应(未配平)如下
I.CuS+Cr2O +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O
+Cr3++H2O
II.Cu2S+Cr2O +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O
+Cr3++H2O
当消耗的CuS、Cu2S的个数相同时,两者去除Cr2O 的离子数之比为
的离子数之比为________ 。
(2)Cr2O3可用于冶金,也可用作陶瓷、耐火材料、颜料业原料及有机合成催化剂等。
①Cr2O3能与NaOH溶液反应生成NaCrO2,请写出Cr2O3与NaOH溶液反应的离子方程式:________ 。
②用碳还原K2Cr2O7可制备Cr2O3,同时生成一种可燃性有毒气体,当该反应中碳与K2Cr2O7的系数之比为2:1时,氧化产物的化学式为________ 。
(3)锰酸钾可用作皮革、纤维漂白剂以及杀菌剂、羊毛的媒染剂等。
①金属锰与熔融碱在氧化剂作用下生成锰酸钾,反应为2Mn+4KOH(熔融)+3O2=2K2MnO4+2H2O,若生成98.5gK2MnO4,则消耗O2的质量为________ 。
②在KOH溶液的环境中KMnO4溶液与Na2SO3反应可以制得K2MnO4,写出该反应的离子方程式________ 。
(1)Cu2S可用作制防污涂料、污水处理剂、催化剂等。
①灼烧Cu2S时,铜的焰色为
A.黄色B.砖红色C.紫色D.绿色
②用CuS、Cu2S处理酸性废水中的Cr2O
 时发生的反应(未配平)如下
时发生的反应(未配平)如下I.CuS+Cr2O
 +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O
+Cr3++H2OII.Cu2S+Cr2O
 +H+→Cu2++SO
+H+→Cu2++SO +Cr3++H2O
+Cr3++H2O当消耗的CuS、Cu2S的个数相同时,两者去除Cr2O
 的离子数之比为
的离子数之比为(2)Cr2O3可用于冶金,也可用作陶瓷、耐火材料、颜料业原料及有机合成催化剂等。
①Cr2O3能与NaOH溶液反应生成NaCrO2,请写出Cr2O3与NaOH溶液反应的离子方程式:
②用碳还原K2Cr2O7可制备Cr2O3,同时生成一种可燃性有毒气体,当该反应中碳与K2Cr2O7的系数之比为2:1时,氧化产物的化学式为
(3)锰酸钾可用作皮革、纤维漂白剂以及杀菌剂、羊毛的媒染剂等。
①金属锰与熔融碱在氧化剂作用下生成锰酸钾,反应为2Mn+4KOH(熔融)+3O2=2K2MnO4+2H2O,若生成98.5gK2MnO4,则消耗O2的质量为
②在KOH溶液的环境中KMnO4溶液与Na2SO3反应可以制得K2MnO4,写出该反应的离子方程式
您最近一年使用:0次
【推荐3】亚硝酸钠(NaNO2)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生Na2O、N2和O2,其水溶液呈碱性,能与AgNO3溶液反应生成难溶于水、易溶于酸的AgNO2。由于NaNO2有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
NaNO2+ KI+ = NO↑+ I2+ K2SO4+ Na2SO4+ H2O
(1)补充并配平该化学方程式___________ (若系数为1,请标注“1”)。
(2)从物质分类角度来看,NaNO2是___________ (填字母)。
a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质 f.离子化合物 g.共价化合物
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是___________ 。
(4)下列方法不能用来区分固体NaNO2和NaCl的是___________(填字母)。
(5)误食NaNO2会导致人体血红蛋白中的Fe2+转化为Fe3+而中毒,该过程中NaNO2表现出的性质与下列___________(填字母)反应中H2O2表现出的性质相同。
(6)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学方程式,并用单线桥表示其电子转移的方向和数目:___________ 。
NaNO2+ KI+ = NO↑+ I2+ K2SO4+ Na2SO4+ H2O
(1)补充并配平该化学方程式
(2)从物质分类角度来看,NaNO2是
a.酸 b.酸式盐 c.碱 d.非电解质 e.电解质 f.离子化合物 g.共价化合物
(3)用上述反应来处理NaNO2并不是最佳方法,其原因是
(4)下列方法不能用来区分固体NaNO2和NaCl的是___________(填字母)。
| A.分别溶于水 |
| B.分别溶于水并滴加HNO3酸化的AgNO3溶液 |
| C.分别加强热并收集气体检验 |
| D.用筷子分别蘸取固体品尝味道 |
A.2H2O2 2H2O+O2↑ 2H2O+O2↑ |
| B.H2O2+Cl2=2HCl+O2↑ |
| C.H2O2+H2SO4+2KI=2H2O+I2+K2SO4 |
| D.5H2O2+2KMnO4+6HCl=2MnCl2+2KCl+5O2↑+8H2O |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】消毒剂在生产生活中有极其重要的作用。
(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量上述物质消毒效率最高的是________ (填序号)。
A.Cl2 B.H2O2 C.ClO2 D.O3
(2)H2O2可作为废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O=A+NH3↑,则生成物A的化学式为_______________________ ,H2O2被称为“绿色氧化剂”的理由是____________________________ 。
(3)漂白剂亚氯酸钠(NaClO2)在常温、黑暗处可保存一年。亚氯酸不稳定,可分解,反应的离子方程式为HClO2→ClO2↑+H++Cl-+H2O(未配平)。在该反应中,当有1 mol ClO2生成时转移的电子个数约为________ 。
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是_______ (用离子方程式表示)。
(1)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1 mol O3转化为1 mol O2和1 mol H2O)等物质常被用作消毒剂。等物质的量上述物质消毒效率最高的是
A.Cl2 B.H2O2 C.ClO2 D.O3
(2)H2O2可作为废液消毒剂,有“绿色氧化剂”的美称。如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O2+H2O=A+NH3↑,则生成物A的化学式为
(3)漂白剂亚氯酸钠(NaClO2)在常温、黑暗处可保存一年。亚氯酸不稳定,可分解,反应的离子方程式为HClO2→ClO2↑+H++Cl-+H2O(未配平)。在该反应中,当有1 mol ClO2生成时转移的电子个数约为
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】新型冠状病毒蔓延期间,为做好自我保护,我们要减少外出,避免与表现出有呼吸道疾病症状的人密切接触,外出最重要的防护措施是佩戴符合要求的口罩。在生活中常见的口罩一般有棉布口罩、医用外科口罩、活性炭口罩和N95口罩。也可以在实验室进行制备84消毒液(有效成分是NaClO)。
(1)新型冠状病毒可以通过气溶胶传播,气溶胶属于分散系中的_______ (“溶液”、“胶体”、“悬浊液”)。
(2)佩戴口罩预防疾病的原理相当于化学实验中的_______ 操作。(“蒸发”、“过滤”“萃取”)
(3)生成N95口罩的主要原料是聚丙烯,它属于_________ (填“金属材料”或“合成材料”)
(4)如图是模拟84消毒液的装置,实验室先制备氯气,再通入氢氧化钠溶液,写出发生的化学反应方程式:________ 。

(5)84消毒液和洁厕灵混合使用时会发生化学反应2HCl+NaClO=NaCl+H2O+X↑,使消毒液失效,杀菌消毒能力减弱,易发生生命危险,X为____ 。
(1)新型冠状病毒可以通过气溶胶传播,气溶胶属于分散系中的
(2)佩戴口罩预防疾病的原理相当于化学实验中的
(3)生成N95口罩的主要原料是聚丙烯,它属于
(4)如图是模拟84消毒液的装置,实验室先制备氯气,再通入氢氧化钠溶液,写出发生的化学反应方程式:

(5)84消毒液和洁厕灵混合使用时会发生化学反应2HCl+NaClO=NaCl+H2O+X↑,使消毒液失效,杀菌消毒能力减弱,易发生生命危险,X为
您最近一年使用:0次
【推荐3】化学与人类生活密切相关。请按要求回答下列问题:
(1)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3+3Cl2+10KOH=2K2FeO4+6KCl+8H2O。在该反应中,还原剂是___ ,当反应中有0.5molK2FeO4生成时,消耗Cl2在标况下的体积为____ ,转移电子的数目为___ 。
(2)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式_______ 。
(3)工业上制漂白粉的化学方程式为___ ,新制氯水在阳光照射下产生无色气体,该反应的化学方程式是___ 。
(4)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:___ 。若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是___ 。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
(1)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3+3Cl2+10KOH=2K2FeO4+6KCl+8H2O。在该反应中,还原剂是
(2)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式
(3)工业上制漂白粉的化学方程式为
(4)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】甲、乙两池电极材料如图所示,请按要求回答下列问题:

(1)若两池中均为Cu(NO3)2溶液,反应一段时间后:
①有红色物质析出的是甲池中的______ 棒(铁、碳);
②乙池碳极上电极反应属于______ (填氧化反应、还原反应)。
③乙池中阳极上发生的电极反应方程式是______ 。
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的化学方程式______ 。
②甲池中碳极上电极反应方程式是______ 。
③若乙池中饱和NaCl溶液100 mL一段时间后在阴极得到112 mL(标准状况)H2,此时乙池溶液的(体积变化忽略不计)pH为______
(3)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①阳电极的材料是______
②阴极反应式是______ 。(说明:杂质发生的电极反应不必写出)

(1)若两池中均为Cu(NO3)2溶液,反应一段时间后:
①有红色物质析出的是甲池中的
②乙池碳极上电极反应属于
③乙池中阳极上发生的电极反应方程式是
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的化学方程式
②甲池中碳极上电极反应方程式是
③若乙池中饱和NaCl溶液100 mL一段时间后在阴极得到112 mL(标准状况)H2,此时乙池溶液的(体积变化忽略不计)pH为
(3)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则:
①阳电极的材料是
②阴极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电解装置如图所示:
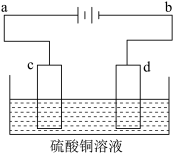
(1)当用惰性电极电解时,c为____________ 极,电极反应________ d为____________ 极,电极反应______________ ,电解总反应的化学方程____________________
(2)①若用此装置进行铁上镀铜则c为__________ (填铁或铜)d为___________ (填铁或铜)电解液浓度_____________ (增大,减小或不变)
②电镀一段时间后对电极进行称量发现两极质量差为16克,则电路中转移的电子___________ mol.
(3)若用此装置进行粗铜的电解精炼。则要求粗铜板是图中电极________ (填图中的字母);若粗铜中还含有Au、Ag、Fe,则Fe以_______ (填离子符号)形式进入溶液,c电极发生的反应______________ ,________________ 。

(1)当用惰性电极电解时,c为
(2)①若用此装置进行铁上镀铜则c为
②电镀一段时间后对电极进行称量发现两极质量差为16克,则电路中转移的电子
(3)若用此装置进行粗铜的电解精炼。则要求粗铜板是图中电极
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】原电池是化学对人类的一项重大贡献。回答下列问题:
(1)铁是用途最广的金属材料之一,但生铁易生锈。请讨论电化学实验中有关铁的性质。
①某原电池装置如图所示,右侧烧杯中的电极反应式为___________ 。
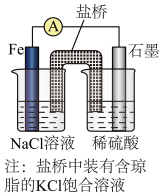
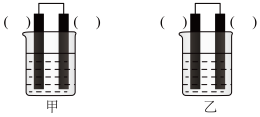
②已知下图甲、乙两池的总反应式均为Fe+H2SO4=FeSO4+H2↑,且在同侧电极(指均在“左电极”或“右电极”)产生H2。请在两池上标出电极材料___________ (填“Fe”或“C”)。
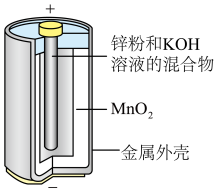
(2)碱性锌锰干电池的剖面图如图所示,已知电池放电后的产物是Zn(OH)2和MnOOH,则其总反应式为___________ ,负极电极反应式为___________ 。
(3)用高铁(Ⅵ)酸盐设计的高铁(Ⅵ)电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应为3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH。
①写出正极电极反应式:___________ 。
②用高铁(Ⅵ)电池作电源,以Fe作阳极,以Cu作阴极,对足量KOH溶液进行电解,当电池中有0.2 mol K2FeO4反应时,则在电解池中生成___________ L(标准状况) H2。
(1)铁是用途最广的金属材料之一,但生铁易生锈。请讨论电化学实验中有关铁的性质。
①某原电池装置如图所示,右侧烧杯中的电极反应式为

②已知下图甲、乙两池的总反应式均为Fe+H2SO4=FeSO4+H2↑,且在同侧电极(指均在“左电极”或“右电极”)产生H2。请在两池上标出电极材料

(2)碱性锌锰干电池的剖面图如图所示,已知电池放电后的产物是Zn(OH)2和MnOOH,则其总反应式为

(3)用高铁(Ⅵ)酸盐设计的高铁(Ⅵ)电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应为3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH。
①写出正极电极反应式:
②用高铁(Ⅵ)电池作电源,以Fe作阳极,以Cu作阴极,对足量KOH溶液进行电解,当电池中有0.2 mol K2FeO4反应时,则在电解池中生成
您最近一年使用:0次



