五氟化锑主要用作氟化工的催化剂,也用作纺织工业物阻燃剂,在染料工业中用于制造染料中间体,此外,还用于制备高纯度金属锑、无机离子交换材料和胶体五氧化二锑。以某锑矿(主要成分为 ,含有少量
,含有少量 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如下图:
的工艺流程如下图:
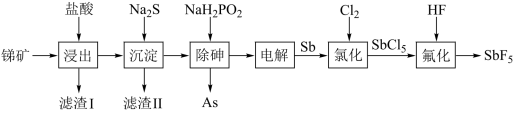
已知:Ⅰ. 、
、 的
的 分别为
分别为 、
、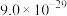 ;
;
Ⅱ. 微溶于水、
微溶于水、 难溶于水,它们均为两性氧化物;
难溶于水,它们均为两性氧化物; 难溶于水。
难溶于水。
回答下列问题:
(1)已知锑与氮元同素主族,原子序数为51,写出锑的价电子排布图_______ 。
(2)“浸出”时少量 转化为“滤渣1”。其成分为
转化为“滤渣1”。其成分为 ,加入氨水“除氯”,同时将其转化为
,加入氨水“除氯”,同时将其转化为 ,能否用
,能否用 溶液代替氨水
溶液代替氨水_______ ,(填“能”或“否”),原因是_______ 。
(3)“沉淀”的过程是加入极稀的 溶液,其目的是使
溶液,其目的是使 和
和 转化为相应的硫化物而除去,当
转化为相应的硫化物而除去,当 、
、 共沉时,
共沉时,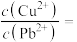
_______ 。
(4)“除砷”时, 转化为H3PO4,该反应中氧化剂和还原剂的物质的量比是
转化为H3PO4,该反应中氧化剂和还原剂的物质的量比是_______ 。
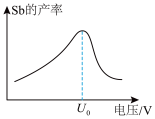
(5)“电解”中锑的产率与电压大小关系如下图所示。当电压未超过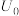 V时,阴极反应方程式为
V时,阴极反应方程式为
 ,当电压超过
,当电压超过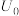 V时,锑的产率降低,阴极还可能发生了
V时,锑的产率降低,阴极还可能发生了_______ 反应。(写出电极反应式)
(6) 与
与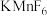 反应。首次实现了用化学方法制取
反应。首次实现了用化学方法制取 ,同时生成
,同时生成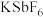 和
和 ,化学反应方程式为
,化学反应方程式为_______ 。
 ,含有少量
,含有少量 、
、 、
、 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如下图:
的工艺流程如下图:
已知:Ⅰ.
 、
、 的
的 分别为
分别为 、
、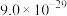 ;
;Ⅱ.
 微溶于水、
微溶于水、 难溶于水,它们均为两性氧化物;
难溶于水,它们均为两性氧化物; 难溶于水。
难溶于水。回答下列问题:
(1)已知锑与氮元同素主族,原子序数为51,写出锑的价电子排布图
(2)“浸出”时少量
 转化为“滤渣1”。其成分为
转化为“滤渣1”。其成分为 ,加入氨水“除氯”,同时将其转化为
,加入氨水“除氯”,同时将其转化为 ,能否用
,能否用 溶液代替氨水
溶液代替氨水(3)“沉淀”的过程是加入极稀的
 溶液,其目的是使
溶液,其目的是使 和
和 转化为相应的硫化物而除去,当
转化为相应的硫化物而除去,当 、
、 共沉时,
共沉时,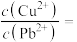
(4)“除砷”时,
 转化为H3PO4,该反应中氧化剂和还原剂的物质的量比是
转化为H3PO4,该反应中氧化剂和还原剂的物质的量比是(5)“电解”中锑的产率与电压大小关系如下图所示。当电压未超过
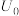 V时,阴极反应方程式为
V时,阴极反应方程式为
 ,当电压超过
,当电压超过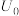 V时,锑的产率降低,阴极还可能发生了
V时,锑的产率降低,阴极还可能发生了
(6)
 与
与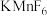 反应。首次实现了用化学方法制取
反应。首次实现了用化学方法制取 ,同时生成
,同时生成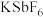 和
和 ,化学反应方程式为
,化学反应方程式为
2024·吉林·模拟预测 查看更多[2]
吉林省东北师范大学附属中学、长春市十一高中、吉林市第一中学、四平一中、松原实验中学2023-2024学年高三上学期1月联合模拟考试化学试题(已下线)专题08 工艺流程综合题-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)
更新时间:2024-02-17 21:12:55
|
相似题推荐
【推荐1】I.磷化铝(AlP)和磷化氢(PH3)都是粮食储备常用的高效熏蒸杀虫剂。
(1)磷元素位于元素周期表第_______ 周期______ 族。AlP遇水蒸气会发生反应放出PH3气体,该反应的另一种产物的化学式为____________ 。
(2)PH3具有强还原性,能与CuSO4溶液反应,配平该反应的化学方程式:________
□CuSO4+□PH3+□H2O═□Cu3P↓+□H3PO4+□H2SO4
(3)工业制备PH3的流程如图所示。
①黄磷和烧碱溶液反应的化学方程式为_________ ,次磷酸的化学式为____________ ,次磷酸属于___________ (填“一”“二”或“三”)元酸。
②若起始时有1molP4参加反应,则整个工业流程中共生成______ mol PH3.(不考虑产物的损失)
II.某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图所示,电极材料为石墨。
①a表示__________ 离子交换膜(填“阴”或“阳”)。A-E分别代表生产中的原料或产品。其中C为硫酸,则A表示_____________ 。E表示___________________ 。
②阳极的电极反应式为________________________________ 。
(1)磷元素位于元素周期表第
(2)PH3具有强还原性,能与CuSO4溶液反应,配平该反应的化学方程式:
□CuSO4+□PH3+□H2O═□Cu3P↓+□H3PO4+□H2SO4
(3)工业制备PH3的流程如图所示。

①黄磷和烧碱溶液反应的化学方程式为
②若起始时有1molP4参加反应,则整个工业流程中共生成
II.某研究小组用NaOH溶液吸收尾气中的二氧化硫,将得到的Na2SO3溶液进行电解,其中阴阳膜组合电解装置如图所示,电极材料为石墨。

①a表示
②阳极的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】金属钼在工业和国防建设中有重要的作用。钼(Mo)的常见化合价为+6、+5、+4。由钼精矿(主要成分是MoS2)可制备单质钼和钼酸钠晶体(Na2MoO4·2H2O),部分流程如图所示:
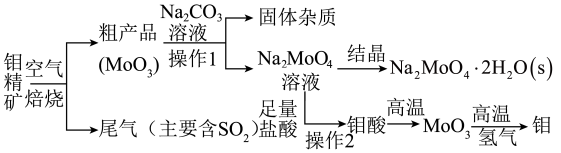
已知:钼酸微溶于水,可溶于碱液和氨水。回答下列问题:
(1)钼精矿焙烧时,每有1 mol MoS2反应,转移电子的物质的量为________ 。
(2)钼精矿焙烧时排放的尾气对环境的主要危害是__________ ,请你提出一种实验室除去该尾气的方法_______ 。
(3)操作2的名称为________ 。由钼酸得到MoO3所用到的硅酸盐材料仪器的名称是________ 。
(4)操作1中,加入碳酸钠溶液充分反应后,碱浸液中c(MoO )=0.80 mol·L-1,c(SO
)=0.80 mol·L-1,c(SO )=0.04 mol·L-1,在结晶前需加入Ba(OH)2固体以除去溶液中的SO
)=0.04 mol·L-1,在结晶前需加入Ba(OH)2固体以除去溶液中的SO 。当BaMoO4开始沉淀时,SO
。当BaMoO4开始沉淀时,SO 的去除率是
的去除率是________ 。[Ksp(BaSO4)=1.1×10-10、Ksp(BaMoO4)=4.0×10-8,溶液体积变化可忽略不计]
(5)焙烧钼精矿所用的装置是多层焙烧炉,如图为各炉层固体物料的物质的量的百分数(φ)。

①x=________ 。
②焙烧炉中也会发生MoS2与MoO3反应生成MoO2和SO2的反应,若该反应转移6 mol电子,则消耗的氧化剂的化学式及物质的量分别为________ 、________ 。

已知:钼酸微溶于水,可溶于碱液和氨水。回答下列问题:
(1)钼精矿焙烧时,每有1 mol MoS2反应,转移电子的物质的量为
(2)钼精矿焙烧时排放的尾气对环境的主要危害是
(3)操作2的名称为
(4)操作1中,加入碳酸钠溶液充分反应后,碱浸液中c(MoO
 )=0.80 mol·L-1,c(SO
)=0.80 mol·L-1,c(SO )=0.04 mol·L-1,在结晶前需加入Ba(OH)2固体以除去溶液中的SO
)=0.04 mol·L-1,在结晶前需加入Ba(OH)2固体以除去溶液中的SO 。当BaMoO4开始沉淀时,SO
。当BaMoO4开始沉淀时,SO 的去除率是
的去除率是(5)焙烧钼精矿所用的装置是多层焙烧炉,如图为各炉层固体物料的物质的量的百分数(φ)。

①x=
②焙烧炉中也会发生MoS2与MoO3反应生成MoO2和SO2的反应,若该反应转移6 mol电子,则消耗的氧化剂的化学式及物质的量分别为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】CH4既是一种重要的能源,也是一种重要的化工原料。
(1)已知8.0gCH4完全燃烧生成液体水放出444.8kJ热量。
CH4(g)+202(g)=CO2(g)+2H2O(1) ∆H=___________ kJ·mol-1。
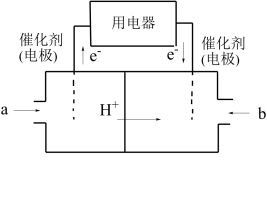
(2)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,则通入a气体的电极名称为___________ ,通入b气体的电极反应式为___________ 。(质子交换膜只允许H'通过)___________ ℃左右。
②该反应催化剂的有效成分为CuAlO2,其用氧化物的形式表示为mCu2O·nAl2O3.m:n=___________ 。
(4)CH4还原法是处理NOx气体的一种方法。一定条件下CH4与NOx反应转化为N2和CO2,若标准状况下8.96LCH4可处理22.4LNOx,则x值为___________ 。
(1)已知8.0gCH4完全燃烧生成液体水放出444.8kJ热量。
CH4(g)+202(g)=CO2(g)+2H2O(1) ∆H=
(2)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理如图所示,则通入a气体的电极名称为
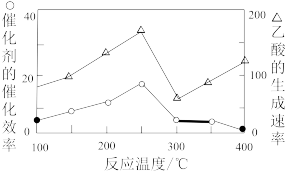
②该反应催化剂的有效成分为CuAlO2,其用氧化物的形式表示为mCu2O·nAl2O3.m:n=
(4)CH4还原法是处理NOx气体的一种方法。一定条件下CH4与NOx反应转化为N2和CO2,若标准状况下8.96LCH4可处理22.4LNOx,则x值为
您最近一年使用:0次
【推荐1】某电镀厂的酸性废液中含 、
、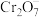 、
、 、
、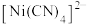 等离子,须处理后排放。
等离子,须处理后排放。
(1)除 、
、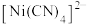 。向废液中加入熟石灰调节
。向废液中加入熟石灰调节 ,再加入
,再加入 溶液,可将
溶液,可将 氧化为
氧化为 和
和 ,其离子方程式为
,其离子方程式为___________ 。加入 可以促进
可以促进 元素转化为
元素转化为 沉淀除去,原因是
沉淀除去,原因是___________ 。
(2)沉淀法回收 (Ⅵ)。已知:
(Ⅵ)。已知: 和
和 微溶于水,
微溶于水,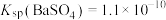 ,
,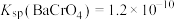 。
。
①向除去 和
和 元素的废液中加入一定量的
元素的废液中加入一定量的 ,可将
,可将 (Ⅵ)转化为
(Ⅵ)转化为 沉淀。相同时间内,
沉淀。相同时间内, 元素沉淀率与溶液初始
元素沉淀率与溶液初始 的关系如图所示。与
的关系如图所示。与 相比,初始
相比,初始 时
时 (Ⅵ)去除率较高的原因是
(Ⅵ)去除率较高的原因是___________ 。 沉淀中混有
沉淀中混有 等杂质,可加入足量硫酸充分反应后过滤,实现
等杂质,可加入足量硫酸充分反应后过滤,实现 (Ⅵ)的分离回收,反应的离子方程式为
(Ⅵ)的分离回收,反应的离子方程式为___________ 。
(3)电解法除 (VI)的一种装置如图所示。利用阳极生成的
(VI)的一种装置如图所示。利用阳极生成的 ,还原
,还原 (VI)生成
(VI)生成 ,最终转化为
,最终转化为 和
和 沉淀除去。
沉淀除去。 的钝化膜,电解效率降低。将电源正负极反接一段时间,钝化膜消失。钝化膜消失的原因为
的钝化膜,电解效率降低。将电源正负极反接一段时间,钝化膜消失。钝化膜消失的原因为___________ 。
②电解时,若维持电流强度为5A,电流效率为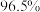 ,除去废水中
,除去废水中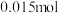 的
的 ,至少需要电解
,至少需要电解___________ 小时(写出计算过程)。
(已知:电流效率( )
)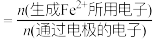 ;
; 。)
。)
 、
、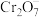 、
、 、
、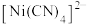 等离子,须处理后排放。
等离子,须处理后排放。(1)除
 、
、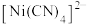 。向废液中加入熟石灰调节
。向废液中加入熟石灰调节 ,再加入
,再加入 溶液,可将
溶液,可将 氧化为
氧化为 和
和 ,其离子方程式为
,其离子方程式为 可以促进
可以促进 元素转化为
元素转化为 沉淀除去,原因是
沉淀除去,原因是(2)沉淀法回收
 (Ⅵ)。已知:
(Ⅵ)。已知: 和
和 微溶于水,
微溶于水,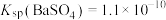 ,
,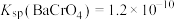 。
。①向除去
 和
和 元素的废液中加入一定量的
元素的废液中加入一定量的 ,可将
,可将 (Ⅵ)转化为
(Ⅵ)转化为 沉淀。相同时间内,
沉淀。相同时间内, 元素沉淀率与溶液初始
元素沉淀率与溶液初始 的关系如图所示。与
的关系如图所示。与 相比,初始
相比,初始 时
时 (Ⅵ)去除率较高的原因是
(Ⅵ)去除率较高的原因是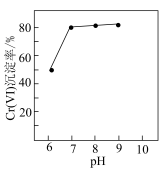
 沉淀中混有
沉淀中混有 等杂质,可加入足量硫酸充分反应后过滤,实现
等杂质,可加入足量硫酸充分反应后过滤,实现 (Ⅵ)的分离回收,反应的离子方程式为
(Ⅵ)的分离回收,反应的离子方程式为(3)电解法除
 (VI)的一种装置如图所示。利用阳极生成的
(VI)的一种装置如图所示。利用阳极生成的 ,还原
,还原 (VI)生成
(VI)生成 ,最终转化为
,最终转化为 和
和 沉淀除去。
沉淀除去。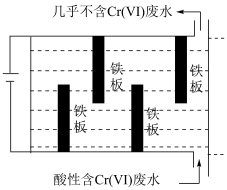
 的钝化膜,电解效率降低。将电源正负极反接一段时间,钝化膜消失。钝化膜消失的原因为
的钝化膜,电解效率降低。将电源正负极反接一段时间,钝化膜消失。钝化膜消失的原因为②电解时,若维持电流强度为5A,电流效率为
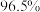 ,除去废水中
,除去废水中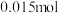 的
的 ,至少需要电解
,至少需要电解(已知:电流效率(
 )
)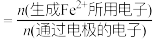 ;
; 。)
。)
您最近一年使用:0次
【推荐2】我国对世界郑重承诺:2030年前实现碳达峰,2060年前实现碳中和,而研发CO2的碳捕捉和碳利用技术则是关键。
(1)大气中的CO2主要来自于煤、石油及其他含碳化合物的燃烧,CH4与CO2重整是CO2利用的研究热点之一。该重整反应体系主要涉及以下反应:
①CH4(g) C(s)+2H2(g) ΔH1=akJ•mol-1
C(s)+2H2(g) ΔH1=akJ•mol-1
②CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=bkJ•mol-1
CO(g)+H2O(g) ΔH2=bkJ•mol-1
③2CO(g) CO2(g)+C(s) ΔH3=ckJ•mol-1
CO2(g)+C(s) ΔH3=ckJ•mol-1
反应CH4(g)+CO2(g) 2CO(g)+2H2(g)的ΔH=
2CO(g)+2H2(g)的ΔH=_____ kJ•mol-1。
(2)多晶Cu是目前唯一被实验证实能高效催化CO2还原为烃类(如C2H4)的金属。如图所示,电解装置中分别以多晶Cu和Pt为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后KHCO3浓度基本保持不变,温度控制在10℃左右。生成C2H4的电极反应式为_____ 。

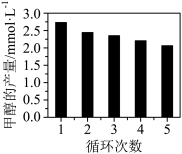
(3)CO2与H2反应如果用Co/C作为催化剂,可以得到含有少量甲酸的甲醇。为了研究催化剂的催化效率,将Co/C催化剂循环使用,相同条件下,随着循环使用次数的增加,甲醇的产量如图所示,试推测甲醇产量变化的可能原因_____ 。
(4)常温下,以NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。用1LNa2CO3溶液将2.33gBaSO4固体全都转化为BaCO3,再过滤,所用的Na2CO3溶液的物质的量浓度至少为_____ mol•L-1。[已知:常温下Ksp(BaSO4)=1×10-11,Ksp(BaCO3)=1×10-10;忽略溶液体积变化]
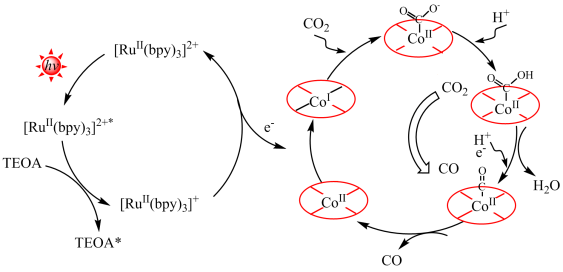
(5)某课题组通过温和的自光刻技术制备出富含氧空位的Co(CO3)0.5(OH)•0.11H2O纳米线(用CoII表示),测试结果表明,该CoII在可见光下具有优异的光催化CO2还原活性。分析表明,该CO2还原催化机理为典型的CoII/CoI反应路径(如图)。首先,光敏剂([Ru(bpy)3]2+)通过可见光照射被激发到激发态([Ru(bpy)3]2+*),随后([Ru(bpy)3]2+*)被TEOA淬灭得到([Ru(bpy)3]+)还原物种,该还原物种将向CoII供激发电子将CoII还原为CoI,_____ 。(结合图示,描述CO2还原为CO的过程)
(1)大气中的CO2主要来自于煤、石油及其他含碳化合物的燃烧,CH4与CO2重整是CO2利用的研究热点之一。该重整反应体系主要涉及以下反应:
①CH4(g)
 C(s)+2H2(g) ΔH1=akJ•mol-1
C(s)+2H2(g) ΔH1=akJ•mol-1②CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=bkJ•mol-1
CO(g)+H2O(g) ΔH2=bkJ•mol-1③2CO(g)
 CO2(g)+C(s) ΔH3=ckJ•mol-1
CO2(g)+C(s) ΔH3=ckJ•mol-1反应CH4(g)+CO2(g)
 2CO(g)+2H2(g)的ΔH=
2CO(g)+2H2(g)的ΔH=(2)多晶Cu是目前唯一被实验证实能高效催化CO2还原为烃类(如C2H4)的金属。如图所示,电解装置中分别以多晶Cu和Pt为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后KHCO3浓度基本保持不变,温度控制在10℃左右。生成C2H4的电极反应式为

(3)CO2与H2反应如果用Co/C作为催化剂,可以得到含有少量甲酸的甲醇。为了研究催化剂的催化效率,将Co/C催化剂循环使用,相同条件下,随着循环使用次数的增加,甲醇的产量如图所示,试推测甲醇产量变化的可能原因

(4)常温下,以NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。用1LNa2CO3溶液将2.33gBaSO4固体全都转化为BaCO3,再过滤,所用的Na2CO3溶液的物质的量浓度至少为
(5)某课题组通过温和的自光刻技术制备出富含氧空位的Co(CO3)0.5(OH)•0.11H2O纳米线(用CoII表示),测试结果表明,该CoII在可见光下具有优异的光催化CO2还原活性。分析表明,该CO2还原催化机理为典型的CoII/CoI反应路径(如图)。首先,光敏剂([Ru(bpy)3]2+)通过可见光照射被激发到激发态([Ru(bpy)3]2+*),随后([Ru(bpy)3]2+*)被TEOA淬灭得到([Ru(bpy)3]+)还原物种,该还原物种将向CoII供激发电子将CoII还原为CoI,

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】以湿法炼锌厂所产的钴锰渣(主要成分为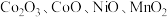 ,含少量
,含少量
 等)为原料回收制备
等)为原料回收制备 的工艺如下:
的工艺如下: ;
;
回答下列问题:
(1)“酸浸”时其中 ,写出
,写出 反应的化学方程式:
反应的化学方程式:___________ ,滤渣1中的硫酸盐是___________ 。
(2)“除铁”时,生成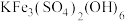 的离子方程式为
的离子方程式为___________ 。
(3)“除铜锌”时, 主要以
主要以___________ [填“ ”或“
”或“ ”]形式除去,其原因是
”]形式除去,其原因是___________ (反应平衡常数 视为反应完全,根据已知信息,写出推理过程)。
视为反应完全,根据已知信息,写出推理过程)。
(4)“滤渣3”中含有MnO2,写出“除锰”时生成MnO2的化学方程式:___________ 。
(5)P204、P507对金属离子的萃取率与 的关系如图所示。
的关系如图所示。___________ 。
②“P507萃取”时,选择合适的pH范围为___________ (填字母)。
A.3~4 B.4~5 C.5~6 D.6~7
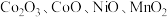 ,含少量
,含少量
 等)为原料回收制备
等)为原料回收制备 的工艺如下:
的工艺如下:
 ;
;回答下列问题:
(1)“酸浸”时其中
 ,写出
,写出 反应的化学方程式:
反应的化学方程式:(2)“除铁”时,生成
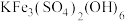 的离子方程式为
的离子方程式为(3)“除铜锌”时,
 主要以
主要以 ”或“
”或“ ”]形式除去,其原因是
”]形式除去,其原因是 视为反应完全,根据已知信息,写出推理过程)。
视为反应完全,根据已知信息,写出推理过程)。(4)“滤渣3”中含有MnO2,写出“除锰”时生成MnO2的化学方程式:
(5)P204、P507对金属离子的萃取率与
 的关系如图所示。
的关系如图所示。
②“P507萃取”时,选择合适的pH范围为
A.3~4 B.4~5 C.5~6 D.6~7
您最近一年使用:0次
【推荐1】羰基硫(COS)主要存在于煤、石油和天然气中,会造成设备腐蚀、环境污染,更危害人体健康。目前,我国已经实现了在催化剂(γ-Al2O3)、低温条件下的精度脱除COS,如图为天然气中脱除COS反应流化床示意图:

(1)①已知:H2(g)+COS(g) H2S(g)+CO(g) △H1=+6.2kJ•mol-1
H2S(g)+CO(g) △H1=+6.2kJ•mol-1
H2(g)+CO2(g) H2O(g)+CO(g) △H2=+41.2kJ•mol-1
H2O(g)+CO(g) △H2=+41.2kJ•mol-1
则COS精度脱除反应H2O(g)+COS(g) H2S(g)+CO2(g)的△H=
H2S(g)+CO2(g)的△H=__ kJ•mol-1。
②将H2O与COS以体积比1:2置于恒温恒容密闭容器中反应,若测得该反应平衡时H2O与COS的体积比1:6,则该温度下,脱除反应的平衡常数K=__ (保留两位小数)。
(2)T℃时,以一定流速、不同物质的量的H2O(g)和COS(g)通过流化床,测得COS(g)脱除速率变化关系如图。

已知:COS脱除反应机理如下,其中吸附在催化剂表面的物种用*标注。
a.吸附:H2O→H2O*
b.反应:COS+H2O*→CO2+H2S*
c.脱附:H2S*→H2S
①若COS(g)脱除速率v=knx(COS)•ny(H2O)(mol•min-1),由图中的数据可算出x、k的值:x=__ ,k=__ 。
②“吸附”步骤为__ (填“快反应”或“慢反应”),理由是__ 。
③脱除反应的决速步骤为__ (填“a”、“b”或“c”)。
④少量氢气可以抑制催化剂积硫(S*)中毒,分析该流化床中可能存在的可逆反应是__ 。
(3)工业上常采用下图所示电解装置,将气态废弃物中的硫化氢转化为可利用的硫。首先通电电解K4[Fe(CN)6]与KHCO3的混合溶液,通电一段时间后,再向所得溶液通入H2S时发生反应的离子方程式为2[Fe(CN)6]3-+2CO32-+H2S═2[Fe(CN)6]4-+2HCO3-+S↓.电解过程中阴极区电极反应式为_ 。


(1)①已知:H2(g)+COS(g)
 H2S(g)+CO(g) △H1=+6.2kJ•mol-1
H2S(g)+CO(g) △H1=+6.2kJ•mol-1H2(g)+CO2(g)
 H2O(g)+CO(g) △H2=+41.2kJ•mol-1
H2O(g)+CO(g) △H2=+41.2kJ•mol-1则COS精度脱除反应H2O(g)+COS(g)
 H2S(g)+CO2(g)的△H=
H2S(g)+CO2(g)的△H=②将H2O与COS以体积比1:2置于恒温恒容密闭容器中反应,若测得该反应平衡时H2O与COS的体积比1:6,则该温度下,脱除反应的平衡常数K=
(2)T℃时,以一定流速、不同物质的量的H2O(g)和COS(g)通过流化床,测得COS(g)脱除速率变化关系如图。

已知:COS脱除反应机理如下,其中吸附在催化剂表面的物种用*标注。
a.吸附:H2O→H2O*
b.反应:COS+H2O*→CO2+H2S*
c.脱附:H2S*→H2S
①若COS(g)脱除速率v=knx(COS)•ny(H2O)(mol•min-1),由图中的数据可算出x、k的值:x=
②“吸附”步骤为
③脱除反应的决速步骤为
④少量氢气可以抑制催化剂积硫(S*)中毒,分析该流化床中可能存在的可逆反应是
(3)工业上常采用下图所示电解装置,将气态废弃物中的硫化氢转化为可利用的硫。首先通电电解K4[Fe(CN)6]与KHCO3的混合溶液,通电一段时间后,再向所得溶液通入H2S时发生反应的离子方程式为2[Fe(CN)6]3-+2CO32-+H2S═2[Fe(CN)6]4-+2HCO3-+S↓.电解过程中阴极区电极反应式为

您最近一年使用:0次
【推荐2】完成下列问题
(1)已知:
反应Ⅰ:N2(g)+O2(g) 2NO(g) ΔH1=akJ/mol
2NO(g) ΔH1=akJ/mol
反应Ⅱ;2NO(g)+O2(g) 2NO2(g) ΔH2=bkJ/mol
2NO2(g) ΔH2=bkJ/mol
反应Ⅲ:2N2O(g) 2N2(g)+O2(g) ΔH3=ckJ/mol
2N2(g)+O2(g) ΔH3=ckJ/mol
反应Ⅳ:N2O(g)+NO2(g) 3NO(g) ΔH=
3NO(g) ΔH=___________ kJ/mol
(2)汽车尾气中的NO和CO可在催化剂作用下生成无污染的气体。在密闭容器中充入反应物,测得平衡时NO的体积分数与温度、压强的关系如图。
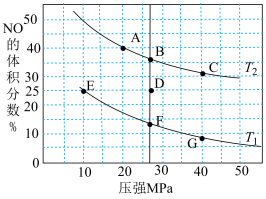
①反应2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH<0,则T1
N2(g)+2CO2(g) ΔH<0,则T1___________ T2(填“>”“=”或“<”)
②该反应达到平衡后,为同时提高反应速率和NO的转化率,可采取的措施有___________ (答两点即可)。
③在D点,对反应容器降温的同时缩小体积至体系压强增大,重新达到的平衡状态可能是图中A~G点中的___________ 点。
(3)在催化剂作用下,利用反应C(s)+2NO(g) N2(g)+CO2(g) ΔH=-34.0kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒容,在相同时间内测得NO的转化率随温度的变化如图所示:
N2(g)+CO2(g) ΔH=-34.0kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒容,在相同时间内测得NO的转化率随温度的变化如图所示:
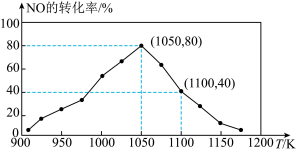
①由图可知,1050K前反应中NO的转化率随温度升高而增大,其原因为___________ ;在1050K时,CO2的体积分数为___________ 。
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1100K、1.1×106Pa时,该反应的化学平衡常数Kp=___________ [已知:气体分压(P分)=气体总压(Pa)×体积分数]。
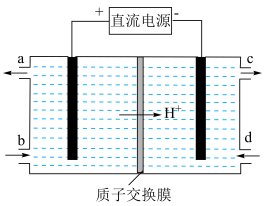
(4)含铈溶液可以处理大气中的氮氧化物,并可通过电解法再生。铈元素(Ce)常见的化合价有+3价、+4价。NO可以被含Ce4+的溶液吸收,生成等物质的量的 、
、 。可采用电解法将上述吸收液中等物质的量
。可采用电解法将上述吸收液中等物质的量 、
、 转化为无毒物质,其原理如图所示。阴极的电极反应式为
转化为无毒物质,其原理如图所示。阴极的电极反应式为___________ 。
(1)已知:
反应Ⅰ:N2(g)+O2(g)
 2NO(g) ΔH1=akJ/mol
2NO(g) ΔH1=akJ/mol反应Ⅱ;2NO(g)+O2(g)
 2NO2(g) ΔH2=bkJ/mol
2NO2(g) ΔH2=bkJ/mol反应Ⅲ:2N2O(g)
 2N2(g)+O2(g) ΔH3=ckJ/mol
2N2(g)+O2(g) ΔH3=ckJ/mol反应Ⅳ:N2O(g)+NO2(g)
 3NO(g) ΔH=
3NO(g) ΔH=(2)汽车尾气中的NO和CO可在催化剂作用下生成无污染的气体。在密闭容器中充入反应物,测得平衡时NO的体积分数与温度、压强的关系如图。

①反应2NO(g)+2CO(g)
 N2(g)+2CO2(g) ΔH<0,则T1
N2(g)+2CO2(g) ΔH<0,则T1②该反应达到平衡后,为同时提高反应速率和NO的转化率,可采取的措施有
③在D点,对反应容器降温的同时缩小体积至体系压强增大,重新达到的平衡状态可能是图中A~G点中的
(3)在催化剂作用下,利用反应C(s)+2NO(g)
 N2(g)+CO2(g) ΔH=-34.0kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒容,在相同时间内测得NO的转化率随温度的变化如图所示:
N2(g)+CO2(g) ΔH=-34.0kJ/mol,用活性炭对NO进行吸附。已知在密闭容器中加入足量的C和一定量的NO气体,保持恒容,在相同时间内测得NO的转化率随温度的变化如图所示:
①由图可知,1050K前反应中NO的转化率随温度升高而增大,其原因为
②用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数(记作Kp)。在1100K、1.1×106Pa时,该反应的化学平衡常数Kp=
(4)含铈溶液可以处理大气中的氮氧化物,并可通过电解法再生。铈元素(Ce)常见的化合价有+3价、+4价。NO可以被含Ce4+的溶液吸收,生成等物质的量的
 、
、 。可采用电解法将上述吸收液中等物质的量
。可采用电解法将上述吸收液中等物质的量 、
、 转化为无毒物质,其原理如图所示。阴极的电极反应式为
转化为无毒物质,其原理如图所示。阴极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】最近,著名记者柴静的雾霾调查纪录片 穹顶之下
穹顶之下 ,在互联网上产生了爆炸性影响.煤燃烧的尾气是造成雾霾天气的原因之一,下列是一种变废为宝的处理方法.
,在互联网上产生了爆炸性影响.煤燃烧的尾气是造成雾霾天气的原因之一,下列是一种变废为宝的处理方法.

(1)上述流程中循环使用的物质有______ ,吸收池Ⅰ吸收的气体有 ______ .
(2)向吸收池Ⅳ得到的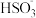 溶液中滴加
溶液中滴加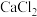 溶液,出现浑浊,pH降低,用平衡移动原理解释溶液pH降低的原因:
溶液,出现浑浊,pH降低,用平衡移动原理解释溶液pH降低的原因: ______ .
(3)电解池Ⅴ制得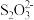 的原理如图1所示.
的原理如图1所示.
写出电解总反应的离子方程式______ .

(4) 和
和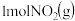 反应生成
反应生成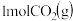 和
和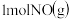 ,反应过程中的能量变化如图2,
,反应过程中的能量变化如图2,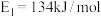 ,
,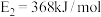 .
.
已知:①
②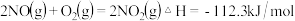
请写出NO与CO反应生成无污染气体的热化学方程式:______ .
(5)上述流程中每一步均恰好完全反应,若制得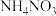 质量为xkg,电解池V制得
质量为xkg,电解池V制得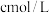 的
的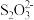 溶液
溶液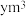 ,则氧化池Ⅵ中消耗的
,则氧化池Ⅵ中消耗的 在标准状况下的体积为
在标准状况下的体积为 ______ 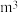 .
.
 穹顶之下
穹顶之下 ,在互联网上产生了爆炸性影响.煤燃烧的尾气是造成雾霾天气的原因之一,下列是一种变废为宝的处理方法.
,在互联网上产生了爆炸性影响.煤燃烧的尾气是造成雾霾天气的原因之一,下列是一种变废为宝的处理方法. 
(1)上述流程中循环使用的物质有
(2)向吸收池Ⅳ得到的
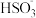 溶液中滴加
溶液中滴加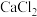 溶液,出现浑浊,pH降低,用平衡移动原理解释溶液pH降低的原因:
溶液,出现浑浊,pH降低,用平衡移动原理解释溶液pH降低的原因: (3)电解池Ⅴ制得
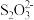 的原理如图1所示.
的原理如图1所示. 写出电解总反应的离子方程式

(4)
 和
和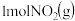 反应生成
反应生成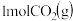 和
和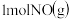 ,反应过程中的能量变化如图2,
,反应过程中的能量变化如图2,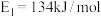 ,
,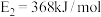 .
.已知:①

②
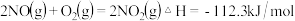
请写出NO与CO反应生成无污染气体的热化学方程式:
(5)上述流程中每一步均恰好完全反应,若制得
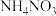 质量为xkg,电解池V制得
质量为xkg,电解池V制得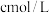 的
的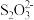 溶液
溶液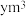 ,则氧化池Ⅵ中消耗的
,则氧化池Ⅵ中消耗的 在标准状况下的体积为
在标准状况下的体积为 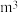 .
.
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】 主要用于电镀工业、生产镍镉电池,用作油脂加氢催化剂、媒染剂等。某兴趣小组用含镍废催化剂(主要含有
主要用于电镀工业、生产镍镉电池,用作油脂加氢催化剂、媒染剂等。某兴趣小组用含镍废催化剂(主要含有 ,还含有
,还含有 、
、 、
、 及其他不溶于酸、碱的杂质)制备
及其他不溶于酸、碱的杂质)制备 ,其流程如下:
,其流程如下:
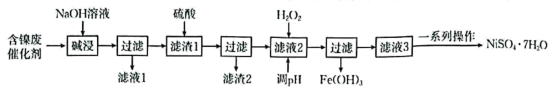
已知:①常温下,部分金属化合物的 近似值如表所示:
近似值如表所示:
②金属活泼性: 。
。
③ 。
。
回答下列问题:
(1) 元素在元素周期表中的位置为
元素在元素周期表中的位置为_______ ,其基态原子的价层电子排布式为_______ 。
(2)“滤液1”中的主要溶质为 、
、_______ 。
(3)加入硫酸时, 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(4)加入 的目的是将
的目的是将 氧化为
氧化为 ,该步骤
,该步骤_______ (填“能”或“不能”)用适量稀硝酸代替,理由是_______ 。然后调节溶液的 ,则此时应调节溶液的
,则此时应调节溶液的 至少为
至少为_______ (保留3位有效数字,离子浓度小于或等于 时认为沉淀完全),检验“滤液3”中杂质金属离子已除尽的操作和现象是
时认为沉淀完全),检验“滤液3”中杂质金属离子已除尽的操作和现象是_______ 。
(5)用配位滴定法测定粗品中 的纯度。取
的纯度。取 粗品溶于水(滴加几滴稀硫酸)配成
粗品溶于水(滴加几滴稀硫酸)配成 溶液,取
溶液,取 溶液于锥形瓶中,滴入几滴紫脲酸胺指示剂(紫色试剂,遇
溶液于锥形瓶中,滴入几滴紫脲酸胺指示剂(紫色试剂,遇 显橙黄色),用浓度为
显橙黄色),用浓度为 的
的 标准液滴定,平均消耗标准液
标准液滴定,平均消耗标准液 。已知:
。已知: 。粗品中
。粗品中 的纯度是
的纯度是_______ %;下列操作会使测定结果偏低的是_______ (填标号)。
A.锥形瓶中溶液颜色由橙黄色局部变为紫色后立即停止滴定
B.滴定前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡
C.滴定前平视读数,滴定后仰视读数
 主要用于电镀工业、生产镍镉电池,用作油脂加氢催化剂、媒染剂等。某兴趣小组用含镍废催化剂(主要含有
主要用于电镀工业、生产镍镉电池,用作油脂加氢催化剂、媒染剂等。某兴趣小组用含镍废催化剂(主要含有 ,还含有
,还含有 、
、 、
、 及其他不溶于酸、碱的杂质)制备
及其他不溶于酸、碱的杂质)制备 ,其流程如下:
,其流程如下:
已知:①常温下,部分金属化合物的
 近似值如表所示:
近似值如表所示:| 化学式 |  |  | 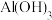 |  |  |
 近似值 近似值 | 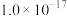 | 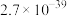 | 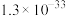 | 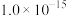 |  |
 。
。③
 。
。回答下列问题:
(1)
 元素在元素周期表中的位置为
元素在元素周期表中的位置为(2)“滤液1”中的主要溶质为
 、
、(3)加入硫酸时,
 发生反应的离子方程式为
发生反应的离子方程式为(4)加入
 的目的是将
的目的是将 氧化为
氧化为 ,该步骤
,该步骤 ,则此时应调节溶液的
,则此时应调节溶液的 至少为
至少为 时认为沉淀完全),检验“滤液3”中杂质金属离子已除尽的操作和现象是
时认为沉淀完全),检验“滤液3”中杂质金属离子已除尽的操作和现象是(5)用配位滴定法测定粗品中
 的纯度。取
的纯度。取 粗品溶于水(滴加几滴稀硫酸)配成
粗品溶于水(滴加几滴稀硫酸)配成 溶液,取
溶液,取 溶液于锥形瓶中,滴入几滴紫脲酸胺指示剂(紫色试剂,遇
溶液于锥形瓶中,滴入几滴紫脲酸胺指示剂(紫色试剂,遇 显橙黄色),用浓度为
显橙黄色),用浓度为 的
的 标准液滴定,平均消耗标准液
标准液滴定,平均消耗标准液 。已知:
。已知: 。粗品中
。粗品中 的纯度是
的纯度是A.锥形瓶中溶液颜色由橙黄色局部变为紫色后立即停止滴定
B.滴定前滴定管尖嘴内有气泡,滴定后尖嘴内无气泡
C.滴定前平视读数,滴定后仰视读数
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】硼氢化钠 是一种潜在储氢剂,在有机合成中也被称为“万能还原剂”。实验室制备、提纯、分析
是一种潜在储氢剂,在有机合成中也被称为“万能还原剂”。实验室制备、提纯、分析 纯度的步骤如下。
纯度的步骤如下。
Ⅰ. 的制备
的制备
利用如图甲装置(加热及夹持装置略)进行操作: ,鼓入
,鼓入 ,升温到110℃,快速搅拌,将融化的Na快速分散到石蜡油中;
,升温到110℃,快速搅拌,将融化的Na快速分散到石蜡油中;
(ⅱ)升温到200℃,关闭 ,打开
,打开 通入
通入 ,充分反应后制得
,充分反应后制得 ;
;
(ⅲ)升温到240℃,持续搅拌下通入 ,打开
,打开 滴入硼酸三甲酯[分子式为
滴入硼酸三甲酯[分子式为 ];
];
(ⅳ)降温后,分离得到 和
和 的固体混合物。
的固体混合物。
已知:
 :可溶于异丙胺或水,常温下与水缓慢反应,强碱环境下能稳定存在
:可溶于异丙胺或水,常温下与水缓慢反应,强碱环境下能稳定存在
 :难溶于异丙胺
:难溶于异丙胺
异丙胺:有机溶剂,沸点:33℃
Ⅱ. 的提纯
的提纯
 可采用索氏提取法提纯,其装置如图乙所示,实验时将
可采用索氏提取法提纯,其装置如图乙所示,实验时将 和
和 的固体混合物放入滤纸套筒1中,烧瓶中加入异丙胺。烧瓶中异丙胺受热蒸发上升,冷凝后滴入滤纸套筒1中,再经导管返回烧瓶,从而实现连续萃取。
的固体混合物放入滤纸套筒1中,烧瓶中加入异丙胺。烧瓶中异丙胺受热蒸发上升,冷凝后滴入滤纸套筒1中,再经导管返回烧瓶,从而实现连续萃取。
步骤1:取m g产品(杂质不参加反应)溶于 溶液后配成
溶液后配成 溶液,取
溶液,取 置于碘量瓶中,加入
置于碘量瓶中,加入 的
的 溶液充分反应。(
溶液充分反应。( )
)
步骤2:向步骤1反应后溶液中加入过量的KI溶液,用稀硫酸调节pH,使过量 转化为
转化为 ,冷却后于暗处放数分钟。
,冷却后于暗处放数分钟。
步骤3:将步骤2所得混合液调pH约为5.0,加入几滴淀粉,用 标准溶液滴定至终点,消耗溶液
标准溶液滴定至终点,消耗溶液 。(
。( )
)
回答下列问题:
(1)仪器a的名称是__________ 。
(2)写出 与
与 反应的化学方程式
反应的化学方程式__________ 。
(3)下列有关说法不正确的是__________。
(4)按照先后顺序对本实验的滴定操作排序
检查是否漏水→蒸馏水洗涤→__________ →__________→a→__________→__________→__________。
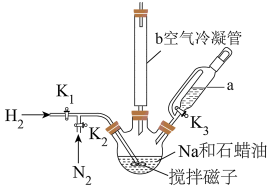
a.加液至“0”刻度以上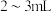 处
处
b.调整液面至“0”刻度或“0”刻度下方,记录读数
c.倾斜转动滴定管,使标准液润湿滴定管内壁,将润洗液从下口排出
d.赶出尖嘴部分气泡
e.向碱式滴定管中加 标准液
标准液
f.向酸式滴定管中加 标准液
标准液
g.左手控制活塞(或挤压玻璃珠),右手振荡锥形瓶
h.左手振荡锥形瓶,右手控制活塞(或挤压玻璃珠)
(5)产品中 的纯度为
的纯度为__________ %。
 是一种潜在储氢剂,在有机合成中也被称为“万能还原剂”。实验室制备、提纯、分析
是一种潜在储氢剂,在有机合成中也被称为“万能还原剂”。实验室制备、提纯、分析 纯度的步骤如下。
纯度的步骤如下。Ⅰ.
 的制备
的制备利用如图甲装置(加热及夹持装置略)进行操作:
 ,鼓入
,鼓入 ,升温到110℃,快速搅拌,将融化的Na快速分散到石蜡油中;
,升温到110℃,快速搅拌,将融化的Na快速分散到石蜡油中;(ⅱ)升温到200℃,关闭
 ,打开
,打开 通入
通入 ,充分反应后制得
,充分反应后制得 ;
;(ⅲ)升温到240℃,持续搅拌下通入
 ,打开
,打开 滴入硼酸三甲酯[分子式为
滴入硼酸三甲酯[分子式为 ];
];(ⅳ)降温后,分离得到
 和
和 的固体混合物。
的固体混合物。已知:
 :可溶于异丙胺或水,常温下与水缓慢反应,强碱环境下能稳定存在
:可溶于异丙胺或水,常温下与水缓慢反应,强碱环境下能稳定存在 :难溶于异丙胺
:难溶于异丙胺异丙胺:有机溶剂,沸点:33℃
Ⅱ.
 的提纯
的提纯 可采用索氏提取法提纯,其装置如图乙所示,实验时将
可采用索氏提取法提纯,其装置如图乙所示,实验时将 和
和 的固体混合物放入滤纸套筒1中,烧瓶中加入异丙胺。烧瓶中异丙胺受热蒸发上升,冷凝后滴入滤纸套筒1中,再经导管返回烧瓶,从而实现连续萃取。
的固体混合物放入滤纸套筒1中,烧瓶中加入异丙胺。烧瓶中异丙胺受热蒸发上升,冷凝后滴入滤纸套筒1中,再经导管返回烧瓶,从而实现连续萃取。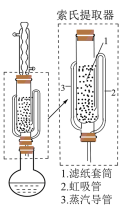
步骤1:取m g产品(杂质不参加反应)溶于
 溶液后配成
溶液后配成 溶液,取
溶液,取 置于碘量瓶中,加入
置于碘量瓶中,加入 的
的 溶液充分反应。(
溶液充分反应。( )
)步骤2:向步骤1反应后溶液中加入过量的KI溶液,用稀硫酸调节pH,使过量
 转化为
转化为 ,冷却后于暗处放数分钟。
,冷却后于暗处放数分钟。步骤3:将步骤2所得混合液调pH约为5.0,加入几滴淀粉,用
 标准溶液滴定至终点,消耗溶液
标准溶液滴定至终点,消耗溶液 。(
。( )
)回答下列问题:
(1)仪器a的名称是
(2)写出
 与
与 反应的化学方程式
反应的化学方程式(3)下列有关说法不正确的是__________。
A. 和 和 中氢化合价相同 中氢化合价相同 | B.装置甲应该处于无水、无氧的反应环境 |
| C.装置乙中异丙胺蒸汽沿导管2上升 | D.萃取完全后, 在圆底烧瓶中 在圆底烧瓶中 |
(4)按照先后顺序对本实验的滴定操作排序
检查是否漏水→蒸馏水洗涤→
a.加液至“0”刻度以上
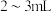 处
处b.调整液面至“0”刻度或“0”刻度下方,记录读数

c.倾斜转动滴定管,使标准液润湿滴定管内壁,将润洗液从下口排出
d.赶出尖嘴部分气泡
e.向碱式滴定管中加
 标准液
标准液f.向酸式滴定管中加
 标准液
标准液g.左手控制活塞(或挤压玻璃珠),右手振荡锥形瓶
h.左手振荡锥形瓶,右手控制活塞(或挤压玻璃珠)
(5)产品中
 的纯度为
的纯度为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】二草酸合铜(Ⅱ)酸钾晶体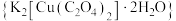 ,是一种工业用化工原料。微溶于冷水,可溶于热水,微溶于酒精,干燥时较为稳定,加热时易分解。现以胆矾和草酸为原料制备二草酸合铜(Ⅱ)酸钾晶体流程如图:
,是一种工业用化工原料。微溶于冷水,可溶于热水,微溶于酒精,干燥时较为稳定,加热时易分解。现以胆矾和草酸为原料制备二草酸合铜(Ⅱ)酸钾晶体流程如图:
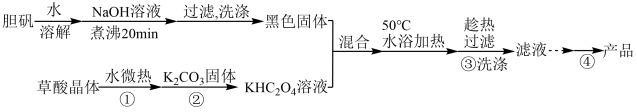
(已知: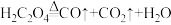 ),请回答:
),请回答:
(1)第①步操作要微热溶解,其原因是避免 分解和
分解和___________ 。
(2)下列关于实验原理和流程的说法正确的是___________ 。
a.黑色固体是否洗涤干净可取少量最后一次洗涤液,用 溶液进行检验
溶液进行检验
b.水浴加热的优点是受热均匀且易于控制温度
c.流程中“混合”操作为:用水溶解滤纸上的黑色固体,再将溶液转入热的 溶液中
溶液中
(3) 水浴加热至反应充分,写出该反应的化学方程式:
水浴加热至反应充分,写出该反应的化学方程式:___________ 。
(4)步骤③所用的洗涤剂最合适的是___________ (填“冷水”、“热水”或“酒精”)。
(5)二草酸合铜(II)酸钾晶体的制备也可以用 晶体和
晶体和 溶液反应得到。从硫酸铜溶液中获得硫酸铜晶体的实验步骤为:加入适量乙醇、蒸发浓缩、冷却结晶、过滤、洗涤、干燥。
溶液反应得到。从硫酸铜溶液中获得硫酸铜晶体的实验步骤为:加入适量乙醇、蒸发浓缩、冷却结晶、过滤、洗涤、干燥。
①加入适量乙醇的优点有:
a.缩短加热的时间,降低能耗;
b.___________ 。
②在蒸发浓缩的初始阶段可通过___________ (填操作名称)回收乙醇。
(6)准确称取制取的晶体试样 溶于
溶于 中,并加水定容至250mL,定容时所用到的仪器有:
中,并加水定容至250mL,定容时所用到的仪器有:___________ 。
(7)在常温下,胆矾溶液与氢氧化钠溶液反应生成氢氧化铜沉淀,当所得溶液的 时,溶液中
时,溶液中
___________ {已知该温度下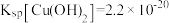 }。
}。
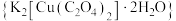 ,是一种工业用化工原料。微溶于冷水,可溶于热水,微溶于酒精,干燥时较为稳定,加热时易分解。现以胆矾和草酸为原料制备二草酸合铜(Ⅱ)酸钾晶体流程如图:
,是一种工业用化工原料。微溶于冷水,可溶于热水,微溶于酒精,干燥时较为稳定,加热时易分解。现以胆矾和草酸为原料制备二草酸合铜(Ⅱ)酸钾晶体流程如图:
(已知:
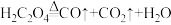 ),请回答:
),请回答:(1)第①步操作要微热溶解,其原因是避免
 分解和
分解和(2)下列关于实验原理和流程的说法正确的是
a.黑色固体是否洗涤干净可取少量最后一次洗涤液,用
 溶液进行检验
溶液进行检验b.水浴加热的优点是受热均匀且易于控制温度
c.流程中“混合”操作为:用水溶解滤纸上的黑色固体,再将溶液转入热的
 溶液中
溶液中(3)
 水浴加热至反应充分,写出该反应的化学方程式:
水浴加热至反应充分,写出该反应的化学方程式:(4)步骤③所用的洗涤剂最合适的是
(5)二草酸合铜(II)酸钾晶体的制备也可以用
 晶体和
晶体和 溶液反应得到。从硫酸铜溶液中获得硫酸铜晶体的实验步骤为:加入适量乙醇、蒸发浓缩、冷却结晶、过滤、洗涤、干燥。
溶液反应得到。从硫酸铜溶液中获得硫酸铜晶体的实验步骤为:加入适量乙醇、蒸发浓缩、冷却结晶、过滤、洗涤、干燥。①加入适量乙醇的优点有:
a.缩短加热的时间,降低能耗;
b.
②在蒸发浓缩的初始阶段可通过
(6)准确称取制取的晶体试样
 溶于
溶于 中,并加水定容至250mL,定容时所用到的仪器有:
中,并加水定容至250mL,定容时所用到的仪器有:(7)在常温下,胆矾溶液与氢氧化钠溶液反应生成氢氧化铜沉淀,当所得溶液的
 时,溶液中
时,溶液中
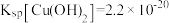 }。
}。
您最近一年使用:0次



