利用压强传感器测定氨气的喷泉实验中的压强变化。___________ 。
(2)可以用___________ 试纸置于三颈瓶口c处验满。
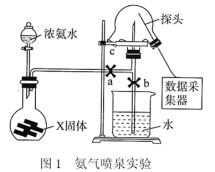
(3)关闭a,将单孔塞(插有吸入水的胶头滴管)塞紧瓶口c,挤压胶头滴管,打开b,完成喷泉实验,电脑绘制三颈瓶内压强变化曲线如图2,___________ 点时喷泉最剧烈(选填A、B、C、D、E)。 且混合均匀,实验开始前烧瓶中气体的平均分子量为
且混合均匀,实验开始前烧瓶中气体的平均分子量为___________ ,实验结束后烧瓶中溶液的物质的量浓度为___________ mol/L。
(2)可以用
(3)关闭a,将单孔塞(插有吸入水的胶头滴管)塞紧瓶口c,挤压胶头滴管,打开b,完成喷泉实验,电脑绘制三颈瓶内压强变化曲线如图2,
 且混合均匀,实验开始前烧瓶中气体的平均分子量为
且混合均匀,实验开始前烧瓶中气体的平均分子量为
更新时间:2024-04-30 08:08:09
|
相似题推荐
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】如图是硫酸试剂标签上的内容。
(1)该硫酸的物质的量浓度为___________ 。
(2)实验室用该硫酸配制240mL0.46mol·L-1的稀硫酸,则
①需要用量筒量取该浓硫酸的体积为___________ mL。
②为完成实验,现有仪器:烧杯、10mL量筒、玻璃棒,还必需的玻璃仪器有___________ 。
(3)下列操作中,容量瓶所具备的功能有___________。
(4)在下列配制过程示意图中,有错误的是(填写序号)___________ 。

(5)在定容操作时,因不慎加水至凹液面最低处超过了刻度线,该如何处理:___________ 。
(6)下列说法正确的是___________ 。
A.洗涤烧杯和玻璃棒2-3次,并将洗涤液移入容量瓶以减少误差
B.将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察,所配溶液浓度会偏低
D.容量瓶使用前先要检查是否漏液,具体操作是向容量瓶中加蒸馏水,倒置不漏液即可
E.容量瓶在使用前未干燥,里面有少量蒸馏水,所配溶液浓度会偏低
(7)配制的稀硫酸转移至试剂瓶中后,填写标签上的内容___________ 。

| 硫酸化学纯(CP) (500ml) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84g/cm3 质量分数:98% |
(1)该硫酸的物质的量浓度为
(2)实验室用该硫酸配制240mL0.46mol·L-1的稀硫酸,则
①需要用量筒量取该浓硫酸的体积为
②为完成实验,现有仪器:烧杯、10mL量筒、玻璃棒,还必需的玻璃仪器有
(3)下列操作中,容量瓶所具备的功能有___________。
| A.配制一定体积准确浓度的标准溶液 |
| B.长期贮存溶液 |
| C.用来溶解固体溶质 |
| D.常用来代替量筒量取一定体积的液体 |
(4)在下列配制过程示意图中,有错误的是(填写序号)

(5)在定容操作时,因不慎加水至凹液面最低处超过了刻度线,该如何处理:
(6)下列说法正确的是
A.洗涤烧杯和玻璃棒2-3次,并将洗涤液移入容量瓶以减少误差
B.将浓硫酸稀释后未冷却至室温便将溶液转移至容量瓶,所配溶液浓度会偏低
C.定容时仰视观察,所配溶液浓度会偏低
D.容量瓶使用前先要检查是否漏液,具体操作是向容量瓶中加蒸馏水,倒置不漏液即可
E.容量瓶在使用前未干燥,里面有少量蒸馏水,所配溶液浓度会偏低
(7)配制的稀硫酸转移至试剂瓶中后,填写标签上的内容

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某实验需要 溶液,配制步骤包括:
溶液,配制步骤包括:
①将容量瓶塞紧,充分摇匀;
②待烧杯中的溶液冷却到室温后,转入__________;
③把称量好的 固体放入烧杯中,加适量蒸馏水溶解;
固体放入烧杯中,加适量蒸馏水溶解;
④用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都转入容量瓶,并轻轻摇匀。
⑤继续加蒸馏水至液面距刻度线1~2cm处,改用__________滴加蒸馏水至溶液凹液面与刻度线相切;
回答下列问题:
(1)用托盘天平称量所需 晶体的质量为
晶体的质量为__________ g。
(2)实验步骤中使用的仪器分别为②__________ 、⑤__________ 。
(3)正确的实验操作顺序为__________ (填序号)。
(4)下列操作会导致所配溶液浓度偏低的是__________ (填字母)。
a.定容时俯视刻度线
b.将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
c.摇匀后发现液面低于容量瓶刻度线,再滴加蒸馏水至刻度线
d.用托盘天平称量晶体时,药品和砝码位置放反了
(5)若所配溶液的密度为 ,则溶液中溶质的质量分数为
,则溶液中溶质的质量分数为__________ 。
 溶液,配制步骤包括:
溶液,配制步骤包括:①将容量瓶塞紧,充分摇匀;
②待烧杯中的溶液冷却到室温后,转入__________;
③把称量好的
 固体放入烧杯中,加适量蒸馏水溶解;
固体放入烧杯中,加适量蒸馏水溶解;④用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都转入容量瓶,并轻轻摇匀。
⑤继续加蒸馏水至液面距刻度线1~2cm处,改用__________滴加蒸馏水至溶液凹液面与刻度线相切;
回答下列问题:
(1)用托盘天平称量所需
 晶体的质量为
晶体的质量为(2)实验步骤中使用的仪器分别为②
(3)正确的实验操作顺序为
(4)下列操作会导致所配溶液浓度偏低的是
a.定容时俯视刻度线
b.将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
c.摇匀后发现液面低于容量瓶刻度线,再滴加蒸馏水至刻度线
d.用托盘天平称量晶体时,药品和砝码位置放反了
(5)若所配溶液的密度为
 ,则溶液中溶质的质量分数为
,则溶液中溶质的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
(1)该“84消毒液”的物质的量浓度约为_______ mol/L。(保留一位小数)
(2)某实验中要用2 mol/L的“84消毒液”500 mL,则需取用上述“84消毒液”_______ m L进行稀释。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL该浓度的消毒液。回答下列问题。
①配制上述溶液需要如图所示的仪器中_______ mL的容量瓶,所需NaClO的质量为_______ g。
②若所配制的次氯酸钠溶液浓度偏小,则下列可能的原因分析中正确的是_______ 。
A.配制前,容量瓶中有少量蒸馏水
B.洗涤液未转移到容量瓶中
C.未冷却,立即转移至容量瓶定容
D.定容时,仰视溶液的凹液面
| 84消毒液 (有效成分)NaClO (规格)1000 mL (质量分数)25% (密度)1.19g/cm3 |
(2)某实验中要用2 mol/L的“84消毒液”500 mL,则需取用上述“84消毒液”
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL该浓度的消毒液。回答下列问题。
①配制上述溶液需要如图所示的仪器中
②若所配制的次氯酸钠溶液浓度偏小,则下列可能的原因分析中正确的是
A.配制前,容量瓶中有少量蒸馏水
B.洗涤液未转移到容量瓶中
C.未冷却,立即转移至容量瓶定容
D.定容时,仰视溶液的凹液面
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】为探究NH3的溶解性,某兴趣小组按如图所示装置进行实验(f为止水夹),请回答下列问题:

(1)写出实验室制取氨气的化学方程式______________ 。
(2)要得到干燥的氨气可选用______________ 作干燥剂。
A.碱石灰(CaO和NaOH的混合物) B.浓硫酸
C.浓硝酸 D.氢氧化钠溶液
(3)用如图装置进行喷泉实验,仪器a是___________ (仪器名称)。
(4)若烧杯c的水中滴有酚酞,实验结束后,a中溶液呈_______ (填“红”或“蓝”)色。

(1)写出实验室制取氨气的化学方程式
(2)要得到干燥的氨气可选用
A.碱石灰(CaO和NaOH的混合物) B.浓硫酸
C.浓硝酸 D.氢氧化钠溶液
(3)用如图装置进行喷泉实验,仪器a是
(4)若烧杯c的水中滴有酚酞,实验结束后,a中溶液呈
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】在化学实验操作技能考查中有三道考题:
a.氧气的实验室制取与性质;
b.二氧化碳的制取、收集和验满;
c.粗盐中难溶性杂质的去除。
小宇抽签后由监考老师引领至实验桌前,该实验桌上摆放了如图1所示药品和仪器。回答下列问题:

(1)图1中所示仪器⑤的名称是:⑤_______ 。
(2)小宇进行的考题是_______ (填序号),其主要操作如图2所示:

其中操作错误的是_______ (填序号);
(3)若用加热氯酸钾的方法制取氧气,写出该化学反应方程式_______
(4)化学活动周中,各竞赛小组设计出了各种有趣的喷泉。
①竞赛I组和竞赛II组查阅资料得知:NH3极易溶于水,1体积水中约可以溶解700体积的NH3,分别设计了图3和图4实验装置。

竞赛I组操作如下:在干燥的烧瓶内收集满纯净干燥的氨气,塞紧带有玻璃管和胶头滴管(预先吸满水)的胶塞,打开止水夹,形成了喷泉。竞赛II组在干燥的烧瓶内收集满纯净干燥的氨气后,其引发喷泉的方法是:打开止水夹,用热毛巾梧住圆底烧瓶。
②竞赛III组也在干燥的烧瓶内收集满纯净干燥的氨气后,设计了如图实验(见图5),引发了喷泉,玻璃套管中的固体是_______ (填序号)。
A.氢氧化钙 B.氯化钠 C.活性炭 D.氧化铜
(5)图6是实验室常见的干燥装置,可用于干燥二氧化碳气体的是_______ (填“甲”或“乙”),不能选另一套的原因是_______ 。
a.氧气的实验室制取与性质;
b.二氧化碳的制取、收集和验满;
c.粗盐中难溶性杂质的去除。
小宇抽签后由监考老师引领至实验桌前,该实验桌上摆放了如图1所示药品和仪器。回答下列问题:

(1)图1中所示仪器⑤的名称是:⑤
(2)小宇进行的考题是

其中操作错误的是
(3)若用加热氯酸钾的方法制取氧气,写出该化学反应方程式
(4)化学活动周中,各竞赛小组设计出了各种有趣的喷泉。
①竞赛I组和竞赛II组查阅资料得知:NH3极易溶于水,1体积水中约可以溶解700体积的NH3,分别设计了图3和图4实验装置。

竞赛I组操作如下:在干燥的烧瓶内收集满纯净干燥的氨气,塞紧带有玻璃管和胶头滴管(预先吸满水)的胶塞,打开止水夹,形成了喷泉。竞赛II组在干燥的烧瓶内收集满纯净干燥的氨气后,其引发喷泉的方法是:打开止水夹,用热毛巾梧住圆底烧瓶。
②竞赛III组也在干燥的烧瓶内收集满纯净干燥的氨气后,设计了如图实验(见图5),引发了喷泉,玻璃套管中的固体是
A.氢氧化钙 B.氯化钠 C.活性炭 D.氧化铜
(5)图6是实验室常见的干燥装置,可用于干燥二氧化碳气体的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】Ⅰ.某同学利用如图所示的装置,验证氨气的喷泉实验。

回答下列问题:
(1)仪器A的名称是_______ 。
(2)写出实验室用NH4Cl和Ca(OH)2制氨气的化学方程式:_______ 。
(3)喷泉实验前需要在仪器A中充满干燥的氨气。
①可用向_______ 填“上”或“下”)排空气法收集氨气。
②下列物质可用于干燥氨气的是_______ 填序号)。
A.浓硫酸 B.碱石灰 C.浓硝酸
(4)引发喷泉实验的操作是_______ 。
Ⅱ.糖类是重要的营养物质,淀粉属于糖类,水解可得葡萄糖。填写下列空白:
(1)葡萄糖与果糖互为_______ 。
(2)假设淀粉部分水解,进行下列验证实验
①为验证仍有淀粉,向水解后的溶液中加入_______ ,溶液变蓝。
②为验证水解产物,向水解后的溶液中加入过量的NaOH溶液和新制Cu(OH)2,加热,现象是_______ 。

回答下列问题:
(1)仪器A的名称是
(2)写出实验室用NH4Cl和Ca(OH)2制氨气的化学方程式:
(3)喷泉实验前需要在仪器A中充满干燥的氨气。
①可用向
②下列物质可用于干燥氨气的是
A.浓硫酸 B.碱石灰 C.浓硝酸
(4)引发喷泉实验的操作是
Ⅱ.糖类是重要的营养物质,淀粉属于糖类,水解可得葡萄糖。填写下列空白:
(1)葡萄糖与果糖互为
(2)假设淀粉部分水解,进行下列验证实验
①为验证仍有淀粉,向水解后的溶液中加入
②为验证水解产物,向水解后的溶液中加入过量的NaOH溶液和新制Cu(OH)2,加热,现象是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某化学兴趣小组为了制取氨气并探究其性质,按下列装置(部分夹持装置已略去)进行实验。

(1)若氨气的发生装置选择a,则其化学反应方程式为____ 。
(2)若氨气的发生装置选择b,则所用的试剂为____ 。
(3)B装置中的干燥剂可选用____ 。
(4)实验中观察到C装置中的现象是____ 。
(5)当实验进行一段时间后,挤压D装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是____ ,发生的化学反应方程式为_____ 。
(6)E中倒扣漏斗的作用是____ 。

(1)若氨气的发生装置选择a,则其化学反应方程式为
(2)若氨气的发生装置选择b,则所用的试剂为
(3)B装置中的干燥剂可选用
(4)实验中观察到C装置中的现象是
(5)当实验进行一段时间后,挤压D装置中的胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
(6)E中倒扣漏斗的作用是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】构建元素化合物之间的转化关系模型是学习元素化合物知识的一种方法。已知A、B、C、D、E是中学化学中常见的五种物质,常温下E是一种无色液体,它们之间有如下反应关系。回答下列问题:

(1)若B是黄绿色气体,上述转化关系常用于实验室B气体的尾气吸收,则该反应的离子方程式为_______________ 。
(2)若A是一种紫红色金属单质,B是一种挥发性酸,反应时生成的C是无色气体,反应的离子方程式是_____________ ,若反应中生成标准状况下1.12 LC气体,则被还原的B物质的量为________ mol。
(3)若实验室中利用A和B的反应制备气体C,C是一种无色刺激性气味、密度比空气小的气体,此反应的化学方程式为___________ ,实验室检验C的方法为 _____________ 。
(4)若常温下A能使铁钝化,B是黑色固体非金属单质, D是一种能使品红溶液褪色的无色气体, A和B反应的化学方程式为___________ ,检验A的钠盐溶液中阴离子的方法是 ____________ 。

(1)若B是黄绿色气体,上述转化关系常用于实验室B气体的尾气吸收,则该反应的离子方程式为
(2)若A是一种紫红色金属单质,B是一种挥发性酸,反应时生成的C是无色气体,反应的离子方程式是
(3)若实验室中利用A和B的反应制备气体C,C是一种无色刺激性气味、密度比空气小的气体,此反应的化学方程式为
(4)若常温下A能使铁钝化,B是黑色固体非金属单质, D是一种能使品红溶液褪色的无色气体, A和B反应的化学方程式为
您最近一年使用:0次




