构建元素化合物之间的转化关系模型是学习元素化合物知识的一种方法。已知A、B、C、D、E是中学化学中常见的五种物质,常温下E是一种无色液体,它们之间有如下反应关系。回答下列问题:

(1)若B是黄绿色气体,上述转化关系常用于实验室B气体的尾气吸收,则该反应的离子方程式为_______________ 。
(2)若A是一种紫红色金属单质,B是一种挥发性酸,反应时生成的C是无色气体,反应的离子方程式是_____________ ,若反应中生成标准状况下1.12 LC气体,则被还原的B物质的量为________ mol。
(3)若实验室中利用A和B的反应制备气体C,C是一种无色刺激性气味、密度比空气小的气体,此反应的化学方程式为___________ ,实验室检验C的方法为 _____________ 。
(4)若常温下A能使铁钝化,B是黑色固体非金属单质, D是一种能使品红溶液褪色的无色气体, A和B反应的化学方程式为___________ ,检验A的钠盐溶液中阴离子的方法是 ____________ 。

(1)若B是黄绿色气体,上述转化关系常用于实验室B气体的尾气吸收,则该反应的离子方程式为
(2)若A是一种紫红色金属单质,B是一种挥发性酸,反应时生成的C是无色气体,反应的离子方程式是
(3)若实验室中利用A和B的反应制备气体C,C是一种无色刺激性气味、密度比空气小的气体,此反应的化学方程式为
(4)若常温下A能使铁钝化,B是黑色固体非金属单质, D是一种能使品红溶液褪色的无色气体, A和B反应的化学方程式为
更新时间:2022-12-11 22:06:00
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】已知B为碱性氧化物,D为淡黄色固体粉末,F为医疗上治疗胃酸过多的一种药剂;物质的转化关系如下图所示,请回答下列问题:
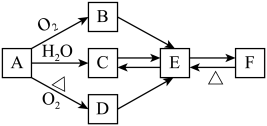
(1)请写出下列物质的化学式: A_______ 、 E_______ 。
(2)请写出下列反应的化学方程式:
A→C:_______ ;
D→E:_______ ;
F→E:_______ 。
(3)将23gA投入47.8g水中,所得溶液质量分数为_______ (用百分数表示)。若把A投入盛有FeCl3的溶液中,溶液中出现_______ (填沉淀颜色)沉淀。

(1)请写出下列物质的化学式: A
(2)请写出下列反应的化学方程式:
A→C:
D→E:
F→E:
(3)将23gA投入47.8g水中,所得溶液质量分数为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】下图转化关系中,A是一种盐,B是气态氯化物,C是单质,F是强酸。且A、B、C、D、E、F中均含有同一种元素。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),则A物质可以是___________ 。


您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】I.如图是氮气经一系列反应制得硝酸的过程。







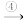

请回答:
(1)下列说法正确的是____ (选填序号字母)。
A.因断开氮气分子内的共价三键需要较多的能量,所以氮气化学性质很稳定
B.反应②、③、④中氮元素均被氧化
C.分别蘸有浓氨水和浓盐酸的玻璃棒靠近时,会产生白烟
(2)反应①的化学方程式为____ 。
II.实验室制取氨气常采用如图所示装置。

(3)试管中盛放的药品是NH4Cl和Ca(OH)2,则试管中的反应方程式为____ 。
(4)球形干燥管内盛放的药品是碱石灰,其作用是____ 。
(5)棉花润湿的目的是____ 。
(6)图中尾部收集氨气时,从所收集气体的纯度上看,若伸入试管中的导管很短,收集效果会____ (“更好”,“更差”,“没有区别”)。








请回答:
(1)下列说法正确的是
A.因断开氮气分子内的共价三键需要较多的能量,所以氮气化学性质很稳定
B.反应②、③、④中氮元素均被氧化
C.分别蘸有浓氨水和浓盐酸的玻璃棒靠近时,会产生白烟
(2)反应①的化学方程式为
II.实验室制取氨气常采用如图所示装置。

(3)试管中盛放的药品是NH4Cl和Ca(OH)2,则试管中的反应方程式为
(4)球形干燥管内盛放的药品是碱石灰,其作用是
(5)棉花润湿的目的是
(6)图中尾部收集氨气时,从所收集气体的纯度上看,若伸入试管中的导管很短,收集效果会
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】回答下列问题:
(1)实验室常见的几种气体发生装置如图A、B、C所示:

①实验室可以用B或C装置制取氨气,如果用C装置,通常使用的药品是_______ ;检查C装置气密性的方法是_______ 。
②若用A装置与D装置相连制取并收集X气体,则X可能是下列气体中的_______ (填序号)。
a. b.NO c.
b.NO c. d.
d.
(2)取化学式为MZ的粉末状化合物进行如下实验。将MZ和足量碳粉充分混合,平铺在反应管a中,在b瓶中盛足量澄清石灰水,按图连接仪器。实验开始时缓缓通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成,同时b瓶的溶液中出现白色浑浊。待反应完全后,停止加热,仍继续通氮气,直至反应管冷却,此时管中的熔融物凝固成银白色金属。根据以上叙述回答:

①元素Z是_______ ;(填名称)
②停止加热是否需要先断开a和b的连接处?为什么?_______ 。
③本实验的尾气是否需处理?_______ (填“需要”或“不需要”),请说明理由_______ 。
(1)实验室常见的几种气体发生装置如图A、B、C所示:

①实验室可以用B或C装置制取氨气,如果用C装置,通常使用的药品是
②若用A装置与D装置相连制取并收集X气体,则X可能是下列气体中的
a.
 b.NO c.
b.NO c. d.
d.
(2)取化学式为MZ的粉末状化合物进行如下实验。将MZ和足量碳粉充分混合,平铺在反应管a中,在b瓶中盛足量澄清石灰水,按图连接仪器。实验开始时缓缓通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成,同时b瓶的溶液中出现白色浑浊。待反应完全后,停止加热,仍继续通氮气,直至反应管冷却,此时管中的熔融物凝固成银白色金属。根据以上叙述回答:

①元素Z是
②停止加热是否需要先断开a和b的连接处?为什么?
③本实验的尾气是否需处理?
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】某小组同学用如图所示装置制取氨气并验证氨气的性质。请回答:

(1)制取氨气的化学方程式是___________ 。
(2)采用题图的方法收集氨气,是因为氨气的密度比空气的___________ (填“大”或“小”)。
(3)把蘸有浓盐酸的玻璃棒靠近集满氨气的试管口,观察到的实验现象是___________ 。
(4)检验试管中氨气是否集满的方法___________ 。
(5)下列可用于干燥氨气的是___________ (填标号,下同)。
A.浓硫酸 B.浓硝酸 C.五氧化二磷 D.碱石灰
(6)生石灰与水反应生成Ca(OH)2并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是___________ 。


(1)制取氨气的化学方程式是
(2)采用题图的方法收集氨气,是因为氨气的密度比空气的
(3)把蘸有浓盐酸的玻璃棒靠近集满氨气的试管口,观察到的实验现象是
(4)检验试管中氨气是否集满的方法
(5)下列可用于干燥氨气的是
A.浓硫酸 B.浓硝酸 C.五氧化二磷 D.碱石灰
(6)生石灰与水反应生成Ca(OH)2并放出热量。实验室利用此原理,向生石灰中滴加浓氨水,可以快速制取氨气。用此方法制取氨气应选用的气体发生装置是

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐1】某实验小组的同学在实验室利用下列装置进行实验。
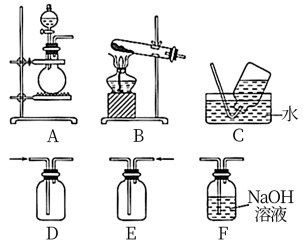
请回答下列问题:
(1)甲同学用铜与浓硝酸在A装置中制备NO2气体,上述装置中可用于收集NO2气体的是___ (填字母),A中发生反应的离子方程式为___ 。
(2)乙同学用图中的装置A进行铜与浓硫酸反应制取SO2气体,装置A中还缺少的仪器名称是___ ,该反应的化学方程式为___ 。
(3)丙同学用装置B制取氨气,发生反应的化学方程式是___ ;若将一端蘸有浓盐酸的玻璃棒接近导管口,观察到的现象是___ ,该反应的化学程式为___ 。
(4)丙同学在实验室中模拟氨的催化氧化反应,该反应中,当生成标准状况下11.2LNO时,被氧化物质的质量是___ g。

请回答下列问题:
(1)甲同学用铜与浓硝酸在A装置中制备NO2气体,上述装置中可用于收集NO2气体的是
(2)乙同学用图中的装置A进行铜与浓硫酸反应制取SO2气体,装置A中还缺少的仪器名称是
(3)丙同学用装置B制取氨气,发生反应的化学方程式是
(4)丙同学在实验室中模拟氨的催化氧化反应,该反应中,当生成标准状况下11.2LNO时,被氧化物质的质量是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】(Ⅰ)已知氯水有漂白性,是因为含有_________ (化学式),能与AgNO3反应生成_________ 色沉淀,是因为含有_______________ (名称)离子;
(Ⅱ)在下图所示的物质转化关系中,A是常见的气态氢化物,其水溶液呈碱性,B是能使带火星的木条复燃的无色无味气体, G是一种红色金属单质。(部分反应中生成物没有全部列出,反应条件未列出)

请回答下列问题:
(1)实验室制取A的化学方程式__________
(2)反应①的化学方程式为___________ 。当有1molA参加反应时,转移______ mol电子。
(3)反应②的化学方程式为________________________ 。
(4)反应③的离子方程式为_____________________
(Ⅱ)在下图所示的物质转化关系中,A是常见的气态氢化物,其水溶液呈碱性,B是能使带火星的木条复燃的无色无味气体, G是一种红色金属单质。(部分反应中生成物没有全部列出,反应条件未列出)

请回答下列问题:
(1)实验室制取A的化学方程式
(2)反应①的化学方程式为
(3)反应②的化学方程式为
(4)反应③的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,进行如下实验:
⑴溶液中肯定存在的离子是________________________ ;
⑵溶液中肯定不存在的离子是________________________ ;
⑶为进一步确定其他离子,应该补充的实验是_____________________________ ;____________________________ 。
| 实验步骤 | 实验现象 |
| ①取少量原溶液,加几滴甲基橙 | 溶液变红色 |
| ②取少量原溶液,浓缩,加Cu片和浓H2SO4,加热 | 有无色气体产生,后在空气中又变成红棕色 |
| ③取少量原溶液,加BaCl2溶液 | 有白色沉淀生成 |
| ④取③中上层清液,加AgNO3溶液 | 有白色沉淀生成,且不溶于HNO3 |
| ⑤取少量原溶液,加NaOH溶液 | 有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
⑴溶液中肯定存在的离子是
⑵溶液中肯定不存在的离子是
⑶为进一步确定其他离子,应该补充的实验是
您最近一年使用:0次




