有一无色透明溶液,欲确定是否含有下列离子:Na+、Mg2+、Al3+、Fe2+、Ba2+、NO3-、SO42-、Cl-、I-、HCO3-,进行如下实验:
⑴溶液中肯定存在的离子是________________________ ;
⑵溶液中肯定不存在的离子是________________________ ;
⑶为进一步确定其他离子,应该补充的实验是_____________________________ ;____________________________ 。
| 实验步骤 | 实验现象 |
| ①取少量原溶液,加几滴甲基橙 | 溶液变红色 |
| ②取少量原溶液,浓缩,加Cu片和浓H2SO4,加热 | 有无色气体产生,后在空气中又变成红棕色 |
| ③取少量原溶液,加BaCl2溶液 | 有白色沉淀生成 |
| ④取③中上层清液,加AgNO3溶液 | 有白色沉淀生成,且不溶于HNO3 |
| ⑤取少量原溶液,加NaOH溶液 | 有白色沉淀生成,当NaOH过量时沉淀部分溶解 |
⑴溶液中肯定存在的离子是
⑵溶液中肯定不存在的离子是
⑶为进一步确定其他离子,应该补充的实验是
9-10高二下·江苏南通·期末 查看更多[3]
更新时间:2019-01-30 18:14:09
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】某溶液中可能含有H+、Na+、NH 、Fe3+、Al3+、SO
、Fe3+、Al3+、SO 、CO
、CO 等离子。向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如图所示。
等离子。向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如图所示。
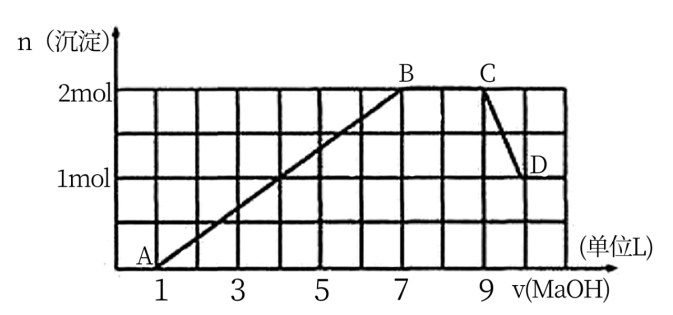
(1)A、B、C、D四点中沉淀成分相同的是(写代号)___________
(2)请写出BC、CD段发生反应的离子方程式___________ 、___________ 。
(3)由图象可推出原溶液中一定含有的金属离子有:___________
(4)若要检验可能存在的离子应采取的方法是___________
(5)原溶液中含有的Fe3+和Al3+的物质的量之比为___________
(6)由图象计算使用的NaOH溶液的物质的量浓度是___________
 、Fe3+、Al3+、SO
、Fe3+、Al3+、SO 、CO
、CO 等离子。向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如图所示。
等离子。向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如图所示。
(1)A、B、C、D四点中沉淀成分相同的是(写代号)
(2)请写出BC、CD段发生反应的离子方程式
(3)由图象可推出原溶液中一定含有的金属离子有:
(4)若要检验可能存在的离子应采取的方法是
(5)原溶液中含有的Fe3+和Al3+的物质的量之比为
(6)由图象计算使用的NaOH溶液的物质的量浓度是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】有一包白色固体粉末,其中可能含有NaCl、Ba(NO3)2、CuSO4、Na2CO3中的一种或几种,现做以下实验:
①取少量白色固体粉末于烧杯中,加水搅拌,有白色不溶物生成,过滤,滤液无色透明。
②取①的白色不溶物少量于试管中,加入足量稀硝酸,固体完全溶解,并有无色气泡产生。
③取①所得的滤液2 mL于试管中,滴入几滴稀硫酸,有白色沉淀产生。
④另取①得到的无色透明溶液少量于试管中,加入足量AgNO3溶液,产生白色沉淀。
根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是________________ (写化学式,下同),一定不含有的物质是________ 。
(2)写出各步变化的离子方程式。
①______________________________ ;
②_______________________________ ;
③________________________ ;
(3)查阅资料可知,铜和浓H2SO4共热,发生如下反应:
Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为
CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为______ 。
(4)亚硝酸钠易溶于水,水溶液显碱性,有氧化性,也有还原性。由于NaNO2有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
NaNO2+KI+ H2SO4 → NO↑+I2+K2SO4+Na2SO4+______。
请完成该化学方程式并配平:_____________________________ 。
①取少量白色固体粉末于烧杯中,加水搅拌,有白色不溶物生成,过滤,滤液无色透明。
②取①的白色不溶物少量于试管中,加入足量稀硝酸,固体完全溶解,并有无色气泡产生。
③取①所得的滤液2 mL于试管中,滴入几滴稀硫酸,有白色沉淀产生。
④另取①得到的无色透明溶液少量于试管中,加入足量AgNO3溶液,产生白色沉淀。
根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是
(2)写出各步变化的离子方程式。
①
②
③
(3)查阅资料可知,铜和浓H2SO4共热,发生如下反应:
Cu+2H2SO4(浓)
 CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为
CuSO4+SO2↑+2H2O,该反应中氧化剂与还原剂的个数之比为(4)亚硝酸钠易溶于水,水溶液显碱性,有氧化性,也有还原性。由于NaNO2有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
NaNO2+KI+ H2SO4 → NO↑+I2+K2SO4+Na2SO4+______。
请完成该化学方程式并配平:
您最近一年使用:0次
【推荐3】有5瓶白色固体试剂,分别是氯化钡、氢氧化钠、硫酸钠、硫酸铵、无水硫酸铜。现只提供蒸馏水,通过下面的实验步骤即可鉴别它们。已知: +OH-
+OH- NH3↑+H2O。 请填写下列空白:
NH3↑+H2O。 请填写下列空白:
(1)取适量固体试剂,分别加入5支试管中,加入适量蒸馏水,振荡试管,观察到的现象是_____________ ,被检出的化学物质是__________ 。
(2)分别取未检出的溶液,向其中加入上述已检出的溶液,根据观察到的现象写出相应的离子方程式:
第1支试管中有白色沉淀生成:____________________ ;
第2支试管中有蓝色沉淀生成:___________________ ;
被检出物质的化学式分别是____ 、______ 。
(3)鉴别余下未检出物质的方法是______________ ,观察到的现象是______________ 。
 +OH-
+OH- NH3↑+H2O。 请填写下列空白:
NH3↑+H2O。 请填写下列空白:(1)取适量固体试剂,分别加入5支试管中,加入适量蒸馏水,振荡试管,观察到的现象是
(2)分别取未检出的溶液,向其中加入上述已检出的溶液,根据观察到的现象写出相应的离子方程式:
第1支试管中有白色沉淀生成:
第2支试管中有蓝色沉淀生成:
被检出物质的化学式分别是
(3)鉴别余下未检出物质的方法是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐1】我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如下(部分物质已略去)。

已知:
①氨气极易溶于水,1体积水可溶解800体积氨气。
②几种盐的溶解度。
(1)写出过程①的化学方程式___________ 。原料有两种气体,应先通入___________ (填“ ”或“
”或“ ”),原因是
”),原因是__________________ 。
(2)操作①中析出 的原因是
的原因是___________ 。
a.碳酸氢钠难溶于水
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(3)制取的碱固体中还混有小苏打,如何除去杂质,写出化学方程式___________________ 。
(4)“侯氏制碱法”中除水外,能够循环利用的物质是___________ (填化学式)。
(5)检验产品碳酸钠中含有氯化钠,请你把以下实验方案补充完整:
操作:取少量试样溶于水中,再滴加___________ 。
现象:___________ 。

已知:
①氨气极易溶于水,1体积水可溶解800体积氨气。
②几种盐的溶解度。
| 物质 | NaCl |  |  |  |
| 溶解度 | 36.0 | 21.7 | 9.6 | 37.2 |
(1)写出过程①的化学方程式
 ”或“
”或“ ”),原因是
”),原因是(2)操作①中析出
 的原因是
的原因是a.碳酸氢钠难溶于水
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(3)制取的碱固体中还混有小苏打,如何除去杂质,写出化学方程式
(4)“侯氏制碱法”中除水外,能够循环利用的物质是
(5)检验产品碳酸钠中含有氯化钠,请你把以下实验方案补充完整:
操作:取少量试样溶于水中,再滴加
现象:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】浩瀚的海洋约占地球表面积的71%,它是一个巨大的宝藏。海水中水储量约为1.3×1018吨,约占地球上总水量的97%。
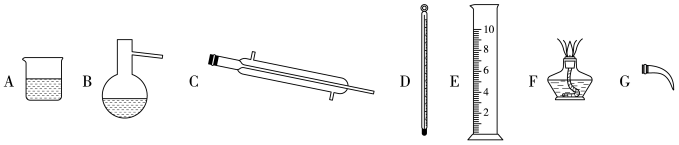
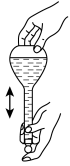
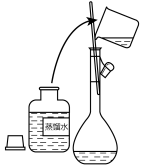
(1)海水淡化主要有蒸馏法。实验室进行水蒸馏的装置有_______ (选填必要序号)。
(2)某苦卤水中主要含有Mg2+、 、K+、Cl-等。根据图的溶解度曲线判断,从中获得K2SO4晶体的最佳方案是先加入适量
、K+、Cl-等。根据图的溶解度曲线判断,从中获得K2SO4晶体的最佳方案是先加入适量_______ 试剂,过滤,_______ 析晶。所得晶体中含有少量KCl杂质,简述实验检验其中Cl-的实验操作与现象_______ 。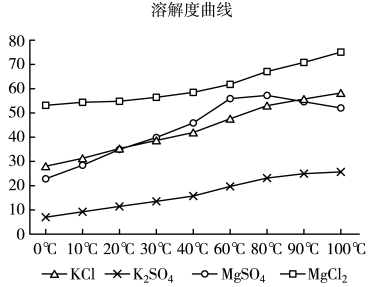
(3)海藻中富含碘元素,实验室模拟海藻提取KI的流程如下:

在灼烧、溶解、过滤、蒸发四个步骤中,均要使用到的一种实验仪器为_______ 。
(4)配制100mL 0.2mol/LKI溶液的操作如下,请正确排序_______ (填数字序号)。
(5)溶解了CO2的水可以溶解自然界中的碳酸钙,产生含 的天然水。写出相应的离子反应方程式
的天然水。写出相应的离子反应方程式_______ 。
(6)海水中含有大量矿物质,你认为海水中会富含石油吗?_______ (填“会”或“不会”)。
(1)海水淡化主要有蒸馏法。实验室进行水蒸馏的装置有

(2)某苦卤水中主要含有Mg2+、
 、K+、Cl-等。根据图的溶解度曲线判断,从中获得K2SO4晶体的最佳方案是先加入适量
、K+、Cl-等。根据图的溶解度曲线判断,从中获得K2SO4晶体的最佳方案是先加入适量
(3)海藻中富含碘元素,实验室模拟海藻提取KI的流程如下:

在灼烧、溶解、过滤、蒸发四个步骤中,均要使用到的一种实验仪器为
(4)配制100mL 0.2mol/LKI溶液的操作如下,请正确排序
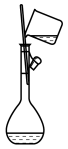 | 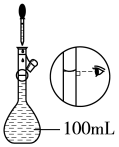 | 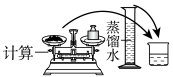 | 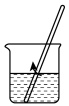 |  |  |
① | ② | ③ | ④ | ⑤ | ⑥ |
 的天然水。写出相应的离子反应方程式
的天然水。写出相应的离子反应方程式(6)海水中含有大量矿物质,你认为海水中会富含石油吗?
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐3】纯碱是一种非常重要的化工原料,在玻璃、肥料、合成洗涤剂等工业中有着广泛的应用。工业上“侯氏制碱法”以NaCl、NH3、CO2及水等为原料制备纯碱,其反应原理为: 。生产纯碱的工艺流程示意图如下:
。生产纯碱的工艺流程示意图如下:
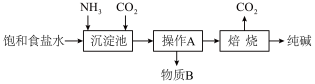
请回答下列问题:
(1)操作A的方法是___________ 。得到的NaHCO3晶体中可能含有少量NaCl、NH4Cl等杂质,检验该晶体中是否含有氯离子杂质的操作方法是___________ ,该工艺流程中可回收再利用的物质是___________ 。
(2)写出焙烧操作中的化学方程式___________ 。
(3)Na2CO3和NaHCO3是两种常见的钠盐,Na2CO3和NaHCO3溶于水溶液均显________ (填“酸性”、“中性”或“碱性”)。相同温度下在水中的溶解度
________  (填“大于”、“等于”或“小于”),写出向饱和碳酸钠溶液中通入CO2的离子方程式
(填“大于”、“等于”或“小于”),写出向饱和碳酸钠溶液中通入CO2的离子方程式___________ 。
 。生产纯碱的工艺流程示意图如下:
。生产纯碱的工艺流程示意图如下:
请回答下列问题:
(1)操作A的方法是
(2)写出焙烧操作中的化学方程式
(3)Na2CO3和NaHCO3是两种常见的钠盐,Na2CO3和NaHCO3溶于水溶液均显

 (填“大于”、“等于”或“小于”),写出向饱和碳酸钠溶液中通入CO2的离子方程式
(填“大于”、“等于”或“小于”),写出向饱和碳酸钠溶液中通入CO2的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】在一定条件下,某些化学反应可用下图表示,请回答下列问题。

(1)若A为一种单质,C、D均为气体且C能使澄清石灰水变浑浊,则B为________ 。
(2)若C是一种极易溶于水的气体,D是一种盐,试写出该反应的化学方程式_________ 。
(3)若C为红棕色气体,D为一种盐,写出符合上述框图反应关系的化学方程式_________ 。(写出其中的一个即可)。

(1)若A为一种单质,C、D均为气体且C能使澄清石灰水变浑浊,则B为
(2)若C是一种极易溶于水的气体,D是一种盐,试写出该反应的化学方程式
(3)若C为红棕色气体,D为一种盐,写出符合上述框图反应关系的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】工业上在一定条件下可用 将
将 还原,减少二氧化氮的污染。某同学在实验室对该反应进行了模拟,实验设计如下图所示(部分夹持装置省略):
还原,减少二氧化氮的污染。某同学在实验室对该反应进行了模拟,实验设计如下图所示(部分夹持装置省略):
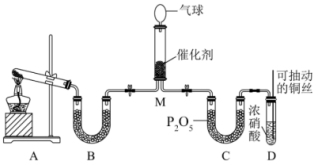
(1)用装置A制备 ,其中发生反应的化学方程式是
,其中发生反应的化学方程式是_______ 。
(2)装置B内的干燥剂是_______ 。
(3)装置D中发生反应的离子方程式是_______ ;铜丝设计为可抽动的目的_______ 。
(4)M装置可将 与
与 转化为环境友好的气体,其反应化学方程式是
转化为环境友好的气体,其反应化学方程式是_______ 。
 将
将 还原,减少二氧化氮的污染。某同学在实验室对该反应进行了模拟,实验设计如下图所示(部分夹持装置省略):
还原,减少二氧化氮的污染。某同学在实验室对该反应进行了模拟,实验设计如下图所示(部分夹持装置省略):
(1)用装置A制备
 ,其中发生反应的化学方程式是
,其中发生反应的化学方程式是(2)装置B内的干燥剂是
(3)装置D中发生反应的离子方程式是
(4)M装置可将
 与
与 转化为环境友好的气体,其反应化学方程式是
转化为环境友好的气体,其反应化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】氮的氧化物( )是大气污染物之一,工业上在一定温度和催化剂条件下用
)是大气污染物之一,工业上在一定温度和催化剂条件下用 将
将 还原生成
还原生成 ,某同学在实验室中对
,某同学在实验室中对 与
与 反应进行了探究。某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。回答下列问题:
反应进行了探究。某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。回答下列问题:___________ ;装置 中圆底烧瓶收集氨气时,请选择氨气的进气口:
中圆底烧瓶收集氨气时,请选择氨气的进气口:___________ (填“ ”或“
”或“ ”)。
”)。
(2)若观察到装置 中的烧瓶内产生了红色喷泉,则说明氨气极易溶于水且水溶液显
中的烧瓶内产生了红色喷泉,则说明氨气极易溶于水且水溶液显___________ 性。
(3)将前面收集到的 充入注射器
充入注射器 中,硬质玻璃管
中,硬质玻璃管 中加入少量催化剂、充入
中加入少量催化剂、充入 (两端用夹子
(两端用夹子 、
、 夹好)。
夹好)。 ,推动注射器活塞,使
,推动注射器活塞,使 中的气体缓慢通入硬质玻璃管
中的气体缓慢通入硬质玻璃管 中,产物无污染,其中反应的化学方程式为
中,产物无污染,其中反应的化学方程式为___________ 。
(4) 与水反应的化学方程式为
与水反应的化学方程式为___________ ,其中氧化剂与还原剂的物质的量之比是___________ 。
(5)写出木炭与浓 反应的化学方程式:
反应的化学方程式:___________ 。
 )是大气污染物之一,工业上在一定温度和催化剂条件下用
)是大气污染物之一,工业上在一定温度和催化剂条件下用 将
将 还原生成
还原生成 ,某同学在实验室中对
,某同学在实验室中对 与
与 反应进行了探究。某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。回答下列问题:
反应进行了探究。某化学实验小组同学利用以下装置制备氨气,并探究氨气的性质(部分仪器已略去)。回答下列问题: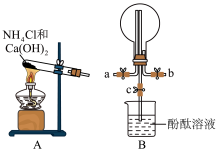
 中圆底烧瓶收集氨气时,请选择氨气的进气口:
中圆底烧瓶收集氨气时,请选择氨气的进气口: ”或“
”或“ ”)。
”)。(2)若观察到装置
 中的烧瓶内产生了红色喷泉,则说明氨气极易溶于水且水溶液显
中的烧瓶内产生了红色喷泉,则说明氨气极易溶于水且水溶液显(3)将前面收集到的
 充入注射器
充入注射器 中,硬质玻璃管
中,硬质玻璃管 中加入少量催化剂、充入
中加入少量催化剂、充入 (两端用夹子
(两端用夹子 、
、 夹好)。
夹好)。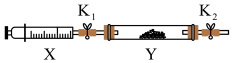
 ,推动注射器活塞,使
,推动注射器活塞,使 中的气体缓慢通入硬质玻璃管
中的气体缓慢通入硬质玻璃管 中,产物无污染,其中反应的化学方程式为
中,产物无污染,其中反应的化学方程式为(4)
 与水反应的化学方程式为
与水反应的化学方程式为(5)写出木炭与浓
 反应的化学方程式:
反应的化学方程式:
您最近一年使用:0次
【推荐1】现有一混合溶液,可能含有以下离子中的若干种:Na+、K+、Ca2+、C1-、 、
、 。取少量该混合溶液进行如下实验:
。取少量该混合溶液进行如下实验:
实验①:用洁净的铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察火焰为紫色;
实验②:向混合溶液中加入足量BaCl2溶液,有白色沉淀生成,过滤;
实验③:向②中得到的白色沉淀中加入足量盐酸,沉淀完全溶解并产生气泡;
实验④:向②过滤后的溶液中加入硝酸银溶液,产生白色沉淀。
回答下列问题:
(1)由实验①推断该混合溶液中一定含有的离子是___________ (填离子符号,下同),检验该离子的实验方法的名称是___________ 。
(2)由实验②③推断该混合溶液中一定含有的离子是___________ ,一定不含的离子有___________ 。实验③中发生反应的离子反应方程式为___________ 。
(3)综合上述实验,是否能确定该混合溶液中含有Cl-_______ (填“是”或“否”)。若“是”下一空无需作答,若“否”请写出检验该混合溶液中Cl-的实验操作及现象___________ 。
 、
、 。取少量该混合溶液进行如下实验:
。取少量该混合溶液进行如下实验:实验①:用洁净的铂丝蘸取溶液,在火焰上灼烧,透过蓝色钴玻璃观察火焰为紫色;
实验②:向混合溶液中加入足量BaCl2溶液,有白色沉淀生成,过滤;
实验③:向②中得到的白色沉淀中加入足量盐酸,沉淀完全溶解并产生气泡;
实验④:向②过滤后的溶液中加入硝酸银溶液,产生白色沉淀。
回答下列问题:
(1)由实验①推断该混合溶液中一定含有的离子是
(2)由实验②③推断该混合溶液中一定含有的离子是
(3)综合上述实验,是否能确定该混合溶液中含有Cl-
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
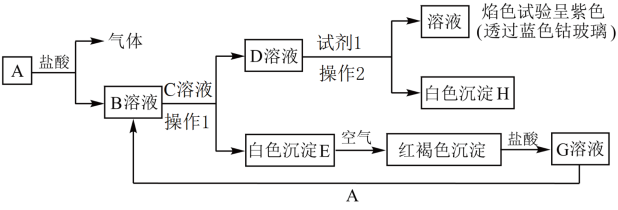
【推荐2】A、B、C、D、F五种物质的焰色反应均为黄色,A、B、C、D与盐酸反应均生成E,此外B还生成一种可燃性气体,C、D还生成一种无色无味气体H,H气体能使澄清石灰水变浑浊。D和A可反应生成C,F和H可反应生成C和另一种无色无味气体(可助燃)。请回答下列问题:
(1)写出下列物质的化学式:A_______ ,E_______ ,F_______
(2)写出下列反应的离子方程式:
①D+盐酸:_______ 。
②B+水:_______ 。
(1)写出下列物质的化学式:A
(2)写出下列反应的离子方程式:
①D+盐酸:
②B+水:
您最近一年使用:0次