浩瀚的海洋约占地球表面积的71%,它是一个巨大的宝藏。海水中水储量约为1.3×1018吨,约占地球上总水量的97%。
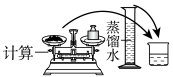
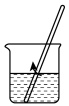
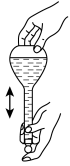
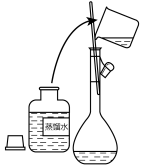
(1)海水淡化主要有蒸馏法。实验室进行水蒸馏的装置有_______ (选填必要序号)。
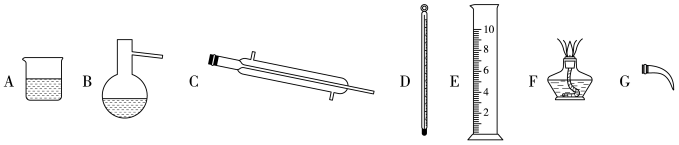
(2)某苦卤水中主要含有Mg2+、 、K+、Cl-等。根据图的溶解度曲线判断,从中获得K2SO4晶体的最佳方案是先加入适量
、K+、Cl-等。根据图的溶解度曲线判断,从中获得K2SO4晶体的最佳方案是先加入适量_______ 试剂,过滤,_______ 析晶。所得晶体中含有少量KCl杂质,简述实验检验其中Cl-的实验操作与现象_______ 。
(3)海藻中富含碘元素,实验室模拟海藻提取KI的流程如下:

在灼烧、溶解、过滤、蒸发四个步骤中,均要使用到的一种实验仪器为_______ 。
(4)配制100mL 0.2mol/LKI溶液的操作如下,请正确排序_______ (填数字序号)。
(5)溶解了CO2的水可以溶解自然界中的碳酸钙,产生含 的天然水。写出相应的离子反应方程式
的天然水。写出相应的离子反应方程式_______ 。
(6)海水中含有大量矿物质,你认为海水中会富含石油吗?_______ (填“会”或“不会”)。
(1)海水淡化主要有蒸馏法。实验室进行水蒸馏的装置有

(2)某苦卤水中主要含有Mg2+、
 、K+、Cl-等。根据图的溶解度曲线判断,从中获得K2SO4晶体的最佳方案是先加入适量
、K+、Cl-等。根据图的溶解度曲线判断,从中获得K2SO4晶体的最佳方案是先加入适量
(3)海藻中富含碘元素,实验室模拟海藻提取KI的流程如下:

在灼烧、溶解、过滤、蒸发四个步骤中,均要使用到的一种实验仪器为
(4)配制100mL 0.2mol/LKI溶液的操作如下,请正确排序
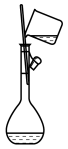 | 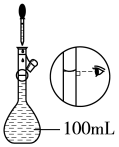 |  |  |  |  |
① | ② | ③ | ④ | ⑤ | ⑥ |
 的天然水。写出相应的离子反应方程式
的天然水。写出相应的离子反应方程式(6)海水中含有大量矿物质,你认为海水中会富含石油吗?
更新时间:2021/02/09 07:42:36
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】我国化学侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下:

(1)实验室制取氨气的反应方程式为______
(2)上述生产纯碱过程副产品是______ 。
(3)沉淀池中发生的化学反应方程式是______ 。
(4)写出上述流程中X物质的电子式______ 。
(5)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了______ (选填循环Ⅰ或循环Ⅱ)的循环。从沉淀池中取出沉淀的操作是_________ 。
(6)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加________ 。

(1)实验室制取氨气的反应方程式为
(2)上述生产纯碱过程副产品是
(3)沉淀池中发生的化学反应方程式是
(4)写出上述流程中X物质的电子式
(5)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了
(6)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
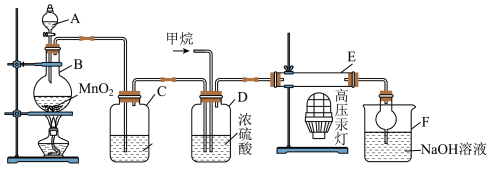
【推荐2】某学习小组为探究甲烷与氯气的反应,设计了如下图所示的装置。
(1)装置C中的试剂为_____ 。
(2)装置E中经过高压汞灯的强光照射,E中的实验现象有_____ 。
(3)装置F中球形干燥管的作用是_____ 。
(4)某同学取反应后F中的溶液,加入足量硝酸酸化的硝酸银溶液,产生白色沉淀,或证明甲烷与氯气发生了取代反应,你认为是否合_____ (填“合理”或“不合理”),请说明理由:_____ 。
(1)装置C中的试剂为
(2)装置E中经过高压汞灯的强光照射,E中的实验现象有
(3)装置F中球形干燥管的作用是
(4)某同学取反应后F中的溶液,加入足量硝酸酸化的硝酸银溶液,产生白色沉淀,或证明甲烷与氯气发生了取代反应,你认为是否合
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
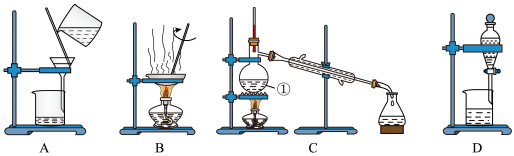
(1)在装置A和装置B中都用到玻璃棒,装置A中玻璃棒的作用是__ ,装置B中玻璃棒的作用是__ ,防止蒸发皿内溶液因局部过热而溅出。
(2)装置C中①的名称是__ ,①中加入沸石的作用是__ ,冷却水的方向是__ 。
(3)从氯化钠溶液中得到氯化钠固体,选择装置__ (填代表装置图的字母,下同);除去自来水中的Cl−等杂质,选择装置__ 。检验自来水中Cl-是否除净的方法:取少量锥形瓶中的水于洁净试管中,滴加__ ,不产生白色沉淀表明Cl−已除净。

(1)在装置A和装置B中都用到玻璃棒,装置A中玻璃棒的作用是
(2)装置C中①的名称是
(3)从氯化钠溶液中得到氯化钠固体,选择装置
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某种抗酸药的有效成分为碳酸氢钠,测定其中碳酸氢钠含量的操作如下(设该药片中的其他成分不与盐酸或氢氧化钠反应):
①配制250mL1.0 mol•L-1稀盐酸和100mL1.0 mol•L-1NaOH溶液;
②向4片研碎后的药片中加入20.0mL蒸馏水;
③加入25.0mL1.0 mol•L-1稀盐酸;
④用1.0 mol•L-1NaOH溶液中和过量的稀盐酸,消耗NaOH溶液的体积为5.0mL。
请回答下列问题:
(1)需称取NaOH固体_______ g。
(2)配制250mL1.0 mol•L-1稀盐酸,需要用到的玻璃仪器有烧杯、量筒、_____ 、_____ 、____ 。
(3)写出步骤③加入稀盐酸发生反应的离子方程式______ 。
(4)配制NaOH溶液过程中,定容时俯视刻度线,则所配溶液浓度______ (填“偏高”“偏低”“无影响”,下同),用该NaOH做上述实验,测得碳酸氢钠含量_____ 。
(5)该药片中碳酸氢钠的含量为_____ g/片。
①配制250mL1.0 mol•L-1稀盐酸和100mL1.0 mol•L-1NaOH溶液;
②向4片研碎后的药片中加入20.0mL蒸馏水;
③加入25.0mL1.0 mol•L-1稀盐酸;
④用1.0 mol•L-1NaOH溶液中和过量的稀盐酸,消耗NaOH溶液的体积为5.0mL。
请回答下列问题:
(1)需称取NaOH固体
(2)配制250mL1.0 mol•L-1稀盐酸,需要用到的玻璃仪器有烧杯、量筒、
(3)写出步骤③加入稀盐酸发生反应的离子方程式
(4)配制NaOH溶液过程中,定容时俯视刻度线,则所配溶液浓度
(5)该药片中碳酸氢钠的含量为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】实验室需要配制100 mL 1mol·L-1的NaOH溶液,进行如下操作:
(1)配制该溶液所需主要仪器除了托盘天平、玻璃棒、烧杯、胶头滴管,还需要的玻璃仪器是___________ 。
(2)计算需要NaOH固体的质量:___________ g.
(3)取出50 mL配制好的溶液,此溶液中NaOH的物质的量浓度为___________ 。
(4)若出现如下情况,导致所配溶液浓度偏高的是___________。
(1)配制该溶液所需主要仪器除了托盘天平、玻璃棒、烧杯、胶头滴管,还需要的玻璃仪器是
(2)计算需要NaOH固体的质量:
(3)取出50 mL配制好的溶液,此溶液中NaOH的物质的量浓度为
(4)若出现如下情况,导致所配溶液浓度偏高的是___________。
| A.称量时砝码已经生锈 |
| B.定容时仰视 |
| C.溶解、转移溶液之后没有对烧杯和玻璃棒进行洗涤操作 |
| D.定容摇匀后,液面低于容量瓶颈上的刻度线 |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐3】掌握仪器名称、组装及使用是中学化学实验的基础,下图为两套实验装置。

(1)写出仪器b的名称__________________ 。
(2)仪器a~e中,使用前必须检查是否漏水的有___________ (填序号)。
(3)利用装置Ⅰ分离四氯化碳和酒精的混合物,温度计水银球的位置应位于_______ 处。冷凝水应由__________________ (填“f”或“g”)口通入。
(4)现需配制 溶液450mL,装置Ⅱ是某同学转移溶液的示意图。
溶液450mL,装置Ⅱ是某同学转移溶液的示意图。
①图中的错误是________ 。除了图中给出的仪器外,为完成本实验还需要的玻璃 仪器有_______ 。
②根据计算得知,需称量 的质量为
的质量为__________________ g。
③下列操作使配制的 溶液浓度偏低的有
溶液浓度偏低的有__________________ 。
A.将砝码放在左盘上, 放在右盘上进行称量(使用游码)
放在右盘上进行称量(使用游码)
B.容量瓶用蒸馏水洗净后,未待干燥便用来配制
C.定容时俯视刻度线
D.定容摇匀后,液面下降,又加水至刻度线

(1)写出仪器b的名称
(2)仪器a~e中,使用前必须检查是否漏水的有
(3)利用装置Ⅰ分离四氯化碳和酒精的混合物,温度计水银球的位置应位于
(4)现需配制
 溶液450mL,装置Ⅱ是某同学转移溶液的示意图。
溶液450mL,装置Ⅱ是某同学转移溶液的示意图。①图中的错误是
②根据计算得知,需称量
 的质量为
的质量为③下列操作使配制的
 溶液浓度偏低的有
溶液浓度偏低的有A.将砝码放在左盘上,
 放在右盘上进行称量(使用游码)
放在右盘上进行称量(使用游码)B.容量瓶用蒸馏水洗净后,未待干燥便用来配制
C.定容时俯视刻度线
D.定容摇匀后,液面下降,又加水至刻度线
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】已知某工业废水中含有大量 CuSO4,少量 Ag+、Hg2+以及部分污泥,通过下述过程可从该废水中回收硫酸铜晶体及其它物质。

(1)步骤 1 的主要操作是___________ ,需用到的玻璃仪器除烧杯外还有____________ 。
(2)步骤 2 中需加入某种试剂后再将混合物分离,该试剂是(填化学式)_________________ ,生成固体残渣成分是(填化学式)______________ 。
步骤 3 中涉及的操作是:蒸发浓缩、______________________ 、过滤、干燥。
步骤 2 应该在通风橱中进行,原因是_______________________________________ 。

(1)步骤 1 的主要操作是
(2)步骤 2 中需加入某种试剂后再将混合物分离,该试剂是(填化学式)
步骤 3 中涉及的操作是:蒸发浓缩、
步骤 2 应该在通风橱中进行,原因是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如下图所示步骤进行操作。回答下列问题:

(1)试剂Ⅰ的化学式为_______ 。
(2)试剂Ⅱ的化学式为_______ ,②中加入试剂Ⅱ的目的是除去A中的____ ,检验该离子已经除尽的方法是________________________________________________________ 。
(3)③中发生反应的化学方程式为_________________________________________________ 。
(4)由E得到KCl晶体的实验操作是_______________ 。

(1)试剂Ⅰ的化学式为
(2)试剂Ⅱ的化学式为
(3)③中发生反应的化学方程式为
(4)由E得到KCl晶体的实验操作是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】I.已知:甲、乙、丙、丁为常见化合物,A、B为单质,相互转化关系如图。其中甲是天然气的主要成分。回答下列问题:
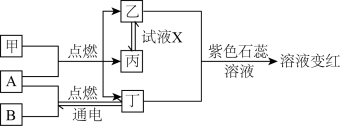
(1)丁物质的名称:_______ ;
(2)检验化合物乙的化学方程式_______ ;
(3)试剂X可能的化学式_______ 、_______ (要求:所选物质类别不同);
II.海水晒制粗盐的主要成分为 , 还含有少量的
, 还含有少量的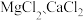 、
、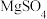 、泥沙等杂质。下面是由粗盐获取较纯净精盐的一种方法:
、泥沙等杂质。下面是由粗盐获取较纯净精盐的一种方法:
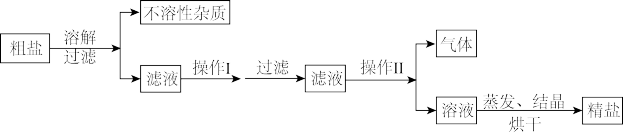
请分析上面流程图示,回答:
(4)为除去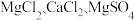 可溶性杂质, 操作 I 中依次加入的物质 (过量) 和顺序, 合理的是_______;
可溶性杂质, 操作 I 中依次加入的物质 (过量) 和顺序, 合理的是_______;
(5)操作I过量加入各物质的目的是_______ ;
(6)为获取较纯净精盐,操作II的具体方法是_______ 。

(1)丁物质的名称:
(2)检验化合物乙的化学方程式
(3)试剂X可能的化学式
II.海水晒制粗盐的主要成分为
 , 还含有少量的
, 还含有少量的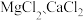 、
、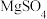 、泥沙等杂质。下面是由粗盐获取较纯净精盐的一种方法:
、泥沙等杂质。下面是由粗盐获取较纯净精盐的一种方法:
请分析上面流程图示,回答:
(4)为除去
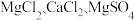 可溶性杂质, 操作 I 中依次加入的物质 (过量) 和顺序, 合理的是_______;
可溶性杂质, 操作 I 中依次加入的物质 (过量) 和顺序, 合理的是_______;A. |
B. |
C.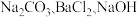 |
D.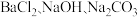 |
(6)为获取较纯净精盐,操作II的具体方法是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐1】回答下列问题:
(1)写出图中①~④仪器的名称:
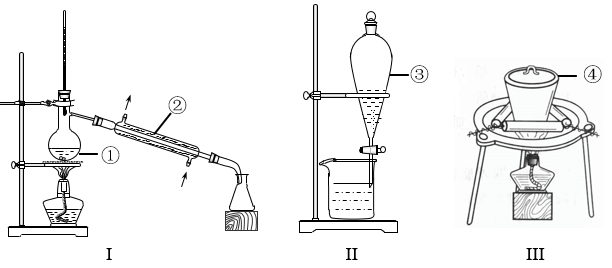
①___________ ;②___________ ;③___________ ;④___________ 。
(2)仪器①~④中,使用时必须检查是否漏水的有___________ 。(填序号)
(3)分离碘水中的碘单质,可先向碘水中加入___________ (填“CCl4”或“乙醇”),现象是___________ ,选择装置___________ (填“Ⅰ”“Ⅱ”或“Ⅲ”) 进行___________ (填操作名称),再选装置___________ (填“Ⅰ”“Ⅱ”或“Ⅲ”)进行分离。
(1)写出图中①~④仪器的名称:

①
(2)仪器①~④中,使用时必须检查是否漏水的有
(3)分离碘水中的碘单质,可先向碘水中加入
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】粗盐提纯实验的科学探究。
I.粗盐中含有较多的杂质,化学兴趣小组同学按照课本“活动与探究”的要求做粗盐提纯实验。
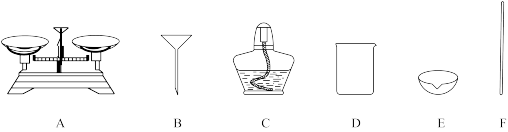
(1)“活动与探究”中,操作步骤有:①计算产率、②过滤、③溶解、④蒸发,正确的操作顺序为___________ (填序号)。
(2)仪器B的名称是___________ ,在实验中三个步骤中都须使用的一种仪器是___________ (填序号)。
(3)称量食盐应放在仪器A的___________ 盘,蒸发时防止液滴飞溅的操作是___________ 。
II.化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙。设计实验方案如下,请参与实验并回答问题。
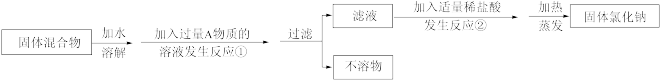
(4)写出A物质的化学式:___________ ,写出A物质的俗称:___________ 。
(5)写出反应②的化学方程式:___________ 。
(6)反应①中加入过量A物质的目的是___________ ;反应②中如果加入盐酸也过量,则对所得到的氯化钠纯度___________ (填“有”或“没有”)影响。
(7)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果___________ (填“增大”、“不变”或“减少”)。
III.化学活动小组查阅资料发现,粗盐中除NaCl外,还含有MgCl2、CaCl2、MgSO4以及泥沙等杂质。他们要除去杂质得到精盐,设计了下列实验方案(序号①~⑧表示实验操作,用于沉淀的试剂稍过量 ):
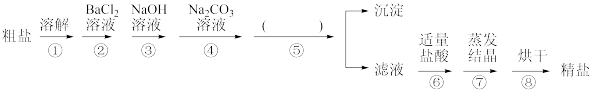
根据上述方案,回答下列问题:
(8)操作①中玻璃棒的作用是___________ 。
(9)第⑤步操作的名称是___________ 。
(10) “蒸发结晶”用到的器材有:铁架台(铁圈)、坩埚钳、石棉网、火柴、玻璃棒、___________ 、酒精灯。
(11)实验中加入“Na2CO3溶液”的目的是___________ 。
(12)利用提供的沉淀试剂,另写出一种添加试剂的操作顺序(填序号):___________ 。
IV.化学兴趣小组同学模拟“海水淡化工业”来制取蒸馏水。实验装置图如下:
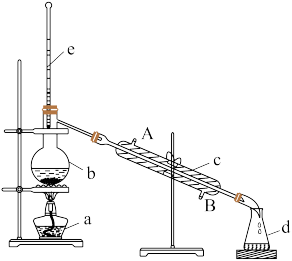
(13)仪器c的名称是___________ 。
(14)该分离混合物的原理是利用___________ 不同,通过加热的方式使其分离。
(15)冷水进水端是___________ 端( 填 A或B )
(16)为防暴沸需向___________ (填仪器名称)中加入___________ (填物品)。
I.粗盐中含有较多的杂质,化学兴趣小组同学按照课本“活动与探究”的要求做粗盐提纯实验。

(1)“活动与探究”中,操作步骤有:①计算产率、②过滤、③溶解、④蒸发,正确的操作顺序为
(2)仪器B的名称是
(3)称量食盐应放在仪器A的
II.化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙。设计实验方案如下,请参与实验并回答问题。

(4)写出A物质的化学式:
(5)写出反应②的化学方程式:
(6)反应①中加入过量A物质的目的是
(7)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果
III.化学活动小组查阅资料发现,粗盐中除NaCl外,还含有MgCl2、CaCl2、MgSO4以及泥沙等杂质。他们要除去杂质得到精盐,设计了下列实验方案(序号①~⑧表示实验操作,用于沉淀的试剂稍

根据上述方案,回答下列问题:
(8)操作①中玻璃棒的作用是
(9)第⑤步操作的名称是
(10) “蒸发结晶”用到的器材有:铁架台(铁圈)、坩埚钳、石棉网、火柴、玻璃棒、
(11)实验中加入“Na2CO3溶液”的目的是
(12)利用提供的沉淀试剂,另写出一种添加试剂的操作顺序(填序号):
IV.化学兴趣小组同学模拟“海水淡化工业”来制取蒸馏水。实验装置图如下:

(13)仪器c的名称是
(14)该分离混合物的原理是利用
(15)冷水进水端是
(16)为防暴沸需向
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】(Ⅰ)用下列仪器的编号回答问题:①容量瓶②蒸馏烧瓶③量筒④烧杯⑤托盘天平⑥分液漏斗
(1)加热时必须垫石棉网的有____________________ 。
(2)使用时必须检查是否漏水的有______________ 。
(3) 标有零刻度的有______________ 。
(Ⅱ)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取法 B.加热分解 C.结晶法 D.分液法 E.蒸馏法 F.过滤法
(4)_____ 分离饱和食盐水和沙子的混合物;
(5)_____ 从硝酸钾和氯化钠的混合溶液中获得硝酸钾;
(6)______ 分离水和苯的混合物;
(7)_____ 分离四氯化碳(沸点76.75℃)和甲苯(沸点为110.6℃),已知四氯化碳和甲苯互溶。
(1)加热时必须垫石棉网的有
(2)使用时必须检查是否漏水的有
(3) 标有零刻度的有
(Ⅱ)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取法 B.加热分解 C.结晶法 D.分液法 E.蒸馏法 F.过滤法
(4)
(5)
(6)
(7)
您最近一年使用:0次



