如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
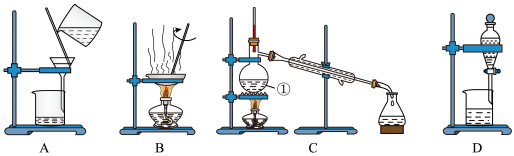
(1)在装置A和装置B中都用到玻璃棒,装置A中玻璃棒的作用是__ ,装置B中玻璃棒的作用是__ ,防止蒸发皿内溶液因局部过热而溅出。
(2)装置C中①的名称是__ ,①中加入沸石的作用是__ ,冷却水的方向是__ 。
(3)从氯化钠溶液中得到氯化钠固体,选择装置__ (填代表装置图的字母,下同);除去自来水中的Cl−等杂质,选择装置__ 。检验自来水中Cl-是否除净的方法:取少量锥形瓶中的水于洁净试管中,滴加__ ,不产生白色沉淀表明Cl−已除净。

(1)在装置A和装置B中都用到玻璃棒,装置A中玻璃棒的作用是
(2)装置C中①的名称是
(3)从氯化钠溶液中得到氯化钠固体,选择装置
更新时间:2020-03-09 09:52:42
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】化学学习小组模拟侯德榜制碱法制取Na2CO3的过程如下:

已知:①反应Ⅰ的化学方程式为:NH3+H2O+CO2=NH4HCO3
②滤液含NH4Cl等溶质
⑴反应Ⅱ为复分解反应,写出该反应的化学方程式______ 。
⑵验证滤液中含Cl-离子的实验方法和现象为______ 。
⑶反应Ⅲ的化学方程式为______ 。

已知:①反应Ⅰ的化学方程式为:NH3+H2O+CO2=NH4HCO3
②滤液含NH4Cl等溶质
⑴反应Ⅱ为复分解反应,写出该反应的化学方程式
⑵验证滤液中含Cl-离子的实验方法和现象为
⑶反应Ⅲ的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】我国化学侯德榜改革国外的纯碱生产工艺,生产流程可简要表示如下:

(1)实验室制取氨气的反应方程式为______
(2)上述生产纯碱过程副产品是______ 。
(3)沉淀池中发生的化学反应方程式是______ 。
(4)写出上述流程中X物质的电子式______ 。
(5)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了______ (选填循环Ⅰ或循环Ⅱ)的循环。从沉淀池中取出沉淀的操作是_________ 。
(6)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加________ 。

(1)实验室制取氨气的反应方程式为
(2)上述生产纯碱过程副产品是
(3)沉淀池中发生的化学反应方程式是
(4)写出上述流程中X物质的电子式
(5)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了
(6)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】回答下列问题:

(1)写出下列仪器的名称:①_____ ,②_____ ,④_____ 。
(2)仪器①~④中,使用时必须检查是否漏水的是_____ (填序号)。
(3)若利用装置I分离酒精和水的混合物,还缺少的仪器_____ ,将仪器补充完整后进行的实验操作的名称为_____ ;②的进水口是_____ (填“f”或“g”)。
(4)现需配制250mL、0.2mol•L-1NaCl溶液,装置II是某同学转移溶液的示意图,指出图中的错误操作:______ 。

(1)写出下列仪器的名称:①
(2)仪器①~④中,使用时必须检查是否漏水的是
(3)若利用装置I分离酒精和水的混合物,还缺少的仪器
(4)现需配制250mL、0.2mol•L-1NaCl溶液,装置II是某同学转移溶液的示意图,指出图中的错误操作:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】某同学设计如下实验方案,以分离NaCl和BaCl2两种固体混合物,回答下列问题:

供选试剂:Na2CO3溶液、Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸
(1)操作②的名称是_____ 。
(2)试剂a是____ (填化学式,下同),试剂b是___ ,固体B是____ 。
(3)加入试剂a、b分别所发生的化学反应方程式为____ 、____ 。
(4)该方案能否达到实验目的___ 。若不能,应如何改进(若能,此问不用回答)____ 。

供选试剂:Na2CO3溶液、Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸
(1)操作②的名称是
(2)试剂a是
(3)加入试剂a、b分别所发生的化学反应方程式为
(4)该方案能否达到实验目的
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】如下图所示是中学化学中常用于混合物分离和提纯的装置:
A.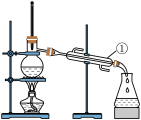 B.
B. 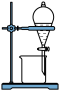 C.
C. 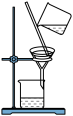 D.
D. 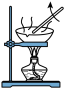
请根据装置图回答下列问题:
(1)从氯化钾溶液中得到氯化钾固体选择装置______ (填代表装置图的字母,下同);除去自来水中的Cl-等杂质得到蒸馏水,选择装置_____ 。
(2)从碘水中分离出I2,选择装置____ ,该分离方法的名称为________ 。
(3)装置A中①的名称是________ ,冷凝水流动的方向是__________ 。
(4)分液时要注意及时________ ,防止上层液体流下。分液后漏斗内剩余的液体从分液漏斗的________ (填“上口”或“下口”)倒入烧杯。
A.
 B.
B.  C.
C.  D.
D. 
请根据装置图回答下列问题:
(1)从氯化钾溶液中得到氯化钾固体选择装置
(2)从碘水中分离出I2,选择装置
(3)装置A中①的名称是
(4)分液时要注意及时
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】航天员王亚平在“天宫课堂”中介绍了空间站中的生活,在轨演示了水球变气球等一系列炫酷又好玩的实验。
Ⅰ.“天宫”中水和氧气的最大化利用是保障生活的重要措施。如图是空间站常用资源再利用模拟图。
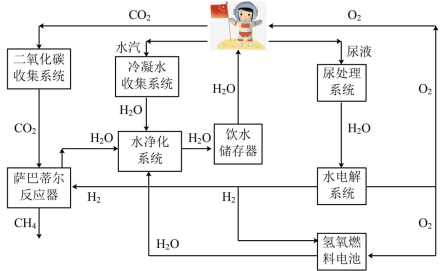
(1)“尿处理系统”采用蒸馏方法对其中成分进行分离。此方法是根据尿液中各成分的___________ 不同进行分离的。
(2)“水电解系统”中发生反应的化学方程式为___________ 。
(3)在水净化系统中,用臭氧( )消素,臭氧在一定条件下转化为氧气的化学方程式为:
)消素,臭氧在一定条件下转化为氧气的化学方程式为:___________ ;该反应___________ (填“属于”或“不属于”)氧化还原反应。
(4)在一定条件下,“萨巴蒂尔反应器”可以除去 ,该反应的化学方程式为
,该反应的化学方程式为_________ 。
Ⅱ.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不溢出,使水球越来越大。
(5)泡腾片在水中发生了如下反应:
___________ (补全化学方程式)。
(6)如果在空间站失重状态下收集制得的氧气,可以选用下列装置中的___________(填序号)。
Ⅰ.“天宫”中水和氧气的最大化利用是保障生活的重要措施。如图是空间站常用资源再利用模拟图。

(1)“尿处理系统”采用蒸馏方法对其中成分进行分离。此方法是根据尿液中各成分的
(2)“水电解系统”中发生反应的化学方程式为
(3)在水净化系统中,用臭氧(
 )消素,臭氧在一定条件下转化为氧气的化学方程式为:
)消素,臭氧在一定条件下转化为氧气的化学方程式为:(4)在一定条件下,“萨巴蒂尔反应器”可以除去
 ,该反应的化学方程式为
,该反应的化学方程式为Ⅱ.王亚平将蓝色颜料注入水球中,整个水球变成蓝色,将泡腾片放入水球中,产生大量气泡向四面八方扩散,充满整个水球。气体并不溢出,使水球越来越大。
(5)泡腾片在水中发生了如下反应:

(6)如果在空间站失重状态下收集制得的氧气,可以选用下列装置中的___________(填序号)。
A. | B.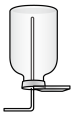 | C.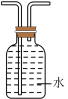 | D. |
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】实验室用苯和液溴制取溴苯并验证其反应类型的实验装置图(夹持装置略)及有关数据如下,按下列步骤回答有关问题。
_______ 。
(2)在a中加入15mL无水苯和少量铁屑,在b中小心加入4mL液态溴,向a中滴入液溴,有白雾生成,a中发生反应的化学方程式为_______ 。
(3)d中CCl4的作用是_______ ;e中出现_______ ,则说明苯与液溴发生了取代反应。
(4)充分反应后,经过下列步骤分离提纯。
①反应后a瓶中的溴苯因溶有溴而显褐色,提纯溴苯的过程中,除去溴苯中的溴依次用水、_______ 溶液、水洗涤。
②向分离出的粗溴苯中加入少量无水氯化钙,静置、过滤。加入氯化钙的目的是_______ 。
③已知苯与溴还可能发生副反应生成对二溴苯(沸点 和邻二溴苯(沸点
和邻二溴苯(沸点 要进一步提纯,再进行
要进一步提纯,再进行_______ (填操作名称)即可得到较纯净的溴苯,该过程中为了受热均匀和易于控制温度,可采用_______ (填“水浴”或“油浴”)加热。
| 苯 | 溴 | 溴苯 | |
| 密度/(g·cm⁻³) | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解性 | 微溶 | 微溶 | 微溶 |

(2)在a中加入15mL无水苯和少量铁屑,在b中小心加入4mL液态溴,向a中滴入液溴,有白雾生成,a中发生反应的化学方程式为
(3)d中CCl4的作用是
(4)充分反应后,经过下列步骤分离提纯。
①反应后a瓶中的溴苯因溶有溴而显褐色,提纯溴苯的过程中,除去溴苯中的溴依次用水、
②向分离出的粗溴苯中加入少量无水氯化钙,静置、过滤。加入氯化钙的目的是
③已知苯与溴还可能发生副反应生成对二溴苯(沸点
 和邻二溴苯(沸点
和邻二溴苯(沸点 要进一步提纯,再进行
要进一步提纯,再进行
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。
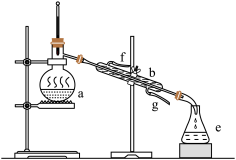
(1)写出下列仪器的名称:c.__________ 。
(2)仪器a~e中,使用前必须检查是否漏水的有___________ 。(填序号)
(3)若利用装置分离四氯化碳和酒精的混合物,温度计水银球的位置在_______ 处。冷凝水由____ 口流出(填f或g)。
(4)现需配制0.1mol/LNaOH溶液450mL,装置是某同学转移溶液的示意图。
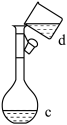
①图中的错误是___________________ 。
②根据计算得知,所需NaOH的质量为_______ 。
(5)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)。容量瓶用蒸馏洗涤后残留有少量的水_______ ;若定容时俯视刻度线______ 。

(1)写出下列仪器的名称:c.
(2)仪器a~e中,使用前必须检查是否漏水的有
(3)若利用装置分离四氯化碳和酒精的混合物,温度计水银球的位置在
(4)现需配制0.1mol/LNaOH溶液450mL,装置是某同学转移溶液的示意图。

①图中的错误是
②根据计算得知,所需NaOH的质量为
(5)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)。容量瓶用蒸馏洗涤后残留有少量的水
您最近一年使用:0次



