下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白(涉及表中元素一律用对应化学符号表示):
(1)在这些元素中,化学性质最不活泼的是:_____________ (填具体元素符号,下同),原子结构示意图为_____________ 。元素⑩名称为_____________ ,在周期表中的位置_________________ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是_________________ ,碱性最强的化合物的电子式是:_________________________ 。
(3)用电子式表示元素②的常见单质_____________ 其结构式为_________________ 。
(4)表示①与⑦的化合物的电子式为_________________ ,该化合物是由_____________ (填“极性”、“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的简单离子,离子半径由大到小的顺序是_________ 。
(6)元素③的简单氢化物的结构式为_____________________ ;该氢化物常温下和元素⑦的单质反应的化学方程式为 _____________________ 。
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)用电子式表示元素②的常见单质
(4)表示①与⑦的化合物的电子式为
(5)③、⑥、⑦三种元素形成的简单离子,离子半径由大到小的顺序是
(6)元素③的简单氢化物的结构式为
更新时间:2024-05-10 11:55:11
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】请同学们仔细阅读表中内容,并回答下列问题:
(1)写出①的元素符号:________ ;②的原子结构示意图:________ ;③的原子结构示意图:_________ ;④的周期:_______ ;⑤的族:________ 。
(2)甲元素最高价氧化物对应的水化物呈___________ 性(填“酸”或“碱”),乙元素最高价氧化物对应的水化物的化学式为___________ ,甲元素最高价氧化物对应的水化物与乙元素最高价氧化物对应的水化物相互反应的化学方程式为___________ 。
(3)甲与乙两元素的单质反应生成的化合物的电子式为___________ 。
(4)甲单质与丙的氢化物反应的化学方程式为______________ 。
元素 | 甲 | 乙 | 丙 |
元素符号 | ① | Cl | O |
原子结构示意图 |
| ② | ③ |
周期 | 三 | ④ | 二 |
族 | ⑤ | VIIA | VIA |
(2)甲元素最高价氧化物对应的水化物呈
(3)甲与乙两元素的单质反应生成的化合物的电子式为
(4)甲单质与丙的氢化物反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐2】KIO3是一种重要的无机化合物,可作为食盐中的补碘剂。回答下列问题:
(1)KIO3的化学名称是_______ 。
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:
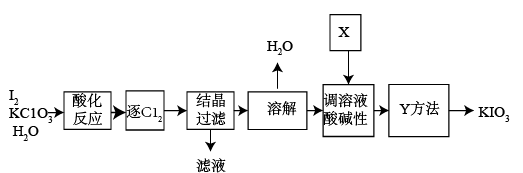
“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是_______ 。“滤液”中的溶质主要是_______ 。“调溶液酸碱性”中发生反应的化学方程式为_______ 。
(3)上述流程中X的电子式:_______ ,属于_______ 化合物(填“共价”或“离子”)。
(4)从溶液中获取KIO3固体的方法为:_______ 。
(1)KIO3的化学名称是
(2)利用“KClO3氧化法”制备KIO3工艺流程如下图所示:

“酸化反应”所得产物有KH(IO3)2、Cl2和KCl。“逐Cl2”采用的方法是
(3)上述流程中X的电子式:
(4)从溶液中获取KIO3固体的方法为:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】X、Y、Z均为短周期元素,X元素的气态氢化物的水溶液滴入无色酚酞变红,Y元素的最外层电子数是次外层电子数的2倍,Z元素是短周期元素中原子半径最大的元素(He、Ne、Ar除外)。
(1)写出X的元素符号____________ ,
(2)元素Y的最简单氢化物的电子式____________________ 。
(3)Z元素在元素周期表位置为_____________ ,
(4)X,Y,Z原子半径有小到大顺序为_______________
(1)写出X的元素符号
(2)元素Y的最简单氢化物的电子式
(3)Z元素在元素周期表位置为
(4)X,Y,Z原子半径有小到大顺序为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】随原子序数递增,八种短周期元素(用字母x等表示)原子半径的相对大小、最高正价或最低负价的变化如下图所示。
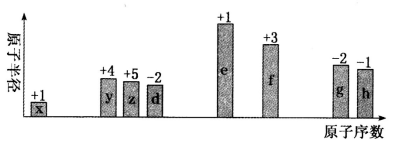
回答下列问题:
(1)用于文物年代测定的元素,其核素符号为_________ 。元素z在周期表中的位置是____________ 。
(2)元素d、e、f、g原子的简单离子半径由大到小的顺序为_________ (用离子符号表示)。
(3)元素f的单质与元素e的最高价氧化物对应的水化物反应的化学方程式为___________________ 。
(4)元素h单质的氧化性强于元素g单质的氧化性的事实是___________ (用离子方程式表示)。

回答下列问题:
(1)用于文物年代测定的元素,其核素符号为
(2)元素d、e、f、g原子的简单离子半径由大到小的顺序为
(3)元素f的单质与元素e的最高价氧化物对应的水化物反应的化学方程式为
(4)元素h单质的氧化性强于元素g单质的氧化性的事实是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下表为元素周期表的一部分,请回答有关问题:
(1)⑤和⑧的元素符号分别是_______ 和_______ 。
(2)表中最活泼的金属是_______ ,非金属性最强的元素是_______ (填写元素符号)。
(3)表中能形成两性氢氧化物的元素是_______ ,分别写出该元素的氢氧化物与⑥最高价氧化物的水化物反应的化学方程式:_______ 。
(4)请设计一个实验,比较⑦⑩单质氧化性的强弱:_______ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(2)表中最活泼的金属是
(3)表中能形成两性氢氧化物的元素是
(4)请设计一个实验,比较⑦⑩单质氧化性的强弱:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位、构、性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
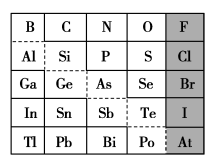
(1)Sn的最高化合价为____ ,Cl的最高价氧化物对应的水化物的化学式为____ ,Bi的最高价氧化物为____ 。
(2)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是____ 元素(填元素符号)。
②酸性:H3AsO4____ (填“>”“<”或“=”,下同)H2SeO4。
③氢化物的还原性:H2O____ H2S。
(3)从下列试剂中选择最佳试剂组合,比较C、Si的非金属性强弱:____ 。(可供选择的药品有CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液)

(1)Sn的最高化合价为
(2)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是
②酸性:H3AsO4
③氢化物的还原性:H2O
(3)从下列试剂中选择最佳试剂组合,比较C、Si的非金属性强弱:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐1】氟化镁( )晶体广泛应用在光学、冶金、国防、医疗等领域。
)晶体广泛应用在光学、冶金、国防、医疗等领域。
(1)镁元素位于元素周期表_______ 区(填“s”“p”“d或“ds”)。
(2) 晶胞示意图中:a.○表示
晶胞示意图中:a.○表示_______ (填离子符号)。b.离子半径: 结合离子结构示意图解释原因:
结合离子结构示意图解释原因:______________ 。
(3)已知 晶胞体积为
晶胞体积为 啊伏伽德罗常数的值为
啊伏伽德罗常数的值为 ,则其晶体密度=
,则其晶体密度=_______  (用代数式表示)。
(用代数式表示)。
Ⅱ.一种由 制备
制备 的工艺流程如下
的工艺流程如下
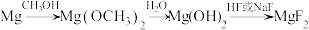
已知:i.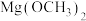 易溶于甲醇;
易溶于甲醇;
ii. ,
,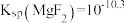 ,
,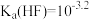
(4)上述流程中,可循环利用的物质是_______ 。
(5)比较相同条件下化学反应速率的大小:① 与
与 ;②
;② 与
与 。
。
a.小组同学预测化学反应速率:①<②,理由是甲基为_______ 基团,导致 键极性:
键极性: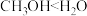 。
。
b.实验表明化学反应速率:①>②,分析其原因可能是:______________ 。
(6)上述流程中 开始转化为
开始转化为 所需氟化物的浓度:
所需氟化物的浓度: 。结合沉淀溶解平衡分析原因:
。结合沉淀溶解平衡分析原因:__________ 。
 )晶体广泛应用在光学、冶金、国防、医疗等领域。
)晶体广泛应用在光学、冶金、国防、医疗等领域。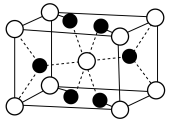
(1)镁元素位于元素周期表
(2)
 晶胞示意图中:a.○表示
晶胞示意图中:a.○表示 结合离子结构示意图解释原因:
结合离子结构示意图解释原因:(3)已知
 晶胞体积为
晶胞体积为 啊伏伽德罗常数的值为
啊伏伽德罗常数的值为 ,则其晶体密度=
,则其晶体密度= (用代数式表示)。
(用代数式表示)。Ⅱ.一种由
 制备
制备 的工艺流程如下
的工艺流程如下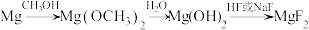
已知:i.
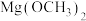 易溶于甲醇;
易溶于甲醇;ii.
 ,
,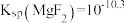 ,
,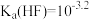
(4)上述流程中,可循环利用的物质是
(5)比较相同条件下化学反应速率的大小:①
 与
与 ;②
;② 与
与 。
。a.小组同学预测化学反应速率:①<②,理由是甲基为
 键极性:
键极性: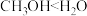 。
。b.实验表明化学反应速率:①>②,分析其原因可能是:
(6)上述流程中
 开始转化为
开始转化为 所需氟化物的浓度:
所需氟化物的浓度: 。结合沉淀溶解平衡分析原因:
。结合沉淀溶解平衡分析原因:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】现有A、B、C、D四种短周期元素,A元素形成的-2价阴离子比氦原子的核外电子数多8个,B元素与A元素可组成一种化合物E,为淡黄色固体,该固体遇到潮湿的空气能生成A的单质;A、C元素原子最外层电子数相同;D元素原子的M层上有7个电子。
(1)写出D元素在周期表中的位置_______ 。
(2)A、C两种元素的简单气态氢化物的稳定性由强到弱为_______ 。(用化学式表示)
(3)写出淡黄色固体E的电子式_______ 。
(4)A2和A3互为_______ 。(填字母代号)
A.同位素 B.同素异形体
(5)B、C、D三种元素的简单离子半径从大到小的顺序是_______ 。(用离子符号表示)
(6)D的单质与B的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(1)写出D元素在周期表中的位置
(2)A、C两种元素的简单气态氢化物的稳定性由强到弱为
(3)写出淡黄色固体E的电子式
(4)A2和A3互为
A.同位素 B.同素异形体
(5)B、C、D三种元素的简单离子半径从大到小的顺序是
(6)D的单质与B的最高价氧化物对应的水化物反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】已知下列9种元素在周期表中的位置,请回答下列问题。
(1)9种元素中化学性质最不活泼的是_______ ,金属性最强是_______ 。(填元素符号)
(2)A、B、C、D、G的简单离子中半径最大的是_______ (填离子符号)。
(3)D单质与B元素的最高价氧化物对应的水化物反应的离子方程式是________ 。
(4)A与F形成的一种化合物可作供氧剂,写出该化合物与二氧化碳反应的化学方程式:_______ 。
(5)B与F按原子个数比为1:1形成的化合物中含有的化学键类型是_______ 。(填“离子键”、“极性键”、“非极性键”)
(6)用电子式表示C与G形成化合物的过程_______ 。
(7)能说明元素G非金属性比H非金属性强的实验事实是_______ (离子方程式表示)
(8)能说明元素C金属性比D金属性强的实验事实是________ (填字母序号)
a.与Cl2反应时,C失去的电子数少即达到稳定结构
b.单质与H+反应时,C比D现象更剧烈
c.最高价氧化物对应的水化物的溶解能力:C>D
| 周期 | 主族和0族 | |||||||
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H | ||||||
(2)A、B、C、D、G的简单离子中半径最大的是
(3)D单质与B元素的最高价氧化物对应的水化物反应的离子方程式是
(4)A与F形成的一种化合物可作供氧剂,写出该化合物与二氧化碳反应的化学方程式:
(5)B与F按原子个数比为1:1形成的化合物中含有的化学键类型是
(6)用电子式表示C与G形成化合物的过程
(7)能说明元素G非金属性比H非金属性强的实验事实是
(8)能说明元素C金属性比D金属性强的实验事实是
a.与Cl2反应时,C失去的电子数少即达到稳定结构
b.单质与H+反应时,C比D现象更剧烈
c.最高价氧化物对应的水化物的溶解能力:C>D
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】根据元素在周期表中的位置能推测元素的原子结构以及相关物质的性质,下图是元素周期表的一部分,请根据图中字母所示元素的位置回答问题。
(1)元素P的原子结构示意图为________ ;元素 的最高价氧化物的电子式为
的最高价氧化物的电子式为________ 。
(2)元素 、
、 、
、 形成的简单离子中,半径由大到小的顺序为
形成的简单离子中,半径由大到小的顺序为_______ (填离子符号)。
(3)下列说法中,正确的有________ (填序号)。
①元素 的单质有多种同素异形体 ②
的单质有多种同素异形体 ②  中仅含离子键,
中仅含离子键,  中仅含共价键
中仅含共价键
③ 和
和  都是离子化合物 ④
都是离子化合物 ④ 比
比  的沸点更高
的沸点更高
(4)已知 离子的核内有
离子的核内有 个中子,
个中子, 的质量数为
的质量数为 ,则
,则 离子里含有电子的物质的量为
离子里含有电子的物质的量为_____  。
。
X | |||||||||||||||||
Y | Z | ||||||||||||||||
M | N | W | T | ||||||||||||||
P |
(1)元素P的原子结构示意图为
 的最高价氧化物的电子式为
的最高价氧化物的电子式为(2)元素
 、
、 、
、 形成的简单离子中,半径由大到小的顺序为
形成的简单离子中,半径由大到小的顺序为(3)下列说法中,正确的有
①元素
 的单质有多种同素异形体 ②
的单质有多种同素异形体 ②  中仅含离子键,
中仅含离子键,  中仅含共价键
中仅含共价键③
 和
和  都是离子化合物 ④
都是离子化合物 ④ 比
比  的沸点更高
的沸点更高(4)已知
 离子的核内有
离子的核内有 个中子,
个中子, 的质量数为
的质量数为 ,则
,则 离子里含有电子的物质的量为
离子里含有电子的物质的量为 。
。
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】W、Q、X、Y、Z是原子序数依次增大的短周期主族元素,其最外层电子数之和为19,W只有一个电子层,Q与X、Y、Z位于不同周期,X、Y相邻,Y原子最外层电子数是Q原子内层电子数的2倍,仅由Z元素形成的固体在常温下为淡黄色。回答下列问题:
(1)Y在元素周期表中的位置为_______ 。
(2)最简单氢化物的沸点:Q_______ (填“>”、“<”或“=”)Z。
(3)写出X元素形成的单质与Q的最高价氧化物对应的水化物的稀溶液发生反应的离子方程式:_______ 。
(4)仅由W、Q、Z三种元素可形成化合物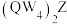 和
和 :
:
①化合物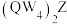 的名称为
的名称为_______ ,该化合物中Q元素的化合价为_______ 价。
②化合物 含有化学键的类型为
含有化学键的类型为_______ (填“离子键”、“共价键”或“离子键与共价键”)。
(5)化合物 与热水反应仅生成X的最高价氧化物对应的水化物和一种具有臭鸡蛋气味的气体,写出其化学方程式:
与热水反应仅生成X的最高价氧化物对应的水化物和一种具有臭鸡蛋气味的气体,写出其化学方程式:_______ 。
(6)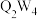 可用作火箭的燃料,1 mol
可用作火箭的燃料,1 mol 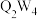 中所含的电子总数为
中所含的电子总数为_______  。
。
(1)Y在元素周期表中的位置为
(2)最简单氢化物的沸点:Q
(3)写出X元素形成的单质与Q的最高价氧化物对应的水化物的稀溶液发生反应的离子方程式:
(4)仅由W、Q、Z三种元素可形成化合物
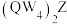 和
和 :
:①化合物
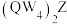 的名称为
的名称为②化合物
 含有化学键的类型为
含有化学键的类型为(5)化合物
 与热水反应仅生成X的最高价氧化物对应的水化物和一种具有臭鸡蛋气味的气体,写出其化学方程式:
与热水反应仅生成X的最高价氧化物对应的水化物和一种具有臭鸡蛋气味的气体,写出其化学方程式:(6)
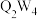 可用作火箭的燃料,1 mol
可用作火箭的燃料,1 mol 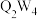 中所含的电子总数为
中所含的电子总数为 。
。
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】判断
(1)范德华力存在于任何物质中_____
(2)范德华力比化学键弱得多_____
(3)CH4、C2H6、C3H8的熔点、沸点依次升高_____
(4)HF、HCl、HBr、HI的稳定性依次减弱,是因为分子间作用力依次减弱_____
(5)卤素单质、卤素氢化物、卤素碳化物(即CX4)的熔、沸点均随着相对分子质量的增大而增大_____
(6)加热蒸发氯化钾水溶液的过程中有分子间作用力的破坏_____
(7)CO2溶于水和干冰升华都只有分子间作用力改变_____
(8)石墨转化为金刚石既有共价键的断裂和生成,也有分子间作用力的破坏_____
(1)范德华力存在于任何物质中
(2)范德华力比化学键弱得多
(3)CH4、C2H6、C3H8的熔点、沸点依次升高
(4)HF、HCl、HBr、HI的稳定性依次减弱,是因为分子间作用力依次减弱
(5)卤素单质、卤素氢化物、卤素碳化物(即CX4)的熔、沸点均随着相对分子质量的增大而增大
(6)加热蒸发氯化钾水溶液的过程中有分子间作用力的破坏
(7)CO2溶于水和干冰升华都只有分子间作用力改变
(8)石墨转化为金刚石既有共价键的断裂和生成,也有分子间作用力的破坏
您最近一年使用:0次