1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位、构、性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
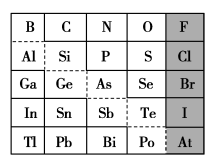
(1)Sn的最高化合价为____ ,Cl的最高价氧化物对应的水化物的化学式为____ ,Bi的最高价氧化物为____ 。
(2)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是____ 元素(填元素符号)。
②酸性:H3AsO4____ (填“>”“<”或“=”,下同)H2SeO4。
③氢化物的还原性:H2O____ H2S。
(3)从下列试剂中选择最佳试剂组合,比较C、Si的非金属性强弱:____ 。(可供选择的药品有CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液)

(1)Sn的最高化合价为
(2)根据元素周期律,推断:
①阴影部分元素简单气态氢化物热稳定性最强的是
②酸性:H3AsO4
③氢化物的还原性:H2O
(3)从下列试剂中选择最佳试剂组合,比较C、Si的非金属性强弱:
更新时间:2022-06-20 21:28:36
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】根据①~⑫元素的编号所在周期表中的位置,用相应的元素符号或者化学用语回答有关问题:
(1)能显 价,还能显
价,还能显 价的元素是
价的元素是___________ 。
(2)最难形成化合物的元素是___________ 。
(3)单质具有半导体性质的元素是___________ 。
(4)元素⑫的最高价氧化物对应水化物的分子式为___________ ;
(5)元素①与⑥形成的18电子的化合物为___________ ;
(6)最新发现的一种单质是由60个原子组成球状结构的分子。这种单质叫足球烯,它是由___________ 元素组成的。
(7)第三周期某元素氢化物(组成为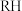 )能和冷水剧烈反应产生氢气,该反应的化学方程式为
)能和冷水剧烈反应产生氢气,该反应的化学方程式为___________ 。
(8)元素⑨的单质与⑧的最高价氧化物对应水化物反应的化学方程式___________ ;
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 3 | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
 价,还能显
价,还能显 价的元素是
价的元素是(2)最难形成化合物的元素是
(3)单质具有半导体性质的元素是
(4)元素⑫的最高价氧化物对应水化物的分子式为
(5)元素①与⑥形成的18电子的化合物为
(6)最新发现的一种单质是由60个原子组成球状结构的分子。这种单质叫足球烯,它是由
(7)第三周期某元素氢化物(组成为
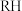 )能和冷水剧烈反应产生氢气,该反应的化学方程式为
)能和冷水剧烈反应产生氢气,该反应的化学方程式为(8)元素⑨的单质与⑧的最高价氧化物对应水化物反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下图是元素周期表的一部分,根据① ~ ⑨在周期表中的位置按题目要求回答:
(1)在元素①~⑨中,金属性最强的元素是__ (填元素符号)。
(2)①、②、③三种元素的原子半径由大到小的顺序是________ (填元素符号)。
(3)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较强的是____ (填化学式)。
(4)元素④的简单氢化物比元素⑧的简单氢化物的稳定性_____ (填“强”或“弱”)。
(5)⑥、⑦、⑨三种元素的常见离子的半径最小的是_______ (用化学式表示)。
(6)元素②和元素④形成的一种化合物在大气中的含量过高时会产生温室效应,写出该化合物的电子式_______ 。
(7)⑤和⑦两种元素的最高价氧化物对应的水化物之间发生反应的离子方程式为____ 。
| 族 周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(2)①、②、③三种元素的原子半径由大到小的顺序是
(3)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较强的是
(4)元素④的简单氢化物比元素⑧的简单氢化物的稳定性
(5)⑥、⑦、⑨三种元素的常见离子的半径最小的是
(6)元素②和元素④形成的一种化合物在大气中的含量过高时会产生温室效应,写出该化合物的电子式
(7)⑤和⑦两种元素的最高价氧化物对应的水化物之间发生反应的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐3】某研究性学习小组设计实验探究元素周期律,如图所示。

(1)仪器a的名称是____________ ,加入的药品为稀硝酸;仪器b的名称是____________ ,加入的药品为碳酸钠固体;b中反应现象为___________ ,验证氮的非金属性比碳的___ (填“强”或“弱”)。
(2)c中装有硅酸钠溶液,c中反应现象为____ ,验证硅的非金属性比碳的___ (填“强”或“弱”)。
(3)结论:同一周期从左到右元素非金属性逐渐____ (填“增强”或“减弱”);同一主族从上到下元素非金属性逐渐_______ (填“增强”或“减弱”)。
(4)某同学考虑到稀硝酸的挥发,则应在装置b和c之间增加一个盛有_______ 试剂的洗气瓶。

(1)仪器a的名称是
(2)c中装有硅酸钠溶液,c中反应现象为
(3)结论:同一周期从左到右元素非金属性逐渐
(4)某同学考虑到稀硝酸的挥发,则应在装置b和c之间增加一个盛有
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】以粗硅(含铁、铝等杂质)为原料,工业上有以下两种制备高纯硅的工艺。已知: 沸点57.7℃,遇水强烈水解;
沸点57.7℃,遇水强烈水解; 沸点31.5℃,且能与
沸点31.5℃,且能与 强烈反应,并在空气中易自燃。
强烈反应,并在空气中易自燃。
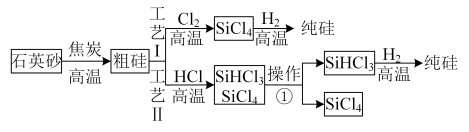
(1)写出制备粗硅的化学反应方程式为_______ 。
(2)粗硅与HCl反应完全后,经冷凝得到的 中含有少量
中含有少量 ,操作①采用的方法为
,操作①采用的方法为_______ 。
(3)实验室用如下装置制备 (反应温度在400℃~500℃)。
(反应温度在400℃~500℃)。
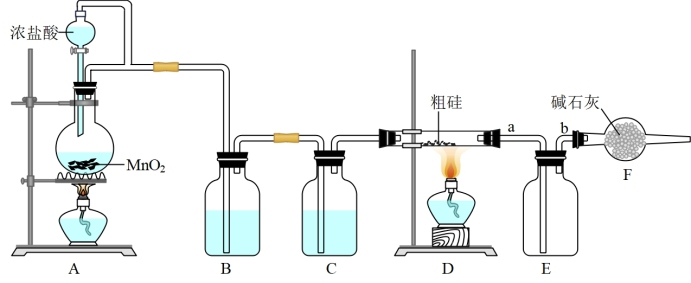
①装置F的作用是_______ 。实验开始应先点燃_______ (填“A”或“D”)装置的酒精灯一段时间后再点燃另一酒精灯。
②写出A装置中发生反应的离子方程式_______ 。
(4)根据如图所示装置回答以下问题:
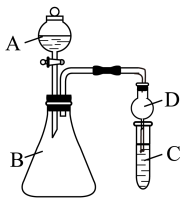
若要用此装置证明非金属性:C>Si,从以下所给物质中选出甲同学设计的实验所用到的物质:①稀盐酸②稀硫酸③碳酸钙④ 溶液⑤碳酸钠。试剂A为
溶液⑤碳酸钠。试剂A为_______ ,试剂C为_______ (填序号)。
 沸点57.7℃,遇水强烈水解;
沸点57.7℃,遇水强烈水解; 沸点31.5℃,且能与
沸点31.5℃,且能与 强烈反应,并在空气中易自燃。
强烈反应,并在空气中易自燃。
(1)写出制备粗硅的化学反应方程式为
(2)粗硅与HCl反应完全后,经冷凝得到的
 中含有少量
中含有少量 ,操作①采用的方法为
,操作①采用的方法为(3)实验室用如下装置制备
 (反应温度在400℃~500℃)。
(反应温度在400℃~500℃)。
①装置F的作用是
②写出A装置中发生反应的离子方程式
(4)根据如图所示装置回答以下问题:

若要用此装置证明非金属性:C>Si,从以下所给物质中选出甲同学设计的实验所用到的物质:①稀盐酸②稀硫酸③碳酸钙④
 溶液⑤碳酸钠。试剂A为
溶液⑤碳酸钠。试剂A为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】已知X、Y、Z、W、Q、P是短周期的主族元素。如图所示,横坐标表示原子半径相对大小,纵坐标表示化合价(最高正价或最低负价)。回答下列问题:

(1)Y在元素周期表中的位置_______ ;Y的单质化学性质稳定,原因是_______ 。
(2)Q的单质与P的最高价氧化物的水化物发生反应的离子方程式为_______ 。
(3)用电子式表示化合物PZ的形成过程_______ 。
(4)将PX投入水中,可得到X的单质,该反应的化学方程式为_______ 。
(5)Z与W相比较,非金属性较强的是_______ (填元素符号),设计实验证明_______ 。

(1)Y在元素周期表中的位置
(2)Q的单质与P的最高价氧化物的水化物发生反应的离子方程式为
(3)用电子式表示化合物PZ的形成过程
(4)将PX投入水中,可得到X的单质,该反应的化学方程式为
(5)Z与W相比较,非金属性较强的是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐1】利用如所示装置可以验证元素的非金属性的变化规律。
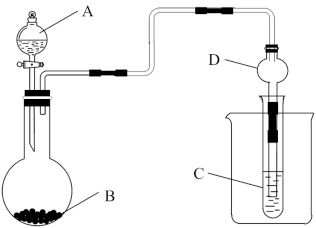
(1)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验,验证氯的非金属性强于硫的非金属性。装置A、B、C中所装药品分别为_______ 、_______ 、_______ ,装置C中的实验现象为有淡黄色沉淀生成,则反应的离子方程式为_______ 。
(2)若要证明非金属性C>Si,则A中应加入_______ 溶液,B中应加入Na2CO3,装置C中发生的化学反应方程式为_______ 。

(1)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验,验证氯的非金属性强于硫的非金属性。装置A、B、C中所装药品分别为
(2)若要证明非金属性C>Si,则A中应加入
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用图装置完成了氧元素的非金属性比硫元素强的实验研究。回答下列问题:
(1)图中A的仪器名称是______________ ,D的作用是__________ 。
(2)N、C、Si的非金属性由强到弱的顺序是:____________________ ;从以下所给物质中选出甲同学设计的实验所用到物质:
A中试剂为_________ ,试剂C为__________ (填序号)。
①稀HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2
(3)①乙同学设计的实验所用到试剂A为_______ ;试剂B为________ ;试剂C为________ 。
②写出C中发生反应的化学方程式_________________________ 。
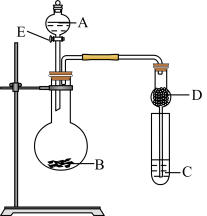
(1)图中A的仪器名称是
(2)N、C、Si的非金属性由强到弱的顺序是:
A中试剂为
①稀HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2
(3)①乙同学设计的实验所用到试剂A为
②写出C中发生反应的化学方程式

您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐3】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验:
Ⅰ.探究同周期元素性质的递变规律
(1)相同条件下,将钠、镁、铝各1 mol分别投入到足量的同浓度的稀盐酸中,试预测实验结果:_______ 与稀盐酸反应最剧烈;______ 与稀盐酸反应产生的气体最多。
(2)向Na2SiO3溶液中加入稀H2SO4出现白色沉淀,可证明S的非金属性比Si强,反应的离子方程式为_____________________________ 。
Ⅱ.探究同主族元素非金属性的递变规律
某研究性学习小组设计了一组实验来探究ⅦA族元素原子的得电子能力强弱规律。下图中A、B、C是三个可供选择制取氯气的装置,装置D的玻璃管中①、②处依次放置蘸有NaBr溶液、NaOH浓溶液的棉球。

(3)写出装置B中仪器a的名称________________ 。
(4)实验室制取氯气还可采用如下原理:2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O,依据该反应原理选择_____________ (填“A”或“B”或“C”)装置制取氯气。
(5)反应装置的导气管连接装置D的X导管,①处发生反应的离子方程式为________________________ ;
Ⅰ.探究同周期元素性质的递变规律
(1)相同条件下,将钠、镁、铝各1 mol分别投入到足量的同浓度的稀盐酸中,试预测实验结果:
(2)向Na2SiO3溶液中加入稀H2SO4出现白色沉淀,可证明S的非金属性比Si强,反应的离子方程式为
Ⅱ.探究同主族元素非金属性的递变规律
某研究性学习小组设计了一组实验来探究ⅦA族元素原子的得电子能力强弱规律。下图中A、B、C是三个可供选择制取氯气的装置,装置D的玻璃管中①、②处依次放置蘸有NaBr溶液、NaOH浓溶液的棉球。

(3)写出装置B中仪器a的名称
(4)实验室制取氯气还可采用如下原理:2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O,依据该反应原理选择
(5)反应装置的导气管连接装置D的X导管,①处发生反应的离子方程式为
您最近一年使用:0次
【推荐1】 NOx是汽车尾气中的主要污染物,在汽车尾气系统中装配催化转化器,可有效降低NOx的排放。
(1)当尾气中空气不足时,NOx (以NO为主)在催化转化器中被CO还原成 排出。
排出。
①基态碳原子中,电子占据最高能级的电子云轮廓图的形状是___________
②氧的基态原子的轨道表示式为___________
③C、N、O电负性由大到小顺序为___________
(2)当尾气中空气过量时,催化转化器中的金属氧化物吸收NOx生成盐。其吸收能力顺序如下: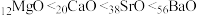
已知:镁、钙、锶、钡的部分电离能数据如下表所示。
①推测Sr的第三电离能a的范围:___________
②MgO、CaO、SrO、BaO对NOx的吸收能力增强,从原子结构角度解释原因:Mg、Ca、Sr、Ba为同主族元素,___________ ,元素的金属性逐渐增强,金属氧化物对NOx的吸收能力逐渐增强。
(3)研究 作为SCR脱硝催化剂的性能时发现:在
作为SCR脱硝催化剂的性能时发现:在 上适当掺杂不同的金属氧化物如
上适当掺杂不同的金属氧化物如 、
、 、
、 、NiO、CuO等有利于提高催化脱硝性能。
、NiO、CuO等有利于提高催化脱硝性能。
①基态V原子的核外价层电子排布式为___________
②若继续寻找使 催化性能更好的掺杂金属氧化物,可以在元素周期表
催化性能更好的掺杂金属氧化物,可以在元素周期表___________ 区寻找恰当元素
A.s B.p C.d D.ds
(1)当尾气中空气不足时,NOx (以NO为主)在催化转化器中被CO还原成
 排出。
排出。①基态碳原子中,电子占据最高能级的电子云轮廓图的形状是
②氧的基态原子的轨道表示式为
③C、N、O电负性由大到小顺序为
(2)当尾气中空气过量时,催化转化器中的金属氧化物吸收NOx生成盐。其吸收能力顺序如下:
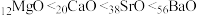
已知:镁、钙、锶、钡的部分电离能数据如下表所示。
| 元素 | Mg | Ca | Sr | Ba | |
电离能/( ) ) |  | 738 | 589.7 | 549 | 502.9 |
 | 1451 | 1145 | 1064 | 965.2 | |
 | 7733 | 4910 | a | 3600 | |
①推测Sr的第三电离能a的范围:
②MgO、CaO、SrO、BaO对NOx的吸收能力增强,从原子结构角度解释原因:Mg、Ca、Sr、Ba为同主族元素,
(3)研究
 作为SCR脱硝催化剂的性能时发现:在
作为SCR脱硝催化剂的性能时发现:在 上适当掺杂不同的金属氧化物如
上适当掺杂不同的金属氧化物如 、
、 、
、 、NiO、CuO等有利于提高催化脱硝性能。
、NiO、CuO等有利于提高催化脱硝性能。①基态V原子的核外价层电子排布式为
②若继续寻找使
 催化性能更好的掺杂金属氧化物,可以在元素周期表
催化性能更好的掺杂金属氧化物,可以在元素周期表A.s B.p C.d D.ds
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】有 、
、 、
、 、
、 、
、 、
、 六种短周期的主族元素,部分信息如下表所示:
六种短周期的主族元素,部分信息如下表所示:
请回答下列问题:
(1) 在元素周期表中的位置是
在元素周期表中的位置是___________ 。
(2) 的单质与
的单质与 的最高价氧化物对应水化物的水溶液反应的离子方程式为
的最高价氧化物对应水化物的水溶液反应的离子方程式为___________ 。
(3)Z、M、Q的简单离子的半径由小到大的顺序为___________ (用离子符号表示)。
(4)简单氢化物稳定性:M___________ R(填“>”或“<”)。
(5)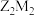 属于
属于___________ 化合物(填“离子”或“共价”),写出它的电子式:___________ 。
(6)写出一条能说明 的金属性比
的金属性比 强的依据:
强的依据:___________ 。
 、
、 、
、 、
、 、
、 、
、 六种短周期的主族元素,部分信息如下表所示:
六种短周期的主族元素,部分信息如下表所示:| 元素 |  |  |  |  |  |  |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.160 | ||
| 主要化合价 | +3 |  |  、 、 | |||
| 其它信息 | 某种核素无中子 | 氧化物具有两性 | 短周期主族元素中原子半径最大 | 次外层电子数是最外层电子数的4倍 |
(1)
 在元素周期表中的位置是
在元素周期表中的位置是(2)
 的单质与
的单质与 的最高价氧化物对应水化物的水溶液反应的离子方程式为
的最高价氧化物对应水化物的水溶液反应的离子方程式为(3)Z、M、Q的简单离子的半径由小到大的顺序为
(4)简单氢化物稳定性:M
(5)
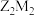 属于
属于(6)写出一条能说明
 的金属性比
的金属性比 强的依据:
强的依据:
您最近一年使用:0次


 。试回答:
。试回答:

