请同学们仔细阅读表中内容,并回答下列问题:
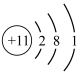
(1)写出①的元素符号:________ ;②的原子结构示意图:________ ;③的原子结构示意图:_________ ;④的周期:_______ ;⑤的族:________ 。
(2)甲元素最高价氧化物对应的水化物呈___________ 性(填“酸”或“碱”),乙元素最高价氧化物对应的水化物的化学式为___________ ,甲元素最高价氧化物对应的水化物与乙元素最高价氧化物对应的水化物相互反应的化学方程式为___________ 。
(3)甲与乙两元素的单质反应生成的化合物的电子式为___________ 。
(4)甲单质与丙的氢化物反应的化学方程式为______________ 。
元素 | 甲 | 乙 | 丙 |
元素符号 | ① | Cl | O |
原子结构示意图 |
| ② | ③ |
周期 | 三 | ④ | 二 |
族 | ⑤ | VIIA | VIA |
(2)甲元素最高价氧化物对应的水化物呈
(3)甲与乙两元素的单质反应生成的化合物的电子式为
(4)甲单质与丙的氢化物反应的化学方程式为
20-21高一上·全国·课时练习 查看更多[1]
(已下线)4.3 化学键(精练)-2020-2021学年上学期高一化学同步精品课堂(人教版必修第一册)
更新时间:2020-12-11 16:29:35
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】A、B、C是短周期元素中的三种相邻元素,A、B为同周期元素,B、C为同主族元素,A、B、C的核外电子数之和为31。请回答下列问题:
(1)A、B、C的元素名称分别为:_________ ,_________ ,________ ;
(2)写出由A元素组成单质的电子式_________ ,画出C离子的结构示意图:_________ ;
(3)用电子式表示C的氢化物的形成过程___________________________________ 。
(1)A、B、C的元素名称分别为:
(2)写出由A元素组成单质的电子式
(3)用电子式表示C的氢化物的形成过程
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
(1)③的原子结构示意图为_______ ;
(2)元素①~⑧中金属性最强的是_______ (填元素符号);
(3)元素①~⑧中最高价氧化物对应的水化物酸性最强的是_______ (填化学式);
(4)⑤、⑥元素的金属性强弱依次_______ (填“增大”“减少”或“不变”)。
| 周期 | 族 | |||||||
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)元素①~⑧中金属性最强的是
(3)元素①~⑧中最高价氧化物对应的水化物酸性最强的是
(4)⑤、⑥元素的金属性强弱依次
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】A、B、C、D均为中学化学常见的纯净物,A是太阳能电池用的光伏材料。C、D为钠盐,两种物质中除钠、氧外的元素最外层都为4个电子。它们之间有如下的反应关系:

(1)画出A原子结构示意图______________________________ 。
(2)写出B物质的一种用途______________________________ 。
(3)D物质的俗名是________________________ 。
(4)写出反应②的化学方程式__________________________________________ 。

(1)画出A原子结构示意图
(2)写出B物质的一种用途
(3)D物质的俗名是
(4)写出反应②的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】元素周期表的形式多种多样,扇形元素周期表的一部分(1~36号元素)如图所示,对比中学常见的元素周期表,思考扇形元素周期表的填充规律。请用准确的化学符号和用语 回答下列问题:

(1)元素1在元素周期表中的位置_______ 。
(2)比较f、o、k简单离子的半径,由大到小的顺序是_______ (用离子符号表示)。
(3)b与e组成的化合物中,含有非极性共价键的化合物的电子式_______ 。
(4)i的最高价氧化物对应水化物的化学式_______ ,比较i、d最简单氢化物的稳定性_______ (用化学式表示)。
(5)比较m、f、g的金属性强弱,由强到弱的顺序是_______ (用元素符号表示)
(6)比较j和h的非金属性强弱,设计简单的实验方案_______ 。

(1)元素1在元素周期表中的位置
(2)比较f、o、k简单离子的半径,由大到小的顺序是
(3)b与e组成的化合物中,含有非极性共价键的化合物的电子式
(4)i的最高价氧化物对应水化物的化学式
(5)比较m、f、g的金属性强弱,由强到弱的顺序是
(6)比较j和h的非金属性强弱,设计简单的实验方案
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
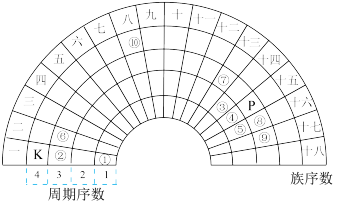
【推荐2】元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1~36号元素)。
(1)氧在该元素周期表 中的位置是___________ 。
(2)②⑤可形成含共价键的离子化合物,该化合物中阴阳离子个数比为___________ 。
(3)⑦的最高价氧化物与②的最高价氧化物对应的水化物反应的离子方程式___________ 。
(4)下列说法不正确 的是___________。
(5)某化合物由⑥和⑨组成,用电子式表示其形成的过程___________ 。
(1)氧在
(2)②⑤可形成含共价键的离子化合物,该化合物中阴阳离子个数比为
(3)⑦的最高价氧化物与②的最高价氧化物对应的水化物反应的离子方程式
(4)下列说法
| A.第3周期共有18种元素 |
| B.元素⑩是人体必需的微量元素 |
| C.②对应的简单离子半径在同周期元素的简单离子中最小 |
| D.①分别与③、④、⑤形成的10电子化合物中热稳定性最好的是①⑤形成的化合物 |
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐3】减少交通事故除遵守交通法规和正确驾驶外,被动安全措施也极为重要,汽车的安全气囊内有叠氮化钠(NaN3)与硝酸铵(NH4NO3)等物质。当汽车在高速行驶中受到猛烈撞击时,这些物质会迅速发生反应,产生大量气体,充满气囊,从而保护驾乘人员安全。
(1)下列判断正确的是_____________ 。
A.道路起雾与H2O分子中化学键断裂相关
B.NH4NO3中只含有极性共价键
C.NaN3受到猛烈撞击与NH4NO3发生反应时化学键一定断裂
D.NaN3、NH4NO3均属于离子化合物
(2)叠氮化钠是一种无色晶体,广泛用于汽车安全气囊及化工合成等。常见的两种制备方法:2NaNH2+N2O=NaN3+NaOH+NH3;3NaNH2+NaNO3=NaN3+3NaOH+NH3↑。
①写出NaNH2的电子式:_____________ 。
②NaOH固体中含有的化学键类型有_____________ 。
(3)已知X、Y、Z、W是四种短周期元素,且原子序数依次增大。W原子的质子数等于Y、Z原子的最外层电子数之和。Y与X形成的分子中有3个共价键,X、Y、Z形成的常见化合物是汽车安全气囊中的一种填充物。请回答下列问题:
①由以上元素两两形成的化合物中,溶于水显碱性的气态氢化物的电子式为_____________ ,其所含的化学键属于_____________ ;含有极性共价键和非极性共价键的化合物的电子式为_____________ 。
②由X、Y、Z形成的常见化合物与W的最高价氧化物对应的水化物的固体加热形成两种氢化物的反应过程中,反应物化学键断裂的类型有_____________ 。
(1)下列判断正确的是
A.道路起雾与H2O分子中化学键断裂相关
B.NH4NO3中只含有极性共价键
C.NaN3受到猛烈撞击与NH4NO3发生反应时化学键一定断裂
D.NaN3、NH4NO3均属于离子化合物
(2)叠氮化钠是一种无色晶体,广泛用于汽车安全气囊及化工合成等。常见的两种制备方法:2NaNH2+N2O=NaN3+NaOH+NH3;3NaNH2+NaNO3=NaN3+3NaOH+NH3↑。
①写出NaNH2的电子式:
②NaOH固体中含有的化学键类型有
(3)已知X、Y、Z、W是四种短周期元素,且原子序数依次增大。W原子的质子数等于Y、Z原子的最外层电子数之和。Y与X形成的分子中有3个共价键,X、Y、Z形成的常见化合物是汽车安全气囊中的一种填充物。请回答下列问题:
①由以上元素两两形成的化合物中,溶于水显碱性的气态氢化物的电子式为
②由X、Y、Z形成的常见化合物与W的最高价氧化物对应的水化物的固体加热形成两种氢化物的反应过程中,反应物化学键断裂的类型有
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表是元素周期表
(1)在上述周期表用元素符号标出铁元素所在的位置______ 。
(2)表中最活泼的金属是______ ,非金属性最强的元素是______ 。(填写元素符号)
(3)⑤的元素符号是______ ,⑤ 形成的单质是_________ 晶体。
(4)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱:___________ 。
| ① | ② | ||||||||||||||||
| ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||||||||||||
| ⑨ | ⑩ | ||||||||||||||||
(1)在上述周期表用元素符号标出铁元素所在的位置
(2)表中最活泼的金属是
(3)⑤的元素符号是
(4)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是周期表中的一部分,根据a—g在周期表中的位置,用元素符号或化学式回答下列问题:
(1)e的元素符号为____________ ;
(2)b、c、d三种元素的非金属性逐渐_______________ (填“减弱”或“增强”);
(3)a元素与f元素形成的化合物的电子式为_________________ ;
(4)最高价氧化物的水化物碱性最强的是__________ ,酸性最强的是__________ ,呈两性的是__________ ;
 族 族周期 | ⅠA | 0 | ||||||
| 1 | a | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | b | c | d | |||||
| 3 | e | g | f | |||||
(2)b、c、d三种元素的非金属性逐渐
(3)a元素与f元素形成的化合物的电子式为
(4)最高价氧化物的水化物碱性最强的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】下表为元素周期表的一部分,请回答有关问题:
(1)⑤和⑧的元素符号分别是______ 和______ 。(填写元素符号)
(2)表中最活泼的金属是______ ,非金属性最强的元素是______ (填写元素符号)
(3)表中能形成两性氢氧化物的元素是______ (填写元素符号),分别写出该元素的氢氧化物与⑥和⑨最高价氧化物的水化物反应的化学方程式:______ ,______ 。
(4)请设计一个实验,比较⑦⑩单质氧化性的强弱:______ 。
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
4 | ⑨ | ⑩ |
(2)表中最活泼的金属是
(3)表中能形成两性氢氧化物的元素是
(4)请设计一个实验,比较⑦⑩单质氧化性的强弱:
您最近一年使用:0次