根据元素在周期表中的位置能推测元素的原子结构以及相关物质的性质,下图是元素周期表的一部分,请根据图中字母所示元素的位置回答问题。
(1)元素P的原子结构示意图为________ ;元素 的最高价氧化物的电子式为
的最高价氧化物的电子式为________ 。
(2)元素 、
、 、
、 形成的简单离子中,半径由大到小的顺序为
形成的简单离子中,半径由大到小的顺序为_______ (填离子符号)。
(3)下列说法中,正确的有________ (填序号)。
①元素 的单质有多种同素异形体 ②
的单质有多种同素异形体 ②  中仅含离子键,
中仅含离子键,  中仅含共价键
中仅含共价键
③ 和
和  都是离子化合物 ④
都是离子化合物 ④ 比
比  的沸点更高
的沸点更高
(4)已知 离子的核内有
离子的核内有 个中子,
个中子, 的质量数为
的质量数为 ,则
,则 离子里含有电子的物质的量为
离子里含有电子的物质的量为_____  。
。
X | |||||||||||||||||
Y | Z | ||||||||||||||||
M | N | W | T | ||||||||||||||
P |
(1)元素P的原子结构示意图为
 的最高价氧化物的电子式为
的最高价氧化物的电子式为(2)元素
 、
、 、
、 形成的简单离子中,半径由大到小的顺序为
形成的简单离子中,半径由大到小的顺序为(3)下列说法中,正确的有
①元素
 的单质有多种同素异形体 ②
的单质有多种同素异形体 ②  中仅含离子键,
中仅含离子键,  中仅含共价键
中仅含共价键③
 和
和  都是离子化合物 ④
都是离子化合物 ④ 比
比  的沸点更高
的沸点更高(4)已知
 离子的核内有
离子的核内有 个中子,
个中子, 的质量数为
的质量数为 ,则
,则 离子里含有电子的物质的量为
离子里含有电子的物质的量为 。
。
更新时间:2020-07-29 09:05:10
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】学习了元素周期律可以把元素化合物知识系统地归纳起来,可以从物质的类别和元素的化合价两个方面在二维空间构造知识体系。例如:

请回答下列问题:
(1)S在周期表中的位置是_______ ;Y的化学式为_______ 。
(2)用电子式表示图中X的形成过程:_______ ;X的水溶液长期在空气中放置容易变浑浊,该变化可说明:S的非金属性比O_______ (填“强或“弱”),用原子结构解释原因为:同主族元素原子的最外层电子数相同,从上到下,_______ ,得电子能力逐渐减弱。
(3)SO2是常见的大气污染物之一,同时也是重要的工业原料。实验室中常把SO2通入_______ 中,通过观察是否褪色检验SO2是否存在;SO2也可以使酸性高锰酸钾溶液褪色,二者褪色原理_______ (填“相同”或“不同”)。
(4)比较H2SO4和Na2SO4的熔点高低,并从微粒间相互作用(化学键、分子间作用力)的角度说出理由_______ 。情况下会生成(间二硝基苯)

请回答下列问题:
(1)S在周期表中的位置是
(2)用电子式表示图中X的形成过程:
(3)SO2是常见的大气污染物之一,同时也是重要的工业原料。实验室中常把SO2通入
(4)比较H2SO4和Na2SO4的熔点高低,并从微粒间相互作用(化学键、分子间作用力)的角度说出理由
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】如图所示为元素周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中属于d区的元素是________ (填编号);④⑤⑥⑦⑧五种元素形成的稳定离子中,离子半径最小的是________ (填离子符号)。
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子的空间结构为________ 。
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与 溶液反应的化学方程式:
溶液反应的化学方程式:________ 。
(4)上述10种元素形成的最高价氧化物对应水化物中,酸性最强的是________ (填化学式)。
(5)下列各组微粒的空间结构相同的是________ (填序号)。
① 和
和 ②
② 和
和 ③
③ 和
和 ④
④ 和
和 ⑤
⑤ 和
和 ⑥
⑥ 、
、 和
和
(6)有两种活性反应中间体粒子,它们的粒子中均含有元素③的1个原子和元素①的3个原子。请依据下面给出的这两种粒子的球棍模型,写出相应的化学式:
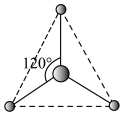
________________ ;
________________ 。

请回答下列问题:
(1)表中属于d区的元素是
(2)表中元素①的6个原子与元素③的6个原子形成的某种环状分子的空间结构为
(3)某些不同族元素的性质也有一定的相似性,如上表中元素⑤与元素②的氢氧化物有相似的性质。请写出元素②的氢氧化物与
 溶液反应的化学方程式:
溶液反应的化学方程式:(4)上述10种元素形成的最高价氧化物对应水化物中,酸性最强的是
(5)下列各组微粒的空间结构相同的是
①
 和
和 ②
② 和
和 ③
③ 和
和 ④
④ 和
和 ⑤
⑤ 和
和 ⑥
⑥ 、
、 和
和
(6)有两种活性反应中间体粒子,它们的粒子中均含有元素③的1个原子和元素①的3个原子。请依据下面给出的这两种粒子的球棍模型,写出相应的化学式:


您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】如表列出了9种元素在元素周期表(元素周期表中给出部分)中的位置。
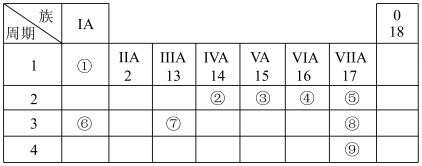
请回答下列问题:
(1)考古工作者利用某元素的一种核素测定一些文物的年代,这种核素的符号是_______ 。
(2)画出元素⑧形成的简单离子的结构示意图:_______ 。
(3)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物反应的离子方程式为_______ 。
(4)元素②③④⑤⑧⑨与元素①形成的最简单化合物中稳定性最强的是_______ (填化学式)。
(5)元素⑦和⑧形成化合物的化学键类型为_______ 。
(6)用电子式表示元素⑥和⑨形成化合物的过程_______ 。

请回答下列问题:
(1)考古工作者利用某元素的一种核素测定一些文物的年代,这种核素的符号是
(2)画出元素⑧形成的简单离子的结构示意图:
(3)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物反应的离子方程式为
(4)元素②③④⑤⑧⑨与元素①形成的最简单化合物中稳定性最强的是
(5)元素⑦和⑧形成化合物的化学键类型为
(6)用电子式表示元素⑥和⑨形成化合物的过程
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】元素A、B、C、D的离子核外都有10个电子,A的氯化物中,电子总数为28,A和B的化合物A2B中共有30个电子,B与C的化合物为C2B3型;C与D的化合物为CD3型。试根据有关元素的化合物的构成确定其化合物的化学式:
ACl:________ ;A2B:________ ;C2B3:________ ;CD3:________ 。
ACl:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】在庆祝中华人民共和国成立70周年的阅兵仪式上,最后亮相的DF-31A洲际战略导弹是我国大国地位、国防实力的显著标志.其制作材料中包含了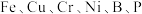 等多种元素.回答下列问题:
等多种元素.回答下列问题:
(1) 元素位于元素周期表的
元素位于元素周期表的_____________ 区, 比
比 稳定的原因为
稳定的原因为_____________ .
(2)材料中列出元素符号的基态原子中,未成对电子数最多的是_____________ ,该元素基态原子中电子占据的最高能层符号是_____________ .
(3)元素周期表中某些元素性质相似,如硼和硅的含氧酸盐都能形成玻璃且互溶,体现了_____________ 规则.
(4)与氧在同一周期的主族元素中第一电离能比氧大的元素有_____________ 个.
(5)下列状态的铁中,电离最外层的一个电子所需能量最大的是_____________(填编号).
(6)储氢合金能有效解决氢气的贮存和运输,对大规模使用氢能具有重要的意义.可用 和
和 处理储氢合金电极,
处理储氢合金电极, 中电负性最小元素的基态原子核外电子有
中电负性最小元素的基态原子核外电子有_____________ 种不同空间运动状态.
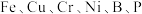 等多种元素.回答下列问题:
等多种元素.回答下列问题:(1)
 元素位于元素周期表的
元素位于元素周期表的 比
比 稳定的原因为
稳定的原因为(2)材料中列出元素符号的基态原子中,未成对电子数最多的是
(3)元素周期表中某些元素性质相似,如硼和硅的含氧酸盐都能形成玻璃且互溶,体现了
(4)与氧在同一周期的主族元素中第一电离能比氧大的元素有
(5)下列状态的铁中,电离最外层的一个电子所需能量最大的是_____________(填编号).
A.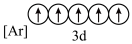 | B. | C.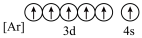 | D.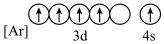 |
(6)储氢合金能有效解决氢气的贮存和运输,对大规模使用氢能具有重要的意义.可用
 和
和 处理储氢合金电极,
处理储氢合金电极, 中电负性最小元素的基态原子核外电子有
中电负性最小元素的基态原子核外电子有
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】A、B、C、D均为短周期元素,他们的原子序数依次增大,B是构成物质种类最多的元素,B和A组成的化合物 B6 A 6 是一种无色透明的液体,不溶于水,密度比水小,C 是地壳中含量最高的非金属元素,D 在同周期元素中原子半径最大。
(1)A、B、D 的元素名称分别为___________ 、____________ 、___________
(2)C 在元素周期表中位置为___________________ 。
(3)A、C、D 能组成多种不同的化合物,这些化合物中既含有极性共价键又含有离子键的化合物为_______________ (写电子式,下同),既含有非极性共价键又含有离子键的化合物为_________________ 。
(4)A 和 D 能组成一种化学活性很高的离子化合物 DA,DA 能和C的单质 C2反应生成一种强碱,请写出 DA 和 C2反应的化学方程式_________________________ 。
(1)A、B、D 的元素名称分别为
(2)C 在元素周期表中位置为
(3)A、C、D 能组成多种不同的化合物,这些化合物中既含有极性共价键又含有离子键的化合物为
(4)A 和 D 能组成一种化学活性很高的离子化合物 DA,DA 能和C的单质 C2反应生成一种强碱,请写出 DA 和 C2反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】元素周期表被认为是“科学共同的语言”,它的发现使化学学习和研究变得有规律可循。其简洁有序的背后,是众多科学家艰苦奋斗的结果。下图是元素周期表的一部分,请按要求回答下列问题:

(1)317年左右,东晋炼丹家葛洪在炼丹时分离出了砷。砷的原子结构示意图为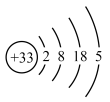 ,砷在周期表中的位置是
,砷在周期表中的位置是___________ 。我国“天宫”空间站的核心舱“天和”选择了高效柔性砷化镓(GaAs)薄膜太阳能电池来供电。原子半径:Ga___________ As(填“>”或“<”)。
(2)1787年,法国化学家拉瓦锡首次发现硅存在于岩石中。硅元素位于元素周期表金属与非金属的分界处,请写出硅单质的一种用途___________ 。
(3)1817年瑞典化学家贝采利乌斯发现硒元素。硫化硒(SeS)可用于治疗脂溢性皮炎。硫元素和硒元素简单气态氢化物热稳定性较强的为___________ (填化学式)。
(4)1825年,丹麦化学家奥斯特首次分离出了铝的单质。铝是地壳中含量最高的金属元素,但铝的利用却比铜和铁晚得多,可能的原因是___________ 。
(5)目前,世界上还有许多科学家为发现新元素孜孜不倦地努力着。可能存在的第119号元素,有人称“类钫”,位于元素周期表第八周期ⅠA族,有关“类钫”的预测说法正确的是
(6)小赵同学在研究元素周期表时发现,碳元素有“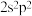 ”这一信息,观察元素周期表后,寻找规律,推测某元素“
”这一信息,观察元素周期表后,寻找规律,推测某元素“ ”中
”中 可能的含义是
可能的含义是___________ 。

(1)317年左右,东晋炼丹家葛洪在炼丹时分离出了砷。砷的原子结构示意图为
 ,砷在周期表中的位置是
,砷在周期表中的位置是(2)1787年,法国化学家拉瓦锡首次发现硅存在于岩石中。硅元素位于元素周期表金属与非金属的分界处,请写出硅单质的一种用途
(3)1817年瑞典化学家贝采利乌斯发现硒元素。硫化硒(SeS)可用于治疗脂溢性皮炎。硫元素和硒元素简单气态氢化物热稳定性较强的为
(4)1825年,丹麦化学家奥斯特首次分离出了铝的单质。铝是地壳中含量最高的金属元素,但铝的利用却比铜和铁晚得多,可能的原因是
(5)目前,世界上还有许多科学家为发现新元素孜孜不倦地努力着。可能存在的第119号元素,有人称“类钫”,位于元素周期表第八周期ⅠA族,有关“类钫”的预测说法正确的是
| A.“类钫”在化合物中显+1价 |
| B.“类钫”单质具有强氧化性 |
| C.“类钫”最高价氧化物对应的水化物为弱碱 |
| D.“类钫”单质能与冷水剧烈反应 |
(6)小赵同学在研究元素周期表时发现,碳元素有“
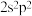 ”这一信息,观察元素周期表后,寻找规律,推测某元素“
”这一信息,观察元素周期表后,寻找规律,推测某元素“ ”中
”中 可能的含义是
可能的含义是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】元素周期表揭示了化学元素间的内在联系,对化学学习和研究有很重要的作用。下表列出了①~⑧八种元素在周期表中的位置:
请按要求回答下列问题:
(1)画出⑧的原子结构示意图________ 。
(2)由③、④、⑦四种元素形成的简单离子半径由大到小的顺序是________ (用离子符号表示)。
(3)由元素①和②形成的最简单化合物甲的电子式为________ ,由元素③和⑥形成化合物乙,则乙与NaOH溶液发生反应的化学方程式为________ 。
(4)硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在元素周期表中的位置如图所示:
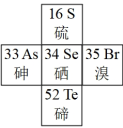
i.在元素周期表中位置表示为________ 。
ii.关于硒的下列说法中正确的是________ 。
A. 既有氧化性又有还原性 B.原子半径由大到小顺序:
既有氧化性又有还原性 B.原子半径由大到小顺序: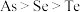
C.热稳定性: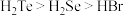 D.酸性:
D.酸性: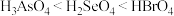
族 周期 | IA | 0 | ||||||
1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
2 | ② | ③ | ||||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
(1)画出⑧的原子结构示意图
(2)由③、④、⑦四种元素形成的简单离子半径由大到小的顺序是
(3)由元素①和②形成的最简单化合物甲的电子式为
(4)硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在元素周期表中的位置如图所示:

i.在元素周期表中位置表示为
ii.关于硒的下列说法中正确的是
A.
 既有氧化性又有还原性 B.原子半径由大到小顺序:
既有氧化性又有还原性 B.原子半径由大到小顺序: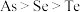
C.热稳定性:
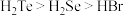 D.酸性:
D.酸性: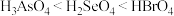
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】下表是元素周期表的一部分
请用元素符号或化学式回答下列问题:
(1)画出D元素的原子结构示意图_______ ;
(2)表中元素,化学性质最不活泼的是_______ ,氧化性最强的单质是_______ ;
(3)元素的最高价氧化物对应的水化物中,碱性最强的是_______ ,呈两性的是_______ ,两者反应的离子方程式为_______ ;
(4)D、E、F对应的气态氢化物中最稳定的是_______ ;
(5)在A、B、C、D中,原子半径最小的是_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | A | |||||||
| 二 | D | E | G | I | ||||
| 三 | B | C | F | H |
(1)画出D元素的原子结构示意图
(2)表中元素,化学性质最不活泼的是
(3)元素的最高价氧化物对应的水化物中,碱性最强的是
(4)D、E、F对应的气态氢化物中最稳定的是
(5)在A、B、C、D中,原子半径最小的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】A、B、C、D、E是五种短周期的主族元素,它们的原子序数依次增大,A、D都能与C按原子个数比为1:1或2:1形成化合物,A、B组成的气态化合物的水溶液呈碱性,E与C的最外层电子数相同。
(1)画出D的原子结构示意图___ ,E元素在周期表中的位置是____ 。
(2)A与C形成原子个数比为1:1的化合物甲,其中含有化学键类型为____ 。
(3)D与C按原子个数比为1:1形成化合物的电子式是____ 。
(4)B、C所形成氢化物的稳定性由强到弱的顺序是____ (填化学式)。
(5)F是一种历史悠久、应用广泛的金属元素。若将F金属投入到盐酸溶液中,生成了浅绿色溶液M。写出M的酸性溶液和A与C形成的化合物甲反应的离子方程式____ 。
(6)E(s)+O2(g)=EO2(g)ΔH1;E(g)+O2(g)=EO2(g) ΔH2,则ΔHl____ ΔH2(填“>”或“<”或“=”)。
(1)画出D的原子结构示意图
(2)A与C形成原子个数比为1:1的化合物甲,其中含有化学键类型为
(3)D与C按原子个数比为1:1形成化合物的电子式是
(4)B、C所形成氢化物的稳定性由强到弱的顺序是
(5)F是一种历史悠久、应用广泛的金属元素。若将F金属投入到盐酸溶液中,生成了浅绿色溶液M。写出M的酸性溶液和A与C形成的化合物甲反应的离子方程式
(6)E(s)+O2(g)=EO2(g)ΔH1;E(g)+O2(g)=EO2(g) ΔH2,则ΔHl
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】X、Y、Z、W、Q、R均为短周期主族元素,且原子序数依次增大。X的原子半径最小,Y是形成有机化合物的必需元素,Z是短周期金属性最强的元素,W是地壳中含量最多的金属元素,Q元素的原子最外层电子数是电子层数的2倍。请回答下列问题:
(1)Y在周期表中的位置是_______
(2)Z与R形成的化合物灼烧时,火焰呈现的颜色是_______
(3)W、Q、R的原子半径由大到小的顺序是_______
(4)已知元素最高价氧化物的水化物的酸性:Q>Y,则元素Q、Y非金属性强弱关系正确的是_______
(5)下列各组元素形成的化合物中一定含有离子键的是_______
(6)元素X的一种核素的质量数是3,则该核素的中子数是_______
(1)Y在周期表中的位置是_______
| A.第二周期IA族 | B.第三周期ⅡA族 |
| C.第二周期IVA族 | D.第三周期IVA族 |
| A.红色 | B.黄色 | C.绿色 | D.紫色 |
| A.R>Q>W | B.W>R>Q | C.Q>R>W | D.W>Q>R |
| A.Q>Y | B.Q=Y | C.Q<Y | D.无法判断 |
| A.X和Q | B.X和Y | C.Y和Q | D.Z和R |
| A.1 | B.2 | C.3 | D.4 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】现有部分短周期元素的性质或原子结构如表:
(1)元素X在元素周期表中的位置为________ 。
(2)元素Y与氢元素形成离子YH 的电子式为
的电子式为______ 。
(3)下列表述中能证明元素X、元素Y非金属性强弱的是_____ 。
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物对应水化物的酸性比X的最高价氧化物对应水化物的酸性强
c.X与Y形成的化合物中X元素呈正价状态
(4)Y的最高价氧化物的水化物与气态氢化物合成的化合物含的化学键类型是_______ 。
(5)写出实验室制取Y的最简单氢化物的化学方程式:________ 。
(6)在100mL 18 mol∙L−1的浓硫酸中加入过量的铜片,加热使之充分反应,若使剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式_______ 。
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 第三周期元素的简单离子中半径最小 |
(2)元素Y与氢元素形成离子YH
 的电子式为
的电子式为(3)下列表述中能证明元素X、元素Y非金属性强弱的是
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物对应水化物的酸性比X的最高价氧化物对应水化物的酸性强
c.X与Y形成的化合物中X元素呈正价状态
(4)Y的最高价氧化物的水化物与气态氢化物合成的化合物含的化学键类型是
(5)写出实验室制取Y的最简单氢化物的化学方程式:
(6)在100mL 18 mol∙L−1的浓硫酸中加入过量的铜片,加热使之充分反应,若使剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式
您最近一年使用:0次



