在庆祝中华人民共和国成立70周年的阅兵仪式上,最后亮相的DF-31A洲际战略导弹是我国大国地位、国防实力的显著标志.其制作材料中包含了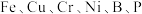 等多种元素.回答下列问题:
等多种元素.回答下列问题:
(1) 元素位于元素周期表的
元素位于元素周期表的_____________ 区, 比
比 稳定的原因为
稳定的原因为_____________ .
(2)材料中列出元素符号的基态原子中,未成对电子数最多的是_____________ ,该元素基态原子中电子占据的最高能层符号是_____________ .
(3)元素周期表中某些元素性质相似,如硼和硅的含氧酸盐都能形成玻璃且互溶,体现了_____________ 规则.
(4)与氧在同一周期的主族元素中第一电离能比氧大的元素有_____________ 个.
(5)下列状态的铁中,电离最外层的一个电子所需能量最大的是_____________(填编号).
(6)储氢合金能有效解决氢气的贮存和运输,对大规模使用氢能具有重要的意义.可用 和
和 处理储氢合金电极,
处理储氢合金电极, 中电负性最小元素的基态原子核外电子有
中电负性最小元素的基态原子核外电子有_____________ 种不同空间运动状态.
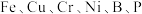 等多种元素.回答下列问题:
等多种元素.回答下列问题:(1)
 元素位于元素周期表的
元素位于元素周期表的 比
比 稳定的原因为
稳定的原因为(2)材料中列出元素符号的基态原子中,未成对电子数最多的是
(3)元素周期表中某些元素性质相似,如硼和硅的含氧酸盐都能形成玻璃且互溶,体现了
(4)与氧在同一周期的主族元素中第一电离能比氧大的元素有
(5)下列状态的铁中,电离最外层的一个电子所需能量最大的是_____________(填编号).
A.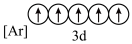 | B. | C.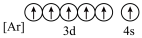 | D.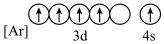 |
(6)储氢合金能有效解决氢气的贮存和运输,对大规模使用氢能具有重要的意义.可用
 和
和 处理储氢合金电极,
处理储氢合金电极, 中电负性最小元素的基态原子核外电子有
中电负性最小元素的基态原子核外电子有
更新时间:2024-01-18 16:33:35
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
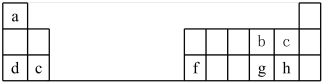
【推荐1】元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。下表是元素周期表的一部分。
(2)a-h元素的最高价氧化物对应的水化物中,酸性最强的是___________ (填化学式)。
(3)b元素有三种稳定核素,其式量分别为16、17、18,则三种核素的中子数之比为___________ 。
(4)c、g、h三种元素形成的气态氢化物中,稳定性最小的物质的结构式是___________ 。
(5)d元素的简单离子的结构示意图为___________ 。
(6)d的最高价氧化物对应水化物与f的最高价氧化物对应水化物的溶液反应的离子方程式为___________ 。
(7)若d单质着火,可用于灭火的物质是___________。
(8)下列关于元素周期表的叙述正确的是___________。
| A.第三周期第6族 | B.第三周期VI主族 |
| C.第三周期第6A族 | D.第三周期VIA族 |
(3)b元素有三种稳定核素,其式量分别为16、17、18,则三种核素的中子数之比为
(4)c、g、h三种元素形成的气态氢化物中,稳定性最小的物质的结构式是
(5)d元素的简单离子的结构示意图为
(6)d的最高价氧化物对应水化物与f的最高价氧化物对应水化物的溶液反应的离子方程式为
(7)若d单质着火,可用于灭火的物质是___________。
| A.自来水 | B.CO2 | C.干沙子 | D.湿抹布 |
| A.元素周期表中所含元素最多的族是BVII族 |
| B.IA族的元素全部是金属元素 |
| C.在元素周期表中金属与非金属的分界处可以找到半导体材料 |
| D.只有IIA族元素的原子最外层有2个电子 |
您最近一年使用:0次
【推荐2】Fe、Co、Ni是三种重要的金属元素。回答下列问题:
(1)Fe、Co、Ni在周期表中的位置为______ ,基态Co原子的价层电子排布式为______ ,与Ni同周期且与Ni具有相同未成对电子数的元素有_______ 种。
(2)Fe、Co、Ni能与Cl2反应,其中Co和Ni生成二氯化物。由此推断FeCl3、CoCl3和Cl2的氧化性由强到弱的顺序为____ 。Co(OH)3与盐酸反应有黄绿色气体生成,写出反应的离子方程式:_____ 。
(3)95℃时将Ni片浸在不同质量分数的硫酸中,经4小时腐蚀后的质量损失情况如图所示。
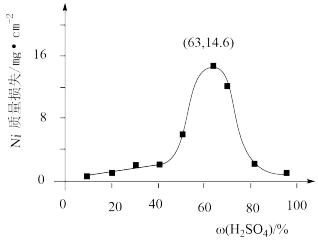
当w(H2SO4)大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为_____ 。由于Ni与硫酸反应很慢,而与稀HNO3反应很快,工业上选用H2SO4和HNO3的混酸与Ni反应制备NiSO4,为了提高产物的纯度,在硫酸中添加HNO3的方式为_____ (填“一次过量”或“少量多次”),此法制备NiSO4的化学方程式为_____ 。
(1)Fe、Co、Ni在周期表中的位置为
(2)Fe、Co、Ni能与Cl2反应,其中Co和Ni生成二氯化物。由此推断FeCl3、CoCl3和Cl2的氧化性由强到弱的顺序为
(3)95℃时将Ni片浸在不同质量分数的硫酸中,经4小时腐蚀后的质量损失情况如图所示。

当w(H2SO4)大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。表中列出了a~g 7种元素在周期表中的位置。
(1)a的元素符号是_______ 。
(2)写出c单质与b的最高价氧化物水化物反应的离子方程式_______ 。
(3)d、e的最高价氧化物对应的水化物中,酸性较强的是_______ 。(填化学式)
(4)已知硒(Se)与d同主族,且位于d下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是_______ 。
① 其单质在常温下呈固态
② SeO2既有氧化性又有还原性
③ 最高价氧化物对应的水化物的化学式为H2SeO3
④ 非金属性比e元素的强
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | a | |||||||
| 3 | b | c | d | e |
(2)写出c单质与b的最高价氧化物水化物反应的离子方程式
(3)d、e的最高价氧化物对应的水化物中,酸性较强的是
(4)已知硒(Se)与d同主族,且位于d下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
① 其单质在常温下呈固态
② SeO2既有氧化性又有还原性
③ 最高价氧化物对应的水化物的化学式为H2SeO3
④ 非金属性比e元素的强
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】元素A、B、C、D的离子核外都有10个电子,A的氯化物中,电子总数为28,A和B的化合物A2B中共有30个电子,B与C的化合物为C2B3型;C与D的化合物为CD3型。试根据有关元素的化合物的构成确定其化合物的化学式:
ACl:________ ;A2B:________ ;C2B3:________ ;CD3:________ 。
ACl:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】下表为元素周期表中的一部分,表中列出8种元素在周期表中的位置,按要求回答下列问题。
(1)在①~⑧元素中化学性质最不活泼的元素的名称是____ ,金属性最强的元素的名称是____ 。
(2)③、④、⑥三种元素中的原子半径最小的是____ (填元素符号)。
(3)①、②、③三种元素形成的离子,离子半径由大到小的顺序是_____ (用离子符号填写)。
(4)④与⑥形成的三原子化合物的电子式为_____ 。
(5)④与氢形成含氢量最高的化合物的结构式____ 。
(6)写出①和③两种元素的最高价氧化物对应的水化物相互反应的离子方程式:____ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ④ | ⑥ | ||||||
| 3 | ① | ② | ③ | ⑤ | ⑦ | ⑧ |
(1)在①~⑧元素中化学性质最不活泼的元素的名称是
(2)③、④、⑥三种元素中的原子半径最小的是
(3)①、②、③三种元素形成的离子,离子半径由大到小的顺序是
(4)④与⑥形成的三原子化合物的电子式为
(5)④与氢形成含氢量最高的化合物的结构式
(6)写出①和③两种元素的最高价氧化物对应的水化物相互反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】元素周期表前20号元素X、Y、Z、W、R的原子序数依次增大,X原子的最外层电子数比最内层电子数多5,其他元素的性质如下表所示:
请回答下列问题:
(1)Y元素在元素周期表中的位置为______________ 。
(2)R元素的最高价氧化物对应水化物的电子式为_____________ ;写出该物质的水溶液与Al反应的离子方程式:_________________ 。
(3)化合物 广泛用于橡胶工业,其结构式为
广泛用于橡胶工业,其结构式为_______ ;从原子结构角度解释Z、W的非金属性强弱的原因:__________ 。
(4)化合物 可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等。
可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等。 与少量
与少量 反应生成两种单质和一种二元化合物,写出该反应的化学方程式:
反应生成两种单质和一种二元化合物,写出该反应的化学方程式:____ ;若 过量,生成物中会有
过量,生成物中会有________ (填化学式)。
| 元素 | Y | Z | W | R |
| 原子半径/pm | 117 | 102 | 99 | - |
| 主要化合价 | -4、+4 | 2、+6 | -1、+7 | +1 |
(1)Y元素在元素周期表中的位置为
(2)R元素的最高价氧化物对应水化物的电子式为
(3)化合物
 广泛用于橡胶工业,其结构式为
广泛用于橡胶工业,其结构式为(4)化合物
 可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等。
可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等。 与少量
与少量 反应生成两种单质和一种二元化合物,写出该反应的化学方程式:
反应生成两种单质和一种二元化合物,写出该反应的化学方程式: 过量,生成物中会有
过量,生成物中会有
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】原子序数依次增大的A、B、C、D、E、F六种元素均为前四周期元素,A是形成化合物种类最多的元素,B与A同周期,其原子核外s能级上的电子总数与p能级上的电子总数相等,C为第3周期元素,其离子半径在该周期中最小,D原子核外p能级上的电子总数比s能级上的电子总数多2,E元素位于元素周期表中的第8列,F的单质为紫红色金属。回答下列问题:
(1)D在元素周期表中的位置为___________ 。
(2)A元素的原子核外共有___________ 种不同运动状态的电子;B元素基态原子中能量最高的电子所占据的原子轨道呈___________ 形。
(3)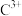 与过量氨水反应的离子方程式为
与过量氨水反应的离子方程式为___________ 。
(4)E元素位于元素周期表中___________ 区(按电子排布分区),其基态原子价电子轨道表示式为___________ 。
(5)基态F原子的核外电子排布式为___________ ,其基态原子核外填充有电子的能量最高的电子层的符号为___________ ,该电子层上具有的原子轨道数是___________ 。
(1)D在元素周期表中的位置为
(2)A元素的原子核外共有
(3)
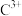 与过量氨水反应的离子方程式为
与过量氨水反应的离子方程式为(4)E元素位于元素周期表中
(5)基态F原子的核外电子排布式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】A、B、C、D、E代表5种元素。请填空:
(1)A元素基态原子的最外层p能级的电子数等于次外层的电子总数,其基态原子的电子排布图为_______ 。
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,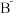 的结构示意图为
的结构示意图为_______ ,C元素在元素周期表的_______ 区。
(3)D元素的正三价离子的3d能级为半充满状态,其基态原子的电子排布式_______ 。试根据原子核外电子排布所遵循的原理解释D的二价阳离子具有较强的还原性,易被氧化为正三价离子的原因:_______ 。
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的价电子排布式为_______ 。
(1)A元素基态原子的最外层p能级的电子数等于次外层的电子总数,其基态原子的电子排布图为
(2)B元素的负一价离子和C元素的正一价离子的电子层结构都与氩相同,
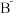 的结构示意图为
的结构示意图为(3)D元素的正三价离子的3d能级为半充满状态,其基态原子的电子排布式
(4)E元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,其基态原子的价电子排布式为
您最近一年使用:0次
【推荐3】X、Y、Z、M、Q是元素周期表前四周期的元素,且原子序数依次增大,其相关信息如表所示:
(1)X最外层电子的轨道表达式是 ___________ 。
(2)M元素的名称是___________ 。
(3)Z元素基态原子中能量最高的电子的电子云在空间有___________ 个伸展方向,原子轨道呈___________ 形。
(4)小范同学写了基态原子P的两个价电子的表达形式,分析其分别违背了什么原理:
①3s13p4:___________ ,
②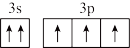 :
:___ 。
(5)元素Q可形成Q2+和Q3+,其中较稳定的是Q3+,原因是___ 。
| 元素 | 相关信息 |
| X | 次外层电子数是最外层电子数的 |
| Y | 形成的氧化物和强酸、强碱都可以反应 |
| Z | 基态原子的最外层p轨道上有两个电子的自旋方向与其他电子的自旋方向相反 |
| M | 前4周期元素原子核外电子排布中未成对电子数最多的元素 |
| Q | 基态原子核外有7个能级上有电子且能量最高的能级上有6个电子 |
(2)M元素的名称是
(3)Z元素基态原子中能量最高的电子的电子云在空间有
(4)小范同学写了基态原子P的两个价电子的表达形式,分析其分别违背了什么原理:
①3s13p4:
②
 :
:(5)元素Q可形成Q2+和Q3+,其中较稳定的是Q3+,原因是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属同一族,它们原子的最外层电子排布为ns1。B和D也属同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)由这五种元素组成的一种化合物是(写化学式)________________________ 。
(2)写出C元素基态原子的电子排布式_________________________ 。
(3)用轨道表示式表示D元素原子的价电子构型____________________ 。
(4)元素B与D的电负性的大小关系是___________ ,C与E的第一电离能的大小关系是___________ 。(填﹥、﹤、﹦,并且用元素符号表示)
(1)由这五种元素组成的一种化合物是(写化学式)
(2)写出C元素基态原子的电子排布式
(3)用轨道表示式表示D元素原子的价电子构型
(4)元素B与D的电负性的大小关系是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】Mn、Fe、Se等元素对人体生命活动非常重要,例如Se参与合成人体内多种含硒酶和含硒
蛋白,具有多种生物功能。请结合图示回答下列问题。
(1)锰和铁同周期且相邻,现有几种锰、铁元素的相应状态,①锰: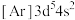 、②铁:
、②铁: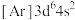 、③锰:
、③锰: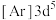 、④铁:
、④铁: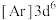 ,失去1个电子需要的能量由大到小排序是___________(填字母)。
,失去1个电子需要的能量由大到小排序是___________(填字母)。
(2)硒代半胱氨酸是第21个组成人体蛋白质的氨基酸,分子式为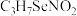 ,其结构简式如图所示。
,其结构简式如图所示。
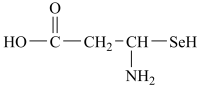
①其中杂化方式为 和
和 的碳原子个数比为
的碳原子个数比为___________ 。
②下列说法正确的是:___________ 。
A.C、N、O三种元素第一电离能从大到小的顺序是
B.硒代半胱氨酸分子中存在的化学键类型包括极性键、非极性键、氢键
C.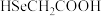 比
比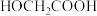 酸性弱
酸性弱
D.一个硒代半胱氨酸分子中σ键和π键的比例为
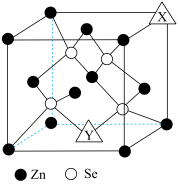
(3)硒化锌是一种化学惰性材料,具有纯度高,环境适应能力强,易于加工等特点,是良好的聚焦镜基材。下图所示是硒化锌晶胞结构(类似金刚石晶胞),从晶胞基本定义可知X、Y均为_______ (填元素符号),距离Se最近的Zn有________ 个,已知晶胞参数为anm,则硒化锌密度为________ 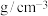 。
。
蛋白,具有多种生物功能。请结合图示回答下列问题。
(1)锰和铁同周期且相邻,现有几种锰、铁元素的相应状态,①锰:
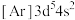 、②铁:
、②铁: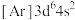 、③锰:
、③锰: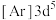 、④铁:
、④铁: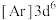 ,失去1个电子需要的能量由大到小排序是___________(填字母)。
,失去1个电子需要的能量由大到小排序是___________(填字母)。| A.①②③④ | B.④③②① | C.③④②① | D.④②③① |
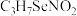 ,其结构简式如图所示。
,其结构简式如图所示。
①其中杂化方式为
 和
和 的碳原子个数比为
的碳原子个数比为②下列说法正确的是:
A.C、N、O三种元素第一电离能从大到小的顺序是

B.硒代半胱氨酸分子中存在的化学键类型包括极性键、非极性键、氢键
C.
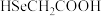 比
比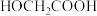 酸性弱
酸性弱D.一个硒代半胱氨酸分子中σ键和π键的比例为

(3)硒化锌是一种化学惰性材料,具有纯度高,环境适应能力强,易于加工等特点,是良好的聚焦镜基材。下图所示是硒化锌晶胞结构(类似金刚石晶胞),从晶胞基本定义可知X、Y均为
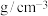 。
。
您最近一年使用:0次
【推荐3】A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表所示。
请回答下列问题(用对应元素的元素符号作答)。
(1)写出D元素基态原子的价层电子排布式:_______ ;基态A原子电子占据最高能级的电子云轮廓图为_______ 形;基态E2+的价层电子排布图:_______ 。
(2)这5种元素中电负性最大的元素是_______ (用元素符号表示,下同),A、B、C三种元素的第一电离能由大到小的顺序为_______ 。
(3)B、C、D的简单离子的半径由大到小的顺序为_______ (用离子符号表示)。
(4)写出含有C的强氧化性的氢化物的电子式:_______ 。
| 元素 | 相关信息 |
| A | 基态原子的价层电子排布为nsnnpn |
| B | 基态原子中的未成对电子数是同周期元素原子中最多的 |
| C | 基态原子的最外层电子数是电子层数的3倍 |
| D | 简单离子是第三周期元素所形成的离子中半径最小的 |
| E | 基态原子的价电子层中的未成对电子数为4 |
(1)写出D元素基态原子的价层电子排布式:
(2)这5种元素中电负性最大的元素是
(3)B、C、D的简单离子的半径由大到小的顺序为
(4)写出含有C的强氧化性的氢化物的电子式:
您最近一年使用:0次



