元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。表中列出了a~g 7种元素在周期表中的位置。
(1)a的元素符号是_______ 。
(2)写出c单质与b的最高价氧化物水化物反应的离子方程式_______ 。
(3)d、e的最高价氧化物对应的水化物中,酸性较强的是_______ 。(填化学式)
(4)已知硒(Se)与d同主族,且位于d下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是_______ 。
① 其单质在常温下呈固态
② SeO2既有氧化性又有还原性
③ 最高价氧化物对应的水化物的化学式为H2SeO3
④ 非金属性比e元素的强
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | a | |||||||
| 3 | b | c | d | e |
(2)写出c单质与b的最高价氧化物水化物反应的离子方程式
(3)d、e的最高价氧化物对应的水化物中,酸性较强的是
(4)已知硒(Se)与d同主族,且位于d下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
① 其单质在常温下呈固态
② SeO2既有氧化性又有还原性
③ 最高价氧化物对应的水化物的化学式为H2SeO3
④ 非金属性比e元素的强
更新时间:2021-07-27 09:29:14
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】在庆祝中华人民共和国成立70周年的阅兵仪式上,最后亮相的DF-31A洲际战略导弹是我国大国地位、国防实力的显著标志.其制作材料中包含了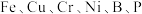 等多种元素.回答下列问题:
等多种元素.回答下列问题:
(1) 元素位于元素周期表的
元素位于元素周期表的_____________ 区, 比
比 稳定的原因为
稳定的原因为_____________ .
(2)材料中列出元素符号的基态原子中,未成对电子数最多的是_____________ ,该元素基态原子中电子占据的最高能层符号是_____________ .
(3)元素周期表中某些元素性质相似,如硼和硅的含氧酸盐都能形成玻璃且互溶,体现了_____________ 规则.
(4)与氧在同一周期的主族元素中第一电离能比氧大的元素有_____________ 个.
(5)下列状态的铁中,电离最外层的一个电子所需能量最大的是_____________(填编号).
(6)储氢合金能有效解决氢气的贮存和运输,对大规模使用氢能具有重要的意义.可用 和
和 处理储氢合金电极,
处理储氢合金电极, 中电负性最小元素的基态原子核外电子有
中电负性最小元素的基态原子核外电子有_____________ 种不同空间运动状态.
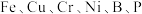 等多种元素.回答下列问题:
等多种元素.回答下列问题:(1)
 元素位于元素周期表的
元素位于元素周期表的 比
比 稳定的原因为
稳定的原因为(2)材料中列出元素符号的基态原子中,未成对电子数最多的是
(3)元素周期表中某些元素性质相似,如硼和硅的含氧酸盐都能形成玻璃且互溶,体现了
(4)与氧在同一周期的主族元素中第一电离能比氧大的元素有
(5)下列状态的铁中,电离最外层的一个电子所需能量最大的是_____________(填编号).
A.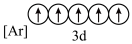 | B. | C.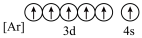 | D.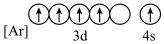 |
(6)储氢合金能有效解决氢气的贮存和运输,对大规模使用氢能具有重要的意义.可用
 和
和 处理储氢合金电极,
处理储氢合金电极, 中电负性最小元素的基态原子核外电子有
中电负性最小元素的基态原子核外电子有
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】碳酸锶(SrCO3)是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90% SrCO3,少量MgCO3、CaCO3、BaCO3等)制备高纯碳酸锶的工艺流程如下:
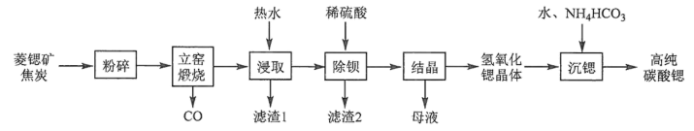
Sr(OH)2在水中的溶解度
(1)元素Sr位于元素周期表第_______ 周期第_______ 族。
(2)菱锶矿、焦炭混合粉碎的目的是_______ 。
(3)“立窑煅烧”中SrCO3与焦炭反应的化学方程式为_______ 。进行煅烧反应的立窑衬里应选择_______ (填“石英砂砖”或“碱性耐火砖”)。

Sr(OH)2在水中的溶解度
| 温度/℃ | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
| 溶解度/(g/100g) | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
(1)元素Sr位于元素周期表第
(2)菱锶矿、焦炭混合粉碎的目的是
(3)“立窑煅烧”中SrCO3与焦炭反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】现有四种元素,其中A、B、C为短周期主族元素,D为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)已知BA5为离子化合物,写出其电子式:_____ 。
(2)B基态原子中能量最高的电子,其电子云在空间有______ 个方向,原子轨道呈______ 形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为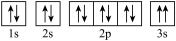 。该同学所画的电子排布图违背了
。该同学所画的电子排布图违背了____ 。
(4)D位于_______ 族_______ 区,价电子排布式为_______ 。
元素 | 相关信息 |
A | 元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
B | 元素原子的核外p电子数比s电子数少1 |
C | 原子的第一至第四电离能分别是I1=738 kJ·mol-1;I2=1 451 kJ·mol-1;I3=7 733 kJ·mol-1;I4=10 540 kJ·mol-1 |
D | 在周期表的第七列 |
(2)B基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为
 。该同学所画的电子排布图违背了
。该同学所画的电子排布图违背了(4)D位于
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题:
(1)写出M原子的外围电子排布式_____ 。
(2)画出Y的负一价离子的电子式_____ ,元素Y的含氧酸中,酸性最强的是_____ (写化学式)。
(3)Y的同周期元素中,第一电离能最大的是______ (写元素符号);同周期主族元素从左到右,原子半径逐渐______ ,原因是______ 。
(4)M与Y形成的一种化合物MY,该化合物难溶于水但易溶于氨水,此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为______ 。
(1)写出M原子的外围电子排布式
(2)画出Y的负一价离子的电子式
(3)Y的同周期元素中,第一电离能最大的是
(4)M与Y形成的一种化合物MY,该化合物难溶于水但易溶于氨水,此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是元素周期表的一部分,回答下列有关问题:
(1)在①~⑫元素中,非金属性最强的元素是______________ 。(填元素符号)
(2) 元素⑤的最高价氧化物的水化物分别与元素③、⑧的最高价氧化物的水化物反应的离子方程式_______________________ ;_______________________ 。
(3)第三周期中原子半径最大的元素跟它同周期原子半径最小的元素它们可以形成化合物,用电子式表示其形成过程__________________________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ |
|
|
(2) 元素⑤的最高价氧化物的水化物分别与元素③、⑧的最高价氧化物的水化物反应的离子方程式
(3)第三周期中原子半径最大的元素跟它同周期原子半径最小的元素它们可以形成化合物,用电子式表示其形成过程
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】Ⅰ.短周期主族元素W、X、Y、Z的原子序数依次增大,元素W的一种单质是熔点高、硬度大的宝石,Y的原子半径在所有短周期主族元素中最大。X和Z同主族,由X、Y和Z三张元素形成的一种盐溶于水后,加入稀盐酸,有刺激性气体产生。回答下列问题:
(1)Y元素在元素周期表中的位置是_________________ 。
(2)Z元素是_____________ (填元素符号),由X和Z两种元素形成的化合物有______________ 。
(3)四种元素中____________ (填元素符号)是形成化合物最多的元素。
Ⅱ.(4)某同学做同周期元素性质递变规律实验时,自 己设计了一套实验方案,并记录了有关实验现象,如表所示:
①本实验的目的是___________________________ 。
②写出与实验方案相对应的实验现象。
与实验方案2对应的实验现象是______________________ (填上表中的序号,下同);与实验方案3对应的实验现象是_________________ 。
③得出规律:同周期元素从左到右____________________ 。
(1)Y元素在元素周期表中的位置是
(2)Z元素是
(3)四种元素中
Ⅱ.(4)某同学做同周期元素性质递变规律实验时,自 己设计了一套实验方案,并记录了有关实验现象,如表所示:
| 实验方案 | 实验现象 |
| 1.用砂纸打磨后的镁带与沸水反应,再向反应液中滴加酚酞 | A.浮于水面,熔成小球,四处游动,逐渐缩小,溶液变红色 |
| 2.向新制的H2S饱和溶液中滴加新制的氯水 | B.产生气体,气体可燃,溶液变浅红色 |
| 3.钠与滴有酚酞试液的冷水反应 | C.反应不十分强烈,产生的气体可以在空气小燃烧 |
| 4.镁带与2 mol/L的盐酸反应 | D.剧烈反应,产生可燃性气体 |
| 5.铝条与 2 mol/L的盐酸反应 | E.生成淡黄色沉淀 |
②写出与实验方案相对应的实验现象。
与实验方案2对应的实验现象是
③得出规律:同周期元素从左到右
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】元素周期表揭示了元素之间的内在联系,使元素构成了一个较为系统的体系.请回答下列问题:
Ⅰ.元素周期表的建立与完善是一个渐进的过程.直至20世纪初,原子结构奥秘被揭示后,元素周期表中元素的排序由依据相对原子质量改为依据原子的_______ 。按照元素在周期表中的顺序给元素编号,得到原子序数。人们发现原子序数与元素的原子结构之间存在如下关系:原子序数=_______ =核外电子数
Ⅱ.图为元素周期表的一部分,序号①~⑥分别代表周期表中相应位置的种元素。
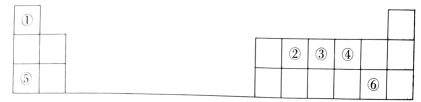
(1)②、③、④三种元素中,原子半径由大到小的顺序为_______ (用元素符号表示)。
(2)①、④、⑤三种元素形成的化合物的电子式为_______ ,该化合物中化学键的类型有_______ 。
(3)元素Q位于第四周期,且与元素⑥均为同一主族元素。请用离子方程说明⑥和Q两种元素单质氧化性的强弱:_______ 。根据元素周期律推测,下列性质中Q不可能具有的是_______ (填选项字母)。
A.最高正化合价为 B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
Ⅰ.元素周期表的建立与完善是一个渐进的过程.直至20世纪初,原子结构奥秘被揭示后,元素周期表中元素的排序由依据相对原子质量改为依据原子的
Ⅱ.图为元素周期表的一部分,序号①~⑥分别代表周期表中相应位置的种元素。

(1)②、③、④三种元素中,原子半径由大到小的顺序为
(2)①、④、⑤三种元素形成的化合物的电子式为
(3)元素Q位于第四周期,且与元素⑥均为同一主族元素。请用离子方程说明⑥和Q两种元素单质氧化性的强弱:
A.最高正化合价为
 B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
B.气态氢化物比⑥的稳定 C.单质在常温下可与氢气化合
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
【推荐2】某同学完成如下实验。
(1)实验记录(请补全表格中空格 )
(2)该实验的目的是______________________ 。
(3)氯、溴、碘单质氧化性逐渐减弱的原因:同主族元素,最外层电子数相同,从上到下,_________ ,得电子能力逐渐减弱。
(1)实验记录(
| 实验步骤 | 实验现象 | 离子方程式 |
 | ①溶液分层 ②下层呈橙色。 | |
 | ①溶液分层 ② | Br2+2I-=I2+2Br- |
(2)该实验的目的是
(3)氯、溴、碘单质氧化性逐渐减弱的原因:同主族元素,最外层电子数相同,从上到下,
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】元素周期表、元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了a~g 7种元素在周期表中的位置。
(1)a的元素符号是_____ 。
(2)b、c的最高价氧化物对应的水化物(氢氧化物)中,碱性较弱的是_____ (填化学式)。
(3)非金属性e强于g,用原子结构解释原因_____________________________ ,得电子能力e大于g。
(4)下列对f及其化合物的推断中,正确的是_____ (填字母)。
A.f的最高化合价为+6价
B.f的氢化物的稳定性弱于d的氢化物的稳定性
C.f的最高价氧化物对应的水化物属于碱
(5)单质c与b的最高价氧化物的水化物反应的化学方程式为___________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | a | |||||||
3 | b | c | d | e | ||||
4 | f | g |
(2)b、c的最高价氧化物对应的水化物(氢氧化物)中,碱性较弱的是
(3)非金属性e强于g,用原子结构解释原因
(4)下列对f及其化合物的推断中,正确的是
A.f的最高化合价为+6价
B.f的氢化物的稳定性弱于d的氢化物的稳定性
C.f的最高价氧化物对应的水化物属于碱
(5)单质c与b的最高价氧化物的水化物反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是元素周期表的一部分,回答下列有关问题:
(1)写出⑥的元素符号: ____________ ,画出⑫ 的原子结构示意图________________ ;
(2)写出③的单质在空气中燃烧后的产物与二氧化碳反应的化学方程式:___________________________________ ;该反应每生成1mol气体转移_______ 个电子。
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是___________________ ,碱性最强的是___________________ ,呈两性的氢氧化物是___________________ ;
(4)写出单质③在空气中燃烧生成产物的电子式___________________ ;
(5)用电子式表示出④的氯化物的形成过程_____________________________________ ;
(6)写出实验室制取⑧的单质的化学方程式___________________________________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)写出③的单质在空气中燃烧后的产物与二氧化碳反应的化学方程式:
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是
(4)写出单质③在空气中燃烧生成产物的电子式
(5)用电子式表示出④的氯化物的形成过程
(6)写出实验室制取⑧的单质的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】A、X,Y、Z、R、W为六种短周期元素。A是短周期中半径最小的元素;X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价代数和为4;Z的单质常用于漂白工业;R是短周期元素中金属性最强的元素,W是生活中的常见金属,其氧化物常作耐高温材料。回答下列问题:
(1)Y元素的名称是___ ,在周期表中的位置是___ 。
(2)写出化合物AZX的电子式:___ ;化合物R2X2存在的化学键类型是___ 。
(3)比较X、Z、R三种元素对应的简单离子半径大小:___ (用离子符号和“>”表示)。
(4)下列事实能证明R比W金属性强的这一结论的是___ (填序号)。
a.R的熔点低于W
b.常温下,R与水剧烈反应而W不能
c.最高价氧化物对应的水化物碱性:ROH>W(OH)3
d.最外层电子数:W>R
(5)写出工业上制备W的单质的化学方程式:___ 。
(6)A单质与X单质在KOH溶液中可以组成燃料电池,则正极附近溶液的pH将___ (填“变大”“变小”或“不变”,下同);放电一段时间KOH的物质的量___ 。
(7)用电子式表示RZ的形成过程:___ 。
(1)Y元素的名称是
(2)写出化合物AZX的电子式:
(3)比较X、Z、R三种元素对应的简单离子半径大小:
(4)下列事实能证明R比W金属性强的这一结论的是
a.R的熔点低于W
b.常温下,R与水剧烈反应而W不能
c.最高价氧化物对应的水化物碱性:ROH>W(OH)3
d.最外层电子数:W>R
(5)写出工业上制备W的单质的化学方程式:
(6)A单质与X单质在KOH溶液中可以组成燃料电池,则正极附近溶液的pH将
(7)用电子式表示RZ的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】现有A、B、M、D、F、E六种短周期元素,原子序数依次增大。它们的性质或原子结构如表所示:
请回答:
(1)M在元素周期表中的位置为____ 。
(2)A、M形成的常见液态化合物中,能杀菌消毒的是____ (填化学式,下同)。
(3)B的最高价氧化物对应的水化物为_____ 。
(4)F与D相比,金属性较强的是____ (填元素符号),请从原子结构的角度解释原因:____ 。
(5)E的单质通入D的最高价氧化物对应水化物的溶液中,可以制取漂白液,发生反应的离子方程式为____ 。
(6)硒元素对人体有一定的保健作用。已知硒元素与M同主族,与钙同周期。下列关于硒的说法错误的是____ (填字母)。
| 元素 | 性质或原子结构 |
| A | 原子核内只有一个质子 |
| B | 形成的单质是空气中含量最多的气体 |
| M | 原子的最外层电子数是次外层电子数的3倍 |
| D | M层比K层少一个电子 |
| E | 最高正化合价与最低负化合价的代数和为6 |
| F | 比D原子序数大1 |
(1)M在元素周期表中的位置为
(2)A、M形成的常见液态化合物中,能杀菌消毒的是
(3)B的最高价氧化物对应的水化物为
(4)F与D相比,金属性较强的是
(5)E的单质通入D的最高价氧化物对应水化物的溶液中,可以制取漂白液,发生反应的离子方程式为
(6)硒元素对人体有一定的保健作用。已知硒元素与M同主族,与钙同周期。下列关于硒的说法错误的是
| A.原子序数为26 | B.常温下为固体,最高价氧化物是SeO3 |
| C.原子半径比钙小 | D.气态氢化物的化学式是H2Se,稳定性比HBr弱 |
您最近一年使用:0次





