下表是元素周期表的一部分,回答下列有关问题:
(1)在①~⑫元素中,非金属性最强的元素是______________ 。(填元素符号)
(2) 元素⑤的最高价氧化物的水化物分别与元素③、⑧的最高价氧化物的水化物反应的离子方程式_______________________ ;_______________________ 。
(3)第三周期中原子半径最大的元素跟它同周期原子半径最小的元素它们可以形成化合物,用电子式表示其形成过程__________________________ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
4 | ⑩ |
|
|
(2) 元素⑤的最高价氧化物的水化物分别与元素③、⑧的最高价氧化物的水化物反应的离子方程式
(3)第三周期中原子半径最大的元素跟它同周期原子半径最小的元素它们可以形成化合物,用电子式表示其形成过程
更新时间:2020/10/03 13:50:27
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是元素周期表的一部分,针对表中的①~⑩中元素,请用化学用语填空回答以下问题:
(1)化学性质最不活泼的元素原子的原子结构示意图为________ 。
(2)元素①、②的简单氢化物的稳定性更强的是______________ (用化学式表示,下同)。
(3)元素的最高价氧化物对应的水化物中酸性最强的是______ ,碱性最强的是____ ,呈两性的氢氧化物是________ ,元素③的最高价氧化物对应水化物中含有的化学键类型为________ 。
(4)在③~⑦元素中,简单离子半径最小的是_________ 。
(5)元素③的过氧化物的电子式为_________ 。
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(2)元素①、②的简单氢化物的稳定性更强的是
(3)元素的最高价氧化物对应的水化物中酸性最强的是
(4)在③~⑦元素中,简单离子半径最小的是
(5)元素③的过氧化物的电子式为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐2】一种哥德式“元素周期表城堡”如图所示,部分元素已标出。回答下列问题:___________ 族。
(2)下列关于图中元素的说法正确的是___________(填标号)。
(3)向苦卤中通入 生成
生成 的离子方程式为
的离子方程式为___________ 。
(4)向 溶液中逐滴加入
溶液中逐滴加入 溶液,观察到先产生白色沉淀,后沉淀溶解。沉淀溶解过程发生反应的离子方程式为
溶液,观察到先产生白色沉淀,后沉淀溶解。沉淀溶解过程发生反应的离子方程式为___________ 。
(5)苯与液溴在铁粉作用下生成溴苯的化学方程式为___________ 。
(6)盛放 溶液的试剂瓶不能用磨口玻璃塞的原因为
溶液的试剂瓶不能用磨口玻璃塞的原因为___________ (用化学方程式表示)。
(7)氧化硅薄膜制备过程中存在物质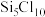 ,从化学键的角度分析
,从化学键的角度分析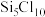 的结构是(a)而不是(b)的原因
的结构是(a)而不是(b)的原因___________ 。
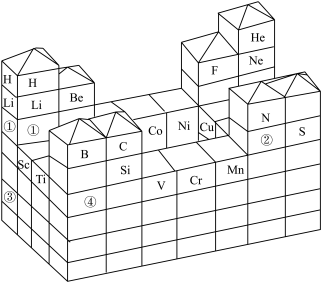
(2)下列关于图中元素的说法正确的是___________(填标号)。
A.单质与水反应的剧烈程度:①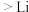 | B.单质与 化合的难易程度:② 化合的难易程度:②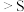 |
| C.③形成的氧化物只有一种 | D.④位于第4周期ⅢA族 |
(3)向苦卤中通入
 生成
生成 的离子方程式为
的离子方程式为(4)向
 溶液中逐滴加入
溶液中逐滴加入 溶液,观察到先产生白色沉淀,后沉淀溶解。沉淀溶解过程发生反应的离子方程式为
溶液,观察到先产生白色沉淀,后沉淀溶解。沉淀溶解过程发生反应的离子方程式为(5)苯与液溴在铁粉作用下生成溴苯的化学方程式为
(6)盛放
 溶液的试剂瓶不能用磨口玻璃塞的原因为
溶液的试剂瓶不能用磨口玻璃塞的原因为(7)氧化硅薄膜制备过程中存在物质
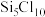 ,从化学键的角度分析
,从化学键的角度分析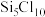 的结构是(a)而不是(b)的原因
的结构是(a)而不是(b)的原因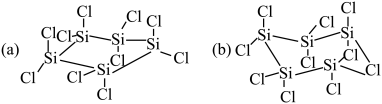
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】下表为元素周期表中的一部分,表中列出8种元素在周期表中的位置,按要求回答下列问题。
(1)在①~⑧元素中化学性质最不活泼的元素的名称是____ ,金属性最强的元素的名称是____ 。
(2)③、④、⑥三种元素中的原子半径最小的是_____________ (填元素符号)。
(3)①、②、③三种元素形成的离子,离子半径由大到小的顺序是____ (用离子符号填写)。
(4)④与⑥形成的化合物的电子式为_____________ 。
(5)写出①和③两种元素的最高价氧化物对应的水化物相互反应的离子方程式:____ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ④ | ⑥ | ||||||
| 3 | ① | ② | ③ | ⑤ | ⑦ | ⑧ |
(1)在①~⑧元素中化学性质最不活泼的元素的名称是
(2)③、④、⑥三种元素中的原子半径最小的是
(3)①、②、③三种元素形成的离子,离子半径由大到小的顺序是
(4)④与⑥形成的化合物的电子式为
(5)写出①和③两种元素的最高价氧化物对应的水化物相互反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
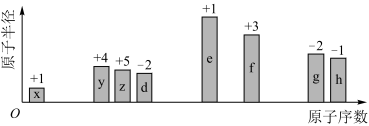
【推荐1】已知随原子序数的递增,8种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如下图所示。回答下列问题:___________ 周期第___________ 族。
(2)d、g的简单离子的半径大小(用化学式表示,下同):___________ ;g、h的最高价氧化物的水化物的酸性强弱顺序:___________ 。
(3)写出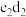 与
与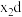 反应的化学方程式:
反应的化学方程式:___________ 。
(4)e与f相比,金属性较强的是___________ (用元素符号表示),下列事实能证明这一结论的是___________ (填字母序号)。
A.e单质的熔点比f单质的低,e单质的硬度也比f单质的小
B.e单质与冷水反应迅速,而f单质与冷水几乎不反应
C.e的最高价氧化物的水化物是强碱,而f的最高价氧化物的水化物具有两性
(2)d、g的简单离子的半径大小(用化学式表示,下同):
(3)写出
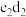 与
与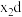 反应的化学方程式:
反应的化学方程式:(4)e与f相比,金属性较强的是
A.e单质的熔点比f单质的低,e单质的硬度也比f单质的小
B.e单质与冷水反应迅速,而f单质与冷水几乎不反应
C.e的最高价氧化物的水化物是强碱,而f的最高价氧化物的水化物具有两性
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】图中反应①是制备SiH4的一种方法,其副产物MgCl2·6NH3是优质的镁资源。回答下列问题:
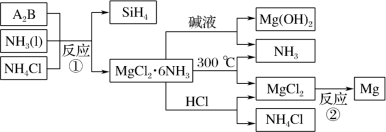
(1)MgCl2·6NH3所含元素( H元素除外)的简单离子半径由大到小的顺序为_______ 。
(2)A2B的化学式为_______ 。图中可以循环使用的物质有_______ 。
(3)为实现燃煤脱硫,向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为稳定的Mg化合物,写出该反应的化学方程式________ 。
(4)近年来,镁在汽车、航空、航天、机械制造、军事等产业中应用迅猛发展。
①写出工业上冶炼金属镁的化学方程式________ 。
②某研究性小组探究以镁条、铝片为电极,一定浓度的氢氧化钠溶液为电解质溶液构成的原电池(如下图所示),刚开始时发现电流表指针向左偏转,镁条作负极;但随后很快指针向右偏转。开始阶段,镁电极上的电极反应式为________ ,其反应类型为_______ (填“氧化”或“还原”)。随后阶段,铝电极上的电极反应式为_______ 。
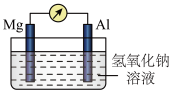
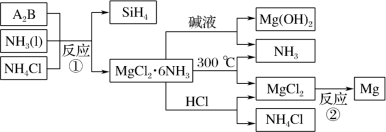
(1)MgCl2·6NH3所含元素( H元素除外)的简单离子半径由大到小的顺序为
(2)A2B的化学式为
(3)为实现燃煤脱硫,向煤中加入浆状Mg(OH)2,使燃烧产生的SO2转化为稳定的Mg化合物,写出该反应的化学方程式
(4)近年来,镁在汽车、航空、航天、机械制造、军事等产业中应用迅猛发展。
①写出工业上冶炼金属镁的化学方程式
②某研究性小组探究以镁条、铝片为电极,一定浓度的氢氧化钠溶液为电解质溶液构成的原电池(如下图所示),刚开始时发现电流表指针向左偏转,镁条作负极;但随后很快指针向右偏转。开始阶段,镁电极上的电极反应式为

您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐1】硅是带来人类文明的重要元素之一,工业上可用石英砂制备。
(1) 在元素周期表中的位置是
在元素周期表中的位置是___________ 。
(2)硅和锗( )属于同主族元素。下列预测合理的是
)属于同主族元素。下列预测合理的是___________ (填序号)。
a. 与
与 化合易于
化合易于 b. 常温下
b. 常温下 是固体
是固体
c.酸性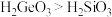 d.
d. 和
和 都可做半导体材料
都可做半导体材料
(3)高纯 可用于制造
可用于制造___________ 。
(4)下图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。
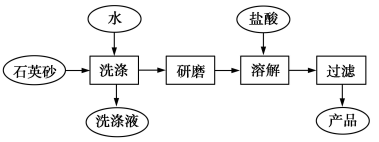
①洗涤石英砂的目的是___________ 。
②将洗净的石英砂研磨成粉末,目的是___________ 。
③在以上流程中,能否将盐酸改为 溶液,请说明理由
溶液,请说明理由___________ 。
(5)氮化硅( )是一种重要的结构陶瓷材料,可由石英与焦炭在高温的氮气流中通过以下反应制备:
)是一种重要的结构陶瓷材料,可由石英与焦炭在高温的氮气流中通过以下反应制备:
①氮化硅中氮元素的化合价___________ 。
②若生成 (标准状况),则生成氮化硅的质量是
(标准状况),则生成氮化硅的质量是___________  (保留一位小数)。
(保留一位小数)。
(1)
 在元素周期表中的位置是
在元素周期表中的位置是(2)硅和锗(
 )属于同主族元素。下列预测合理的是
)属于同主族元素。下列预测合理的是a.
 与
与 化合易于
化合易于 b. 常温下
b. 常温下 是固体
是固体c.酸性
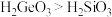 d.
d. 和
和 都可做半导体材料
都可做半导体材料(3)高纯
 可用于制造
可用于制造(4)下图是用海边的石英砂(含氯化钠、氧化铝等杂质)制备二氧化硅粗产品的工艺流程。

①洗涤石英砂的目的是
②将洗净的石英砂研磨成粉末,目的是
③在以上流程中,能否将盐酸改为
 溶液,请说明理由
溶液,请说明理由(5)氮化硅(
 )是一种重要的结构陶瓷材料,可由石英与焦炭在高温的氮气流中通过以下反应制备:
)是一种重要的结构陶瓷材料,可由石英与焦炭在高温的氮气流中通过以下反应制备:
①氮化硅中氮元素的化合价
②若生成
 (标准状况),则生成氮化硅的质量是
(标准状况),则生成氮化硅的质量是 (保留一位小数)。
(保留一位小数)。
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】下表是元素周期表的一部分,按要求填空(填元素符号 或化学式 ):
(1)写出③和⑧的单质反应产物的电子式________ 。
(2)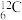 在周期表中的位置
在周期表中的位置________ ,它与氧气完全燃烧的产物的电子式________ ;
(3)在③与④的单质 中,化学性质较活泼的是________ ,判断的实验依据是________ ;
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)
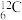 在周期表中的位置
在周期表中的位置(3)在③与④的
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】几种元素在周期表中的位置如下,用化学用语 回答下列问题:
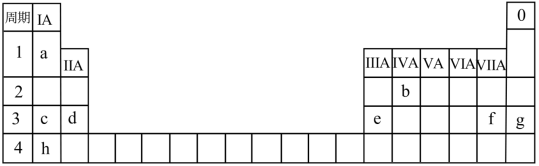
(1)表中所列元素,化学性质最不活泼的是___________ 。
(2)上图中,元素a与b形成的10 e-的分子是___________ 。
(3)元素c在空气中燃烧的产物中所含化学键有___________ 。
(4)d、e、h三种元素最高价氧化物对应水化物碱性最弱的是___________ ,其中h与水反应的化学方程式为___________ 。
(5)f单质的电子式为___________ 。
(6)德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。分析可知,铷在元素周期表中的位置是___________ ,关于铷的下列说法中正确的是___________ (填字母序号)。
a.与水反应比钠更剧烈b.单质具有很强氧化性
c. 在空气中易吸收水和二氧化碳d.RbOH的碱性比同浓度的NaOH弱
在空气中易吸收水和二氧化碳d.RbOH的碱性比同浓度的NaOH弱

(1)表中所列元素,化学性质最不活泼的是
(2)上图中,元素a与b形成的10 e-的分子是
(3)元素c在空气中燃烧的产物中所含化学键有
(4)d、e、h三种元素最高价氧化物对应水化物碱性最弱的是
(5)f单质的电子式为
(6)德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。分析可知,铷在元素周期表中的位置是
a.与水反应比钠更剧烈b.单质具有很强氧化性
c.
 在空气中易吸收水和二氧化碳d.RbOH的碱性比同浓度的NaOH弱
在空气中易吸收水和二氧化碳d.RbOH的碱性比同浓度的NaOH弱
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】下表是元素周期表的一部分,请参照元素①~⑤在表中的位置,回答下列问题:
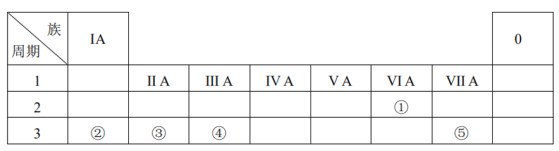
(1)①的原子结构示意图是_______ 。
(2)②、③、④三种元素的原子半径最小的是_______ (写元素符号)。
(3)②和⑤可形成离子化合物,用电子式表示其形成过程_______ 。
(4)下列事实能判断②和③的金属性强弱的是_______ (填字母,下同)。
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
(5)硒(Se)位于第四周期,与①同主族。下列推断正确的是_______ 。
a.SeO2只具有还原性
b. Se的最低负化合价是-2 价
c. Se的气态氢化物的稳定性比①的强

(1)①的原子结构示意图是
(2)②、③、④三种元素的原子半径最小的是
(3)②和⑤可形成离子化合物,用电子式表示其形成过程
(4)下列事实能判断②和③的金属性强弱的是
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
(5)硒(Se)位于第四周期,与①同主族。下列推断正确的是
a.SeO2只具有还原性
b. Se的最低负化合价是-2 价
c. Se的气态氢化物的稳定性比①的强
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】已知X、Y、Z均为元素周期表中前20号元素,X和Z位于同一周期,Y的阳离子和Z的阴离子的核外电子排布相同,Y2Z2与H2Z或XZ2反应都能生成单质气体Z2。
(1)写出元素名称:X________ ,Y________ ,Z________ 。
(2)写出下列物质的电子式:Y2Z2__________________ ,XZ2__________________ 。
(3)用电子式表示Y2Z的形成过程:____________________________ 。
(1)写出元素名称:X
(2)写出下列物质的电子式:Y2Z2
(3)用电子式表示Y2Z的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有10个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)写出下列元素符号:A_______ , C_______ ,D_______ ,E_______
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:_______ 。
(3)写出A、B两元素的最高价氧化物的水化物之间的相互反应的化学方程式:_______ 。
(4)比较C、D的最高价氧化物的水化物的酸性:(用化学式表示)_______
(1)写出下列元素符号:A
(2)A与E两元素可形成化合物,用电子式表示其化合物的形成过程:
(3)写出A、B两元素的最高价氧化物的水化物之间的相互反应的化学方程式:
(4)比较C、D的最高价氧化物的水化物的酸性:(用化学式表示)
您最近一年使用:0次





