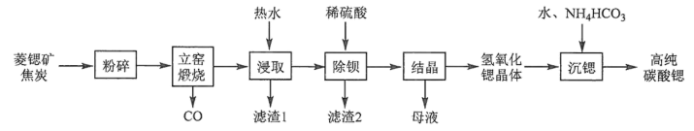
碳酸锶(SrCO3)是一种重要的工业原料,广泛用于生产锶铁氧体磁性材料。一种以菱锶矿(含80~90% SrCO3,少量MgCO3、CaCO3、BaCO3等)制备高纯碳酸锶的工艺流程如下:
Sr(OH)2在水中的溶解度
(1)元素Sr位于元素周期表第_______ 周期第_______ 族。
(2)菱锶矿、焦炭混合粉碎的目的是_______ 。
(3)“立窑煅烧”中SrCO3与焦炭反应的化学方程式为_______ 。进行煅烧反应的立窑衬里应选择_______ (填“石英砂砖”或“碱性耐火砖”)。

Sr(OH)2在水中的溶解度
| 温度/℃ | 10 | 20 | 30 | 40 | 60 | 80 | 90 | 100 |
| 溶解度/(g/100g) | 1.25 | 1.77 | 2.64 | 3.95 | 8.42 | 20.2 | 44.5 | 91.2 |
(1)元素Sr位于元素周期表第
(2)菱锶矿、焦炭混合粉碎的目的是
(3)“立窑煅烧”中SrCO3与焦炭反应的化学方程式为
2021高三·全国·专题练习 查看更多[1]
(已下线)热点10 氧化还原反应与电极反应-2021年高考化学【热点·重点·难点】专练(新高考)
更新时间:2021-03-21 22:17:24
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂(LiFePO4)。LiFePO4的一种制备方法如图。
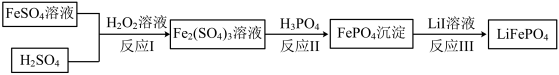
已知:H3PO4能电离出PO 。
。
(1)LiFePO4中,铁元素的化合价为_____ 。
(2)反应I中H2O2的作用是_____ 。
(3)检测反应II中铁离子是否完全反应的操作是_____ 。(离子检验常用的表达方式为:取xx试剂,向其中滴加xx,若出现xx现象,则说明xx结论。)
(4)反应Ⅲ的化学方程式是_____ 。

已知:H3PO4能电离出PO
 。
。(1)LiFePO4中,铁元素的化合价为
(2)反应I中H2O2的作用是
(3)检测反应II中铁离子是否完全反应的操作是
(4)反应Ⅲ的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
解题方法
【推荐2】二氧化氯消毒剂是国际公认的高效消毒灭菌剂。二氧化氯漂白液中常含有ClO2和Cl2两种主要成分。化学兴趣小组同学为测定某二氧化氯漂白液中ClO2的浓度,进行如下实验:
[实验I]配制250mL0.1mol/L的Na2S2O3溶液,步骤如下:
①用天平准确称取一定质量的Na2S2O3·5H2O固体,放入烧杯,用适量蒸馏水溶解;
②待溶液恢复至室温后,将烧杯中的溶液转移至250mL容量瓶中;
③用蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将每次洗涤的溶液转入容量瓶中,振荡;
④继续向容量瓶中加水至距刻度线1~2cm处,改用胶头滴管加水至刻度线;
⑤将容量瓶塞盖好,充分摇匀。
回答下列问题:
(1)容量瓶在使用前必须进行的操作是_______ 。
(2)配制溶液过程中需称量Na2S2O3·5H2O固体的质量为_______ g。
(3)配制溶液过程中,若未进行步骤③操作,则配制的溶液浓度_______ 。 填“偏高”、“偏低”或“无影响”
填“偏高”、“偏低”或“无影响”
[实验II]测定二氧化氯漂白液中ClO2浓度,步骤如下:
①量取5mL二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到25mL,再向其中加入过量KI溶液,二氧化氯漂白液中的两种成分分别发生反应:2ClO2+2KI=2KClO2+I2、Cl2+2KI=2KCl+I2
②加入淀粉作指示剂,向其中逐滴加入0.1mol/L的Na2S2O3溶液至反应恰好完全进行,过程中发生的反应为:2Na2S2O3+I2=Na2S4O6+2NaI
③加入稀硫酸调节溶液pH=3,发生反应:KClO2+4KI+2H2SO4=KCl+2K2SO4+2I2+2H2O
④再逐滴加入0.1mol/L的Na2S2O3溶液,反应恰好完全进行时,该步消耗Na2S2O3溶液20mL。
回答下列问题:
(4)用单线桥标出反应中电子转移的方向和数目:2ClO2+2KI=2KClO2+I2。_______
(5)该二氧化氯漂白液中ClO2的浓度为_______ g/L(写出计算过程)。
[实验I]配制250mL0.1mol/L的Na2S2O3溶液,步骤如下:
①用天平准确称取一定质量的Na2S2O3·5H2O固体,放入烧杯,用适量蒸馏水溶解;
②待溶液恢复至室温后,将烧杯中的溶液转移至250mL容量瓶中;
③用蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将每次洗涤的溶液转入容量瓶中,振荡;
④继续向容量瓶中加水至距刻度线1~2cm处,改用胶头滴管加水至刻度线;
⑤将容量瓶塞盖好,充分摇匀。
回答下列问题:
(1)容量瓶在使用前必须进行的操作是
(2)配制溶液过程中需称量Na2S2O3·5H2O固体的质量为
(3)配制溶液过程中,若未进行步骤③操作,则配制的溶液浓度
 填“偏高”、“偏低”或“无影响”
填“偏高”、“偏低”或“无影响”
[实验II]测定二氧化氯漂白液中ClO2浓度,步骤如下:
①量取5mL二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到25mL,再向其中加入过量KI溶液,二氧化氯漂白液中的两种成分分别发生反应:2ClO2+2KI=2KClO2+I2、Cl2+2KI=2KCl+I2
②加入淀粉作指示剂,向其中逐滴加入0.1mol/L的Na2S2O3溶液至反应恰好完全进行,过程中发生的反应为:2Na2S2O3+I2=Na2S4O6+2NaI
③加入稀硫酸调节溶液pH=3,发生反应:KClO2+4KI+2H2SO4=KCl+2K2SO4+2I2+2H2O
④再逐滴加入0.1mol/L的Na2S2O3溶液,反应恰好完全进行时,该步消耗Na2S2O3溶液20mL。
回答下列问题:
(4)用单线桥标出反应中电子转移的方向和数目:2ClO2+2KI=2KClO2+I2。
(5)该二氧化氯漂白液中ClO2的浓度为
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】某湿法炼锌的萃余液中含有 、
、 、
、 、
、 、
、 、
、 及30~60
及30~60
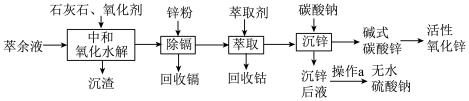
 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
已知:
回答下列问题:
(1)“中和氧化水解”时,先加入适量的石灰石调节溶液的pH为1.0;加入一定量的 ;再加入石灰石调节溶液的pH为4.0。
;再加入石灰石调节溶液的pH为4.0。
①“氧化”时, 转化为
转化为 除去,反应的离子方程式为
除去,反应的离子方程式为________ ,为提高反应速率可采取的措施_______ (举1例)。
②“沉渣”的主要成分除 、
、 外还有
外还有______ 。
③“氧化”时,若加入过量的 ,钴元素将会进入“沉渣”中,则氧化水解后的溶液中含钴微粒浓度为
,钴元素将会进入“沉渣”中,则氧化水解后的溶液中含钴微粒浓度为______  。
。
(2)“除镉”时,主要反应的离子方程式为________ 。
(3)“沉锌”时,在近中性条件下加入 可得碱式碳酸锌[
可得碱式碳酸锌[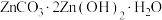 ]固体,同时产生大量的气体。
]固体,同时产生大量的气体。
①产生大量气体的原因是________ 。
②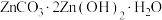 需洗涤,检验是否洗净的试剂是
需洗涤,检验是否洗净的试剂是________ 。
(4)不同质量分数的 溶液在不同温度下析出
溶液在不同温度下析出 晶体的物种如图所示。欲从含20%
晶体的物种如图所示。欲从含20%  及微量杂质的“沉锌后液”中直接析出无水
及微量杂质的“沉锌后液”中直接析出无水 ,“操作a”步骤为
,“操作a”步骤为________ 。

 、
、 、
、 、
、 、
、 、
、 及30~60
及30~60
 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图:
已知:
| 沉淀物 |  |  |  |  | 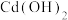 |
 | 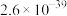 |  | 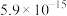 |  | 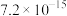 |
(1)“中和氧化水解”时,先加入适量的石灰石调节溶液的pH为1.0;加入一定量的
 ;再加入石灰石调节溶液的pH为4.0。
;再加入石灰石调节溶液的pH为4.0。①“氧化”时,
 转化为
转化为 除去,反应的离子方程式为
除去,反应的离子方程式为②“沉渣”的主要成分除
 、
、 外还有
外还有③“氧化”时,若加入过量的
 ,钴元素将会进入“沉渣”中,则氧化水解后的溶液中含钴微粒浓度为
,钴元素将会进入“沉渣”中,则氧化水解后的溶液中含钴微粒浓度为 。
。(2)“除镉”时,主要反应的离子方程式为
(3)“沉锌”时,在近中性条件下加入
 可得碱式碳酸锌[
可得碱式碳酸锌[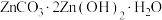 ]固体,同时产生大量的气体。
]固体,同时产生大量的气体。①产生大量气体的原因是
②
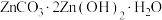 需洗涤,检验是否洗净的试剂是
需洗涤,检验是否洗净的试剂是(4)不同质量分数的
 溶液在不同温度下析出
溶液在不同温度下析出 晶体的物种如图所示。欲从含20%
晶体的物种如图所示。欲从含20%  及微量杂质的“沉锌后液”中直接析出无水
及微量杂质的“沉锌后液”中直接析出无水 ,“操作a”步骤为
,“操作a”步骤为
您最近一年使用:0次
【推荐1】锰酸锂( )是锂电池的正极材料,有望取代
)是锂电池的正极材料,有望取代 。一种以废旧电池正极材料(主要成分为
。一种以废旧电池正极材料(主要成分为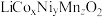 ,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备
,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备 的流程如下:
的流程如下:
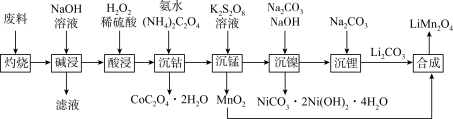
回答下列问题:
(1)Ni位于元素周期表中___________ 区。
(2) 的结构为:
的结构为: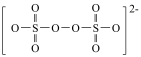 ,用“□”圈出
,用“□”圈出 中体现强氧化性的基团
中体现强氧化性的基团___________ 。
(3)“灼烧”的目的是除去___________ 、___________ 。
(4)根据“酸浸”前后物质价态的变化,推测双氧水发生反应的产物是___________ 。
(5)“沉锰”过程中,溶液先变为紫红色,一段时间后紫红色褪去。已知:加入 溶液之前,锰以
溶液之前,锰以 形式存在且溶液为弱酸性。则溶液变为紫红色的原因是
形式存在且溶液为弱酸性。则溶液变为紫红色的原因是___________ (用离子方程式表示)。由流程推测,“紫红色褪去”后,还可观察到的实验现象是___________ 。
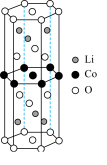
(6) 材料在脱锂过程中形成的某种晶体为六方晶系,结构如图。晶胞Li、Co、O的个数比为
材料在脱锂过程中形成的某种晶体为六方晶系,结构如图。晶胞Li、Co、O的个数比为___________ 。
 )是锂电池的正极材料,有望取代
)是锂电池的正极材料,有望取代 。一种以废旧电池正极材料(主要成分为
。一种以废旧电池正极材料(主要成分为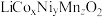 ,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备
,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备 的流程如下:
的流程如下:
回答下列问题:
(1)Ni位于元素周期表中
(2)
 的结构为:
的结构为: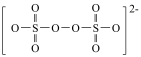 ,用“□”圈出
,用“□”圈出 中体现强氧化性的基团
中体现强氧化性的基团(3)“灼烧”的目的是除去
(4)根据“酸浸”前后物质价态的变化,推测双氧水发生反应的产物是
(5)“沉锰”过程中,溶液先变为紫红色,一段时间后紫红色褪去。已知:加入
 溶液之前,锰以
溶液之前,锰以 形式存在且溶液为弱酸性。则溶液变为紫红色的原因是
形式存在且溶液为弱酸性。则溶液变为紫红色的原因是(6)
 材料在脱锂过程中形成的某种晶体为六方晶系,结构如图。晶胞Li、Co、O的个数比为
材料在脱锂过程中形成的某种晶体为六方晶系,结构如图。晶胞Li、Co、O的个数比为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】元素周期表是学习和研究化学的重要工具。
(1)原子序数为 1~18 的元素在元素周期表中的位置如下表所示。
①Al原子的核电荷数为____ 。②钠离子的结构示意图为____ 。
③周期表中磷元素的有关信息为 ,图中“30.97”所表示的含义是
,图中“30.97”所表示的含义是____ 。
(2)根据周期表体现的结构与性质之间的关系,某同学构建了铜及其化合物的“化合价﹣物质类别”关系图。
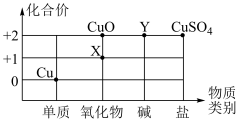
①写出物质 X 的化学式:________________ 。
②写出由物质 Y 转化为 CuSO4的化学反应方程式:_______________ 。
③氧化还原反应是化学学习中的核心概念,对氧化还原反应的定义为有化合价升降的反应,下列转化中属于氧化还原反应的是_________________ 。
A、Cu—X B、X—CuO C、CuO—Y D、Y—CuSO4
(1)原子序数为 1~18 的元素在元素周期表中的位置如下表所示。
| 第1周期 | H | He | ||||||
| 第2周期 | Li | Be | B | C | N | O | F | Ne |
| 第3周期 | Na | Mg | Al | Si | P | S | Cl | Ar |
①Al原子的核电荷数为
③周期表中磷元素的有关信息为
 ,图中“30.97”所表示的含义是
,图中“30.97”所表示的含义是(2)根据周期表体现的结构与性质之间的关系,某同学构建了铜及其化合物的“化合价﹣物质类别”关系图。

①写出物质 X 的化学式:
②写出由物质 Y 转化为 CuSO4的化学反应方程式:
③氧化还原反应是化学学习中的核心概念,对氧化还原反应的定义为有化合价升降的反应,下列转化中属于氧化还原反应的是
A、Cu—X B、X—CuO C、CuO—Y D、Y—CuSO4
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐3】已知元素A、B、C、D的原子结构示意图分别为:

请回答下列问题(用元素符号回答)。
(1)写出元素的元素符号:A___________ 、B___________ 、C___________ 、D___________ 。
(2)元素A位于周期表的第___________ 周期第___________ 族。
(3)属于同周期元素的是___________ 、___________ 和___________ ,属于同主族元素的是___________ 和___________ 。
(4)属于卤族元素的是___________ 和___________ 。

请回答下列问题(用元素符号回答)。
(1)写出元素的元素符号:A
(2)元素A位于周期表的第
(3)属于同周期元素的是
(4)属于卤族元素的是
您最近一年使用:0次



