锰酸锂( )是锂电池的正极材料,有望取代
)是锂电池的正极材料,有望取代 。一种以废旧电池正极材料(主要成分为
。一种以废旧电池正极材料(主要成分为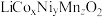 ,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备
,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备 的流程如下:
的流程如下:
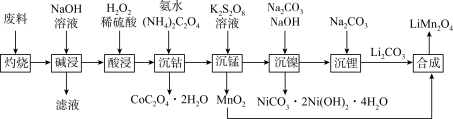
回答下列问题:
(1)Ni位于元素周期表中___________ 区。
(2) 的结构为:
的结构为: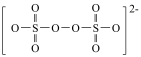 ,用“□”圈出
,用“□”圈出 中体现强氧化性的基团
中体现强氧化性的基团___________ 。
(3)“灼烧”的目的是除去___________ 、___________ 。
(4)根据“酸浸”前后物质价态的变化,推测双氧水发生反应的产物是___________ 。
(5)“沉锰”过程中,溶液先变为紫红色,一段时间后紫红色褪去。已知:加入 溶液之前,锰以
溶液之前,锰以 形式存在且溶液为弱酸性。则溶液变为紫红色的原因是
形式存在且溶液为弱酸性。则溶液变为紫红色的原因是___________ (用离子方程式表示)。由流程推测,“紫红色褪去”后,还可观察到的实验现象是___________ 。
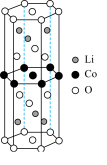
(6) 材料在脱锂过程中形成的某种晶体为六方晶系,结构如图。晶胞Li、Co、O的个数比为
材料在脱锂过程中形成的某种晶体为六方晶系,结构如图。晶胞Li、Co、O的个数比为___________ 。
 )是锂电池的正极材料,有望取代
)是锂电池的正极材料,有望取代 。一种以废旧电池正极材料(主要成分为
。一种以废旧电池正极材料(主要成分为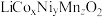 ,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备
,其中Co为+3价,还含少量铝箔、炭黑和有机黏合剂)为原料制备 的流程如下:
的流程如下:
回答下列问题:
(1)Ni位于元素周期表中
(2)
 的结构为:
的结构为: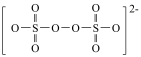 ,用“□”圈出
,用“□”圈出 中体现强氧化性的基团
中体现强氧化性的基团(3)“灼烧”的目的是除去
(4)根据“酸浸”前后物质价态的变化,推测双氧水发生反应的产物是
(5)“沉锰”过程中,溶液先变为紫红色,一段时间后紫红色褪去。已知:加入
 溶液之前,锰以
溶液之前,锰以 形式存在且溶液为弱酸性。则溶液变为紫红色的原因是
形式存在且溶液为弱酸性。则溶液变为紫红色的原因是(6)
 材料在脱锂过程中形成的某种晶体为六方晶系,结构如图。晶胞Li、Co、O的个数比为
材料在脱锂过程中形成的某种晶体为六方晶系,结构如图。晶胞Li、Co、O的个数比为
更新时间:2024-04-09 14:05:00
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐1】已知B为碱性氧化物,D为淡黄色固体粉末,F为医疗上治疗胃酸过多的一种药剂;物质的转化关系如图所示,请回答下列问题:

(1)请写出下列物质的化学式:A_____ 、F______ 。
(2)请写出下列反应的方程式:
①D→E(写化学方程式):_____ ;
②C→E(写在水溶液中进行的离子方程式):_____ 。
(3)将4.6gA投入47.8g水中,所得溶液中溶质的质量分数为______ (用百分数表示,保留一位小数)。若把A投入盛有CuSO4的溶液中,溶液中出现______ (填沉淀颜色)沉淀。

(1)请写出下列物质的化学式:A
(2)请写出下列反应的方程式:
①D→E(写化学方程式):
②C→E(写在水溶液中进行的离子方程式):
(3)将4.6gA投入47.8g水中,所得溶液中溶质的质量分数为
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐2】一氧化二氯( )为国际公认的高效安全灭菌消毒剂之一,其部分性质如下:
)为国际公认的高效安全灭菌消毒剂之一,其部分性质如下:
实验室制备原理: 。
。
现用如图所示装置设计实验制备少量 。(已知实验室制
。(已知实验室制 的方法:
的方法: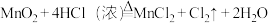 )
)

(1)仪器组装完成、加药品前应进行的实验操作为_______ 。
(2)装置A中发生反应的离子方程式为_______ 。
(3)装置B中盛放的试剂是_______ 溶液。
(4)E装置中冰水混合物的作用_______ 。
(5)反应结束后,请设计简单实验证明装置C中的残留固体中含有NaCl,_______ 。
 )为国际公认的高效安全灭菌消毒剂之一,其部分性质如下:
)为国际公认的高效安全灭菌消毒剂之一,其部分性质如下:| 物理性质 | 化学性质 |
常温下, 是棕黄色有刺激性气味的气体;熔点:-120.6℃:沸点2.0℃ 是棕黄色有刺激性气味的气体;熔点:-120.6℃:沸点2.0℃ |  热稳定性差,常温下即可分解;易溶于水,同时反应生成次氯酸。 热稳定性差,常温下即可分解;易溶于水,同时反应生成次氯酸。 |
 。
。现用如图所示装置设计实验制备少量
 。(已知实验室制
。(已知实验室制 的方法:
的方法: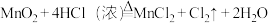 )
)
(1)仪器组装完成、加药品前应进行的实验操作为
(2)装置A中发生反应的离子方程式为
(3)装置B中盛放的试剂是
(4)E装置中冰水混合物的作用
(5)反应结束后,请设计简单实验证明装置C中的残留固体中含有NaCl,
您最近半年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】I.铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)是提取氧化铝的原料,主要工艺流程如下:
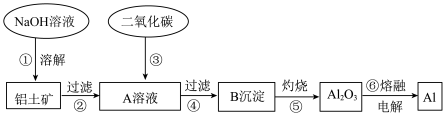
注:SiO2在该条件下与NaOH反应转化为铝硅酸钠沉淀。
(1)第①步反应后得到的A溶液中溶质的主要成分为___________ 。
(2)第②步“过滤”中产生的滤渣中,除铝硅酸钠外还有___________ (填化学式)。
(3)第③步反应的产物为沉淀B与NaHCO3,此步反应的离子方程式是___________ 。
(4)某学习小组利用上述工艺流程从100g铝土矿(Al2O3的质量分数为85%)中提取氧化铝,再利用电解得到单质铝。最终得到的单质铝质量为___________(请填入字母)。
Ⅱ.某研究人员将Na2O2与Al的混合物溶于足量的水中,充分反应后得到澄清溶液,同时产生气体3.5g;向上述澄清溶液中滴加100mL的7mol/L盐酸,白色沉淀先生成后又恰好溶解。
(5)原混合物中Na2O2与Al的物质的量之比为___________ (请填写最简整数比)。

注:SiO2在该条件下与NaOH反应转化为铝硅酸钠沉淀。
(1)第①步反应后得到的A溶液中溶质的主要成分为
(2)第②步“过滤”中产生的滤渣中,除铝硅酸钠外还有
(3)第③步反应的产物为沉淀B与NaHCO3,此步反应的离子方程式是
(4)某学习小组利用上述工艺流程从100g铝土矿(Al2O3的质量分数为85%)中提取氧化铝,再利用电解得到单质铝。最终得到的单质铝质量为___________(请填入字母)。
| A.小于45g | B.等于45g | C.大于45g | D.无法确定 |
Ⅱ.某研究人员将Na2O2与Al的混合物溶于足量的水中,充分反应后得到澄清溶液,同时产生气体3.5g;向上述澄清溶液中滴加100mL的7mol/L盐酸,白色沉淀先生成后又恰好溶解。
(5)原混合物中Na2O2与Al的物质的量之比为
您最近半年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】三水锑酸钠( )常用作显像管、光学玻璃和各种高级玻璃的澄清剂,一种以锑矿(含
)常用作显像管、光学玻璃和各种高级玻璃的澄清剂,一种以锑矿(含 、
、 、
、 、
、 等)为原料合成三水锑酸钠的工艺流程如下图。
等)为原料合成三水锑酸钠的工艺流程如下图。
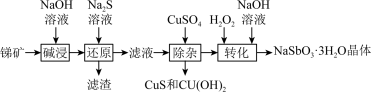
已知:ⅰ.常温下,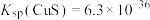 、
、 ;
;
ⅱ. 冷水中不溶,溶于硫化钠溶液;
冷水中不溶,溶于硫化钠溶液; 冷水中不溶,热水中发生水解形成胶体。
冷水中不溶,热水中发生水解形成胶体。
(1)“碱浸”和“还原”中加快锑矿浸出速率的具体措施为___________ (任写两条)。
(2)“滤渣”中除了含有 外,还含有
外,还含有___________ (填化学式)。
(3)“还原”步骤中 溶液的作用为
溶液的作用为___________ ; 转化为
转化为 的离子方程式为
的离子方程式为___________ 。
(4)“除杂”步骤后溶液的 ,则此时溶液中
,则此时溶液中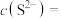
___________ 。
(5)“转化”时发生反应的化学方程式为___________ ;该过程中加入 溶液的目的是
溶液的目的是___________ 。
 )常用作显像管、光学玻璃和各种高级玻璃的澄清剂,一种以锑矿(含
)常用作显像管、光学玻璃和各种高级玻璃的澄清剂,一种以锑矿(含 、
、 、
、 、
、 等)为原料合成三水锑酸钠的工艺流程如下图。
等)为原料合成三水锑酸钠的工艺流程如下图。
已知:ⅰ.常温下,
 、
、 ;
;ⅱ.
 冷水中不溶,溶于硫化钠溶液;
冷水中不溶,溶于硫化钠溶液; 冷水中不溶,热水中发生水解形成胶体。
冷水中不溶,热水中发生水解形成胶体。(1)“碱浸”和“还原”中加快锑矿浸出速率的具体措施为
(2)“滤渣”中除了含有
 外,还含有
外,还含有(3)“还原”步骤中
 溶液的作用为
溶液的作用为 转化为
转化为 的离子方程式为
的离子方程式为(4)“除杂”步骤后溶液的
 ,则此时溶液中
,则此时溶液中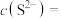
(5)“转化”时发生反应的化学方程式为
 溶液的目的是
溶液的目的是
您最近半年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】KMnO4是一种用途广泛的氧化剂,可由软锰矿(主要成分为MnO2)通过下列方法制备:
a.软锰矿与过量KOH、KClO3固体熔融生成K2MnO4;
b.溶解、过滤后将滤液酸化,使K2MnO4完全转化为MnO2和KMnO4;
c.滤去MnO2,将滤液浓缩、结晶得到深紫色的KMnO4产品。
测定KMnO4产品的纯度可用标准Na2S2O3溶液进行测定。
(1)写出a的化学方程式_______ 。
(2)写出b的离子方程式_______ 。
(3)配制250mL0.1000 mol∙L−1标准Na2S2O3溶液:
①用托盘天平称取_______ g硫代硫酸钠固体样品,将其在_______ 中用新煮沸并冷却的蒸馏水溶解,完全溶解后,全部转移至_______ 中,加蒸馏水至溶液的凹液面最低处与刻度线相切。
②若配制中未洗涤烧杯及玻璃棒,则溶液浓度_______ (填“偏大”、“偏小”或“无影响”,下同),若定容时仰视刻度线,则溶液浓度_______ 。
(4)测定KMnO4产品的纯度:取3份0.6000g上述制得的KMnO4产品,酸化后分别用0.100 mol∙L−1标准Na2S2O3溶液进行反应,有关离子方程式为 。记录所消耗Na2S2O3溶液的体积为:
。记录所消耗Na2S2O3溶液的体积为:
计算该KMnO4产品的纯度为_______ 。(保留小数点后两位)
a.软锰矿与过量KOH、KClO3固体熔融生成K2MnO4;
b.溶解、过滤后将滤液酸化,使K2MnO4完全转化为MnO2和KMnO4;
c.滤去MnO2,将滤液浓缩、结晶得到深紫色的KMnO4产品。
测定KMnO4产品的纯度可用标准Na2S2O3溶液进行测定。
(1)写出a的化学方程式
(2)写出b的离子方程式
(3)配制250mL0.1000 mol∙L−1标准Na2S2O3溶液:
①用托盘天平称取
②若配制中未洗涤烧杯及玻璃棒,则溶液浓度
(4)测定KMnO4产品的纯度:取3份0.6000g上述制得的KMnO4产品,酸化后分别用0.100 mol∙L−1标准Na2S2O3溶液进行反应,有关离子方程式为
 。记录所消耗Na2S2O3溶液的体积为:
。记录所消耗Na2S2O3溶液的体积为:| 测定次数 | 第1次 | 第2次 | 第3次 |
| V[Na2S2O3(aq)]/mL | 20.00 | 19.90 | 21.10 |
您最近半年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】钛是一种重要的金属,以钛铁矿[主要成分为钛酸亚铁 ,还含有少量
,还含有少量 ]为原料制备钛的工艺流程如图所示。
]为原料制备钛的工艺流程如图所示。
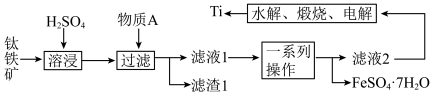
(1)“溶浸”过程中生成了 ,其中
,其中 的化合价为
的化合价为_______________ ,“溶浸”过程发生的主要反应的化学方程式为_______________ 。
(2)物质A为单质,化学式为_______________ ,“一系列操作”为蒸发浓缩、_______________ 和过滤.
(3)将少量 溶于水,加入一定量的
溶于水,加入一定量的 溶液,可制得
溶液,可制得 ,写出反应的离子方程式为
,写出反应的离子方程式为_______________ 。
(4)若反应后的溶液中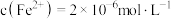 ,则溶液中
,则溶液中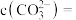
_______________  (已知:常温下
(已知:常温下 饱和溶液浓度为
饱和溶液浓度为 )。
)。
 ,还含有少量
,还含有少量 ]为原料制备钛的工艺流程如图所示。
]为原料制备钛的工艺流程如图所示。
(1)“溶浸”过程中生成了
 ,其中
,其中 的化合价为
的化合价为(2)物质A为单质,化学式为
(3)将少量
 溶于水,加入一定量的
溶于水,加入一定量的 溶液,可制得
溶液,可制得 ,写出反应的离子方程式为
,写出反应的离子方程式为(4)若反应后的溶液中
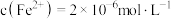 ,则溶液中
,则溶液中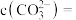
 (已知:常温下
(已知:常温下 饱和溶液浓度为
饱和溶液浓度为 )。
)。
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。下表是元素周期表的一部分。
(2)a-h元素的最高价氧化物对应的水化物中,酸性最强的是___________ (填化学式)。
(3)b元素有三种稳定核素,其式量分别为16、17、18,则三种核素的中子数之比为___________ 。
(4)c、g、h三种元素形成的气态氢化物中,稳定性最小的物质的结构式是___________ 。
(5)d元素的简单离子的结构示意图为___________ 。
(6)d的最高价氧化物对应水化物与f的最高价氧化物对应水化物的溶液反应的离子方程式为___________ 。
(7)若d单质着火,可用于灭火的物质是___________。
(8)下列关于元素周期表的叙述正确的是___________。
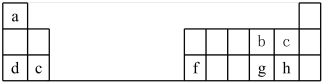
| A.第三周期第6族 | B.第三周期VI主族 |
| C.第三周期第6A族 | D.第三周期VIA族 |
(3)b元素有三种稳定核素,其式量分别为16、17、18,则三种核素的中子数之比为
(4)c、g、h三种元素形成的气态氢化物中,稳定性最小的物质的结构式是
(5)d元素的简单离子的结构示意图为
(6)d的最高价氧化物对应水化物与f的最高价氧化物对应水化物的溶液反应的离子方程式为
(7)若d单质着火,可用于灭火的物质是___________。
| A.自来水 | B.CO2 | C.干沙子 | D.湿抹布 |
| A.元素周期表中所含元素最多的族是BVII族 |
| B.IA族的元素全部是金属元素 |
| C.在元素周期表中金属与非金属的分界处可以找到半导体材料 |
| D.只有IIA族元素的原子最外层有2个电子 |
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】钙和铜合金可用作电解制钙的阴极电极材料,回答下列问题:
(1)Cu在元素周期表中的位置是_______ ,基态Cu2+核外电子填充的最高能级符号为_____ 。
(2)CaCO3高温分解可制得CaO。CaO与C在一定条件下可生成CaC2,CaC2与水反应生成Ca(OH)2和一种4原子气体分子。
①该气体分子的电子式______ ,该气体分子中σ键与π键的数目之比为______ 。
②C原子未成对电子的数目为______ 。
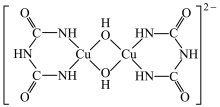
(3)在碱性溶液中,缩二脲HN(CONH2)2与CuSO4反应得到一种特征紫色物质,其结构如下图所示,该反应原理可用于检验蛋白质或其他含肽键的化合物。______ 、_______ 。
(1)Cu在元素周期表中的位置是
(2)CaCO3高温分解可制得CaO。CaO与C在一定条件下可生成CaC2,CaC2与水反应生成Ca(OH)2和一种4原子气体分子。
①该气体分子的电子式
②C原子未成对电子的数目为
(3)在碱性溶液中,缩二脲HN(CONH2)2与CuSO4反应得到一种特征紫色物质,其结构如下图所示,该反应原理可用于检验蛋白质或其他含肽键的化合物。
您最近半年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。表中列出了a~g 7种元素在周期表中的位置。
(1)a的元素符号是_______ 。
(2)写出c单质与b的最高价氧化物水化物反应的离子方程式_______ 。
(3)d、e的最高价氧化物对应的水化物中,酸性较强的是_______ 。(填化学式)
(4)已知硒(Se)与d同主族,且位于d下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是_______ 。
① 其单质在常温下呈固态
② SeO2既有氧化性又有还原性
③ 最高价氧化物对应的水化物的化学式为H2SeO3
④ 非金属性比e元素的强
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | a | |||||||
| 3 | b | c | d | e |
(2)写出c单质与b的最高价氧化物水化物反应的离子方程式
(3)d、e的最高价氧化物对应的水化物中,酸性较强的是
(4)已知硒(Se)与d同主族,且位于d下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
① 其单质在常温下呈固态
② SeO2既有氧化性又有还原性
③ 最高价氧化物对应的水化物的化学式为H2SeO3
④ 非金属性比e元素的强
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
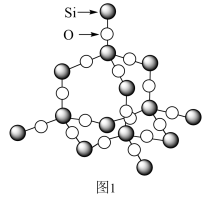
【推荐1】硅因为具有半导体的性质被认为是一种比较特殊的非金属元素,它的单质是硬度较大的非金属单质。铬单质为钢灰色金属,是自然界硬度最大的金属。
(1)若铬的一种同位素原子核内有28个中子,试写出该同位素原子的原子符号,写出基态铬原子的核外电子排布_______ 。
(2)与硅同周期的金属第一电离能由大到小排列:_______ 。与硅同周期的非金属电负性由小到大排列:_______ 。
(3)图2为二氧化硅的晶胞示意图,由图可知,二氧化硅是_______ (选填“原子晶体”、“分子晶体”或“离子晶体”,下同)。与硅同主族的元素碳的氧化物干冰是_______ 。1mol二氧化硅晶体所含有的σ键个数为_______ 。1mol的乙炔含有π键的个数为_______ 。
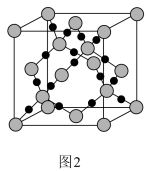
(4)已知二氧化硅的晶胞参数为anm,计算SiO2的密度_______ g/cm3。(列出计算式)

(1)若铬的一种同位素原子核内有28个中子,试写出该同位素原子的原子符号,写出基态铬原子的核外电子排布
(2)与硅同周期的金属第一电离能由大到小排列:
(3)图2为二氧化硅的晶胞示意图,由图可知,二氧化硅是

(4)已知二氧化硅的晶胞参数为anm,计算SiO2的密度
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】砷化铟(InAs)是一种优良的半导体化合物,有广泛用途。
(1)基态In的价层电子排布式为5s25p1,In在周期表中的位置是____________ 。
(2)在Ar保护下分别将InCl3和AsCl3在气化室中加热转化为蒸气,在反应室中混合反应,即可得到橘黄色的InAs晶体。已知:AsCl3和InCl3均为分子晶体。AsCl3沸点为130℃,InCl3沸点为500℃
①33As简化的电子排布式为___________ 。
②AsCl3分子的空间结构为___________ 。
③AsCl3沸点低于InCl3沸点的原因是___________ 。
④InCl3晶体中分子间存在配位键,配位原子是___________ 。
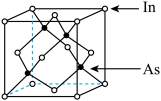
(3)InAs为原子之间以共价键的成键方式结合而成的晶体,其晶胞结构如图所示。已知该晶胞棱长为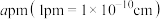 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,InAs的摩尔质量为Mg·mol-1,则该晶体的密度
,InAs的摩尔质量为Mg·mol-1,则该晶体的密度
___________ g·cm-3。
(1)基态In的价层电子排布式为5s25p1,In在周期表中的位置是
(2)在Ar保护下分别将InCl3和AsCl3在气化室中加热转化为蒸气,在反应室中混合反应,即可得到橘黄色的InAs晶体。已知:AsCl3和InCl3均为分子晶体。AsCl3沸点为130℃,InCl3沸点为500℃

①33As简化的电子排布式为
②AsCl3分子的空间结构为
③AsCl3沸点低于InCl3沸点的原因是
④InCl3晶体中分子间存在配位键,配位原子是
(3)InAs为原子之间以共价键的成键方式结合而成的晶体,其晶胞结构如图所示。已知该晶胞棱长为
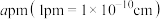 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,InAs的摩尔质量为Mg·mol-1,则该晶体的密度
,InAs的摩尔质量为Mg·mol-1,则该晶体的密度
您最近半年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】钛酸锌(ZnTiO3)是一种抗菌涂料,应用于人造骨骼等生物移植技术。回答下列问题:
(1)基态Zn原子的电子占据能量最高的能层符号为_____________ ,与Zn同周期的所有副族元素的基态原子中,最外层电子数与Zn相同的元素有___________ 种
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物。则电负性C____ B(选填“>或“<”);第一电离能N>O,原因是__________________________________________ 。
(3)ZnTiO3与80%H2SO4反应可生成TiOSO4。
① 的空间构型为
的空间构型为_____________ ,其中硫原子采用____________ 杂化。
②与 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为_________________ (任写一种即可)
(4)Zn与S所形成化合物晶体的晶胞如图所示。

①与Zn原子距离最近的Zn原子有___________ 个。
②该化合物的化学式为_________________________________ 。
③已知该晶体的晶胞参数为a×10-12m,阿伏加 德罗常数为NA。则该晶体的密度为__________________ g/cm3(列式即可)
(1)基态Zn原子的电子占据能量最高的能层符号为
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物。则电负性C
(3)ZnTiO3与80%H2SO4反应可生成TiOSO4。
①
 的空间构型为
的空间构型为②与
 互为等电子体的分子的化学式为
互为等电子体的分子的化学式为(4)Zn与S所形成化合物晶体的晶胞如图所示。

①与Zn原子距离最近的Zn原子有
②该化合物的化学式为
③已知该晶体的晶胞参数为a×10-12m,阿伏加 德罗常数为NA。则该晶体的密度为
您最近半年使用:0次



